
Darmstadtium
Acerca de este escuelas selección Wikipedia
Esta selección Escuelas fue originalmente elegido por SOS para las escuelas en el mundo en desarrollo que no tienen acceso a Internet. Está disponible como una descarga intranet. El patrocinio de los niños ayuda a los niños en el mundo en desarrollo para aprender también.
| Darmstadtium | |||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
110 Ds | |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| Apariencia | |||||||||||||||||||||||||||||||||||||
| desconocido | |||||||||||||||||||||||||||||||||||||
| Propiedades generales | |||||||||||||||||||||||||||||||||||||
| Nombre, símbolo, número | darmstadtium, Ds, 110 | ||||||||||||||||||||||||||||||||||||
| Pronunciación | / d ɑr m ʃ t ɑː t yo ə m / darm- SHTAHT -ee-əm | ||||||||||||||||||||||||||||||||||||
| Categoría metálico | desconocido pero probablemente un metal de transición | ||||||||||||||||||||||||||||||||||||
| Grupo, período, bloque | 10, 7, d | ||||||||||||||||||||||||||||||||||||
| Peso atómico estándar | [281] | ||||||||||||||||||||||||||||||||||||
| Configuración electrónica | [ Rn ] 5f 14 6d 8 7s 2 (Valor de referencia) 2, 8, 18, 32, 32, 16, 2 (Valor de referencia) ![Capas de electrones de darmstadtium (2, 8, 18, 32, 32, 16, 2 (prevista) [2])](../../images/1190/119044.png) | ||||||||||||||||||||||||||||||||||||
| Historia | |||||||||||||||||||||||||||||||||||||
| Descubrimiento | Gesellschaft für Schwerionenforschung (1994) | ||||||||||||||||||||||||||||||||||||
| Propiedades físicas | |||||||||||||||||||||||||||||||||||||
| Fase | sólido (prevista) | ||||||||||||||||||||||||||||||||||||
| Densidad (cerca rt) | 34.8 (prevista) g · cm -3 | ||||||||||||||||||||||||||||||||||||
| Propiedades atómicas | |||||||||||||||||||||||||||||||||||||
| Estados de oxidación | 8, 6, 4, 2, 0 (valor de referencia) | ||||||||||||||||||||||||||||||||||||
| Energías de ionización ( más) | Primero: 955,2 (estimado) kJ · mol -1 | ||||||||||||||||||||||||||||||||||||
| Segundo: 1891.1 (estimado) kJ · mol -1 | |||||||||||||||||||||||||||||||||||||
| Tercero: 3029.6 (estimado) kJ · mol -1 | |||||||||||||||||||||||||||||||||||||
| Radio atómico | 118 (estimado) pm | ||||||||||||||||||||||||||||||||||||
| Radio covalente | 128 (estimado) pm | ||||||||||||||||||||||||||||||||||||
| Miscelánea | |||||||||||||||||||||||||||||||||||||
| Número de registro del CAS | 54083-77-1 | ||||||||||||||||||||||||||||||||||||
| La mayoría de los isótopos estables | |||||||||||||||||||||||||||||||||||||
| Artículo principal: Los isótopos de darmstadtium | |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
Darmstadtium es un elemento químico con el símbolo de Ds y número atómico 110. Es un extremadamente radioactivo elemento sintético (un elemento que se puede crear en un laboratorio pero no se encuentra en la naturaleza). La conocida más estable isótopo , darmstadtium-281, tiene una vida media de aproximadamente 11 segundos, pero es posible que esta isótopo darmstadtium puede tener un isómero con una vida media más larga, 3,7 minutos. Darmstadtium primero fue creado en 1994 por la GSI cerca Darmstadt, Alemania. Fue nombrado después de la ciudad de Darmstadt, donde fue descubierto.
En la tabla periódica , es una d-bloque Transactínido. Es un miembro de la Séptimo período y se coloca en el grupo 10 elementos, aunque no hay experimentos químicos todavía no se han llevado a cabo para confirmar que se comporta como el más pesado homólogo de platino en el grupo 10. Darmstadtium se calcula que tiene propiedades similares a las de sus homólogos más ligeros, níquel , paladio y platino.
Historia
Descubrimiento
Darmstadtium era primero creado el 9 de noviembre de 1994, en el Instituto de Investigación de Iones Pesados (Gesellschaft für Schwerionenforschung) en Darmstadt, Alemania , por Peter Armbruster y Gottfried Münzenberg, bajo la dirección de Sigurd Hofmann. El equipo bombardeó un plomo blanco -208 con núcleos acelerados de níquel-62 y se detecta un solo átomo del isótopo darmstadtium-269:
- 208
82 Pb + 62
28 Ni → 269
110 Ds + 1
0 n
En la misma serie de experimentos, el mismo equipo también llevó a cabo la reacción usando más pesados níquel-64 iones. Durante dos carreras, 9 átomos de 271 Ds se convincentemente detectados por correlación con conocidas propiedades de desintegración hija:
- 208
82 Pb + 64
28 Ni → 271
110 Ds + 1
0 n
La Grupo de Trabajo Conjunto de IUPAC / IUPAP (PTC) reconoció que el equipo GSI como descubridores en su informe de 2001.
Naming
El nombre darmstadtium (Ds) fue sugerido por el equipo de GSI en honor de la ciudad de Darmstadt, donde se descubrió el elemento. El equipo GSI originalmente también consideró nombrar el elemento wixhausium, después de que el suburbio de Darmstadt conocido como Wixhausen donde se descubrió el elemento, pero finalmente se decidió por darmstadtium. El nuevo nombre fue recomendado oficialmente por IUPAC el 16 de agosto de 2003.
Nucleosíntesis
Elementos súper pesados como darmstadtium se producen mediante el bombardeo de elementos más ligeros en aceleradores de partículas que inducen reacciones de fusión. Considerando que la mayoría de los isótopos de darmstadtium pueden sintetizarse directamente de esta manera, algunos otros más pesados sólo se han observado como productos de desintegración de elementos con mayores números atómicos .
Dependiendo de las energías involucradas, los primeros están separados en "caliente" y "frío". En las reacciones de fusión en caliente,, proyectiles de alta energía muy ligeros son acelerados hacia objetivos muy pesados ( actínidos ), dando lugar a núcleos compuestos en energía de alta excitación (~ 40-50 MeV) que puede evaporarse ya sea de fisión o varios 3 a 5) neutrones (. En las reacciones de fusión en frío, los núcleos condensados producidos tienen una energía de excitación relativamente baja (~ 10-20 MeV), que disminuye la probabilidad de que estos productos serán sometidos a las reacciones de fisión. Mientras los núcleos fundidos se enfríen a la estado fundamental, que requieren emisión de sólo uno o dos neutrones, y por lo tanto, permite la generación de productos más ricos en neutrones. Este último es un concepto diferente de la de la fusión nuclear, donde se reivindica que deberían alcanzarse en condiciones de temperatura ambiente (ver fusión fría).
Fusión fría
Antes de la primera síntesis exitosa de darmstadtium en 1994 por la Equipo GSI, los científicos de GSI también trató de sintetizar darmstadtium bombardeando plomo-208 con el níquel-64 en 1986. No se identificaron átomos darmstadtium. Después de una actualización de sus instalaciones, el equipo de GSI detectó exitosamente 9 átomos de 271 Ds en dos carreras de su experimento descubrimiento en 1994. Esta reacción se repitió con éxito en 2000 por GSI (4 átomos), en 2000 y 2004 por la Laboratorio Nacional Lawrence Berkeley (LBNL) (9 átomos en total) y en 2002 por RIKEN (14 átomos). El equipo GSI estudió la reacción análoga con el níquel-62 en lugar de níquel-64 en 1994 como parte de su descubrimiento experimento. Se detectaron tres átomos de 269 Ds. Una cuarta cadena de desintegración se midió pero se retrae posteriormente.
Además de las reacciones oficiales de descubrimiento, en octubre-noviembre de 2000, el equipo de GSI estudió también la reacción análoga utilizando un blanco de plomo-207 con el fin de sintetizar el nuevo isótopo 270 Ds. Tuvieron éxito en la síntesis de 8 átomos de 270 Ds, relativa a un isómero estado fundamental, 270 Ds, y un alto vuelta estado metaestable, 270m Ds.
En 1986, un equipo de la Instituto Conjunto de Investigación Nuclear (ICIN) en Dubna, Rusia , estudió la reacción:
- 209
83 Bi + 59
27 Co → 267
110 Ds + 1
0 n
Fueron incapaces de detectar cualquier átomos darmstadtium. En 1995, el equipo de LBNL informó que habían tenido éxito en la detección de un solo átomo de 267 Ds utilizando esta reacción. Sin embargo, no se midieron varios decaimientos y se requiere más investigación para confirmar este hallazgo.
Fusión caliente
En septiembre de 1994, el equipo de Dubna detectó un solo átomo de 273 Ds bombardeando un objetivo plutonio-244 con acelerados de azufre -34 núcleos.
Los experimentos se han realizado en 2004 en el Laboratorio Flerov de Reacciones Nucleares en Dubna estudio de las características de fisión del núcleo compuesto 280 Ds, producidos a través de la reacción nuclear:
- 232
90 Th + 48
20 Ca → 280
110 Ds * → fisión
El resultado reveló núcleos cómo este compuesto tal como la fisión predominantemente expulsando magia y núcleos doblemente mágicos como 132 Sn ( Z = 50, N = 82). No se obtuvieron átomos darmstadtium. Un núcleo compuesto es una combinación flexible de nucleones que no han dispuestas a sí mismos en proyectiles nucleares todavía. No tiene ninguna estructura interna y se mantiene unida sólo por las fuerzas de colisión entre el objetivo y el proyectil núcleos. Se estima que requiere alrededor de 10 -14 s para los nucleones para organizar ellos mismos en conchas nucleares, momento en el que el núcleo compuesto se convierte en una nucleido, y este número es utilizado por IUPAC como el mínimo de vida media de un isótopo reivindicada debe tener potencialmente ser reconocido como ser descubierto. Por lo tanto, el isótopo 280 Ds permanece actualmente desconocido.
Como producto de la desintegración
| Residuo de evaporación | Isótopo darmstadtium observada |
|---|---|
| 277 Cn | 273 Ds |
| 285 Fl, 281 Cn | 277 Ds |
| 291 Lv, Fl 287, 283 Cn | 279 Ds |
| 293 Lv, Fl 289, 285 Cn | 281 Ds |
Darmstadtium se ha observado que los productos de desintegración de copernicium . Copernicio actualmente tiene seis isótopos conocidos, cuatro de los cuales se ha demostrado que someterse alfa se desintegra para convertirse en núcleos darmstadtium, con números de masa entre 273 y 281. Darmstadtium isótopos con números de masa 277, 279 y 281 hasta la fecha sólo se han producido por los núcleos Copernicium decadencia. Núcleos Copernicium padres pueden ser ellos mismos los productos de desintegración de flerovium o livermorium . Hasta la fecha, no hay otros elementos se han conocido a decaer a darmstadtium. Por ejemplo, en 2004, el equipo de Dubna ( ICIN) identificado darmstadtium-281 como un producto en el decaimiento de livermorium a través de una secuencia de desintegración alfa:
- 293
116 Lv → 289
114 Fl + 4
2 Él - 289
114 Fl → 285
112 Cn + 4
2 Él - 285
112 Cn → 281
110 Ds + 4
2 Él
Isótopos
| Isótopo | Media vida | Decaimiento modo | Descubrimiento año | Reacción |
|---|---|---|---|---|
| 267 Ds? | 2.8 mS | α | 1994 | 209 Bi (59 Co, n) |
| 268 Ds | 100? mS | α? | desconocido | - |
| 269 Ds | 179 mS | α | 1994 | 208 Pb (62 Ni, n) |
| 270 Ds | 100 mS | α, SF | 2000 | 207 Pb (64 Ni, n) |
| 270m Ds | 6.0 ms | α, Informática | 2000 | 207 Pb (64 Ni, n) |
| 271 Ds | 1,63 ms | α | 1994 | 208 Pb (64 Ni, n) |
| 271m Ds | 69 ms | α | 1994 | 208 Pb (64 Ni, n) |
| 272 Ds | 1? s | SF? | desconocido | - |
| 273 Ds | 170 mS | α | 1996 | 244 Pu (34 S, 5n) |
| 274 Ds | 2? s | α, SF? | desconocido | - |
| 275 Ds | 2? s | α? | desconocido | - |
| 276 Ds | 5? s | α? | desconocido | - |
| 277 Ds | 5.7 ms | α | 2010 | 285 Fl (-, 2α) |
| 278 Ds | 10? s | α, SF? | desconocido | - |
| 279 Ds | 0.18 s | α, SF | 2002 | 291 Lv (-, 3α) |
| 280 Ds | 11? s | SF? | desconocido | - |
| 281 Ds | 11 s | SF | 1999 | 289 Fl (-, 2α) |
| 281m Ds? | ~ 3,7 min | α | 1999 | 289 Fl (-, 2α) |
Darmstadtium no tiene isótopos estables o de origen natural. Varios isótopos radiactivos han sido sintetizados en el laboratorio, ya sea mediante la fusión de dos átomos o mediante la observación de la desintegración de elementos más pesados. Ocho isótopos diferentes de darmstadtium se han reportado con masas atómicas 267, 269-271, 273, 277, 279, y 281, aunque darmstadtium-267 es sin confirmar. Tres isótopos darmstadtium, darmstadtium-270, darmstadtium-271, y darmstadtium-281, han conocido estados metaestables (aunque la de darmstadtium-281 es sin confirmar). La mayoría de éstos se desintegran principalmente a través de la desintegración alfa, pero algunos pasan por fisión espontánea.
Estabilidad y vida media
Todos los isótopos darmstadtium son extremadamente inestables y radiactivos; En general, los isótopos más pesados son más estables que el encendedor. El isótopo darmstadtium conocido más estable, 281 Ds, es también el más pesado conocido isótopo darmstadtium; que tiene una vida media de 11 segundos, aunque un estado metaestable, 281m Ds, se ha informado que tienen una vida media de alrededor de 3,7 minutos más. El isótopo 279 Ds tiene una vida media de 0,18 segundos, respectivamente. Los seis isótopos restantes y dos estados metaestables tienen vidas medias entre 1 microsegundo y 70 milisegundos. Algunos isótopos desconocidos en esta región, tales como 272, 274 a 276 Ds Ds, y 280 Ds, se prevé que también tienen más larga vida media de unos segundos. Antes de su descubrimiento, 277 Ds se prevé que también tienen una larga vida media de unos 5 segundos; sin embargo, se ha encontrado ya que para tener una vida media muy corta de sólo 5,7 milisegundos.
El isótopo no descubierto 284 Ds se ha predicho que es la más estable hacia desintegración beta; sin embargo, no se conoce ningún isótopo darmstadtium se ha observado que someterse desintegración beta. Cálculo teórico en un modelo de túnel cuántico reproduce el decaimiento alfa experimental sobre la vida media de los isótopos darmstadtium conocidos. También predice que el isótopo 294 sin descubrir Ds, que tiene una número mágico de neutrones (184), tendría una vida media de desintegración alfa del orden de 311 años.
Isomería Nuclear
- 281 Ds
La producción de 281 Ds por el decaimiento de 289 Fl o 293 dos modos de desintegración muy diferentes Lv ha producido. El modo más común y es fácilmente confirmado fisión espontánea, con una vida media de 11 s. Un modo mucho más raro y aún sin confirmar es alfa decadencia por la emisión de una partícula alfa con energía 8.77 MeV con una vida media observada de alrededor de 3,7 min. Esta decadencia se asocia con una vía única descomposición de los nucleidos padres y debe ser asignado a un nivel de isómeros. La vida media sugiere que se debe asignar a un estado de isómeros, pero se necesita más investigación para confirmar estos informes.
- 271 Ds
Datos de la desintegración de la síntesis directa de 271 Ds indica claramente la presencia de dos isómeros nucleares. La primera emite partículas alfa con energías 10,74 y 10,69 MeV y tiene una vida media de 1,63 ms. El otro sólo emite paricles alfa con una energía de 10,71 MeV y tiene una vida media de 69 ms. La primera ha sido asignada al estado fundamental y el segundo a un nivel de isómeros. Se ha sugerido que la proximidad de las energías desintegración alfa indica que el nivel de isómeros puede decaer principalmente por retardada transición isomérica al estado fundamental, lo que resulta en una energía alfa medido idéntica y una vida media combinada para los dos procesos.
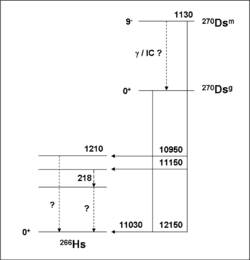
- 270 Ds
La producción directa de 270 Ds ha identificado claramente dos isómeros nucleares. El estado fundamental decae por emisión alfa en el estado fundamental de 266 Hs mediante la emisión de una partícula alfa con energía 11,03 MeV y tiene una vida media de 0,10 ms. El estado metaestable decae por emisión alfa, emisores de partículas alfa con energías de 12,15, 11,15, y 10,95 MeV y tiene una vida media de 6 ms. Cuando el estado metaestable emite una partícula alfa de la energía 12,15 MeV, que se desintegra en el estado fundamental de 266 Hs, que indica que tiene 1,12 MeV de exceso de energía.
Propiedades predichas
Químico
Darmstadtium es el octavo miembro de la serie 6d de metales de transición . Desde copernicium (elemento 112) ha demostrado ser un metal de transición, se espera que todos los elementos de 104 a 112 formarían una cuarta serie de metales de transición, con darmstadtium como parte de la metales del grupo del platino. Los cálculos sobre su potenciales de ionización y atómico y radios iónicos son similares a la de su homólogo más ligero de platino , lo que implica que las propiedades básicas de darmstadtium se asemejan a los de la otra grupo 10 elementos, níquel , paladio y platino.
Predicción de las propiedades químicas probables de darmstadtium no ha recibido mucha atención recientemente. Se espera Darmstadtium ser una noble metal. Con base en los estados de oxidación más estable de los grupo más ligero 10 elementos, los estados de oxidación más estables de darmstadtium se prevé están los 6, 4, 2 y estados; sin embargo, el estado neutro se prevé que sea el más estable en soluciones acuosas. En comparación, sólo se conoce de platino para mostrar el estado de oxidación máximo en el grupo, 6, mientras que los estados más estables son 4 y 2 tanto para el níquel y paladio. Se espera además que los estados de oxidación máximo de elementos de bohrium (elemento 107) a darmstadtium (elemento 110) pueden ser estables en la fase gaseosa, pero no en solución acuosa. Hexafluoruro Darmstadtium (DSF 6) se predice que tienen propiedades muy similares a su homólogo más ligero platino hexafluoruro (PtF 6), que tienen estructuras electrónicas muy similares y potenciales de ionización.
Física y atómica
Se espera Darmstadtium a ser un sólido en condiciones normales. Debe ser una muy pesada de metal con una densidad de alrededor de 34,8 g / cm 3. En comparación, el elemento más denso conocido que ha tenido midió su densidad, osmio , tiene una densidad de sólo 22,61 g / cm 3. Esto resulta de alto peso atómico de darmstadtium, la lantánidos y actínidos contracciones, y efectos relativistas, aunque la producción de suficiente darmstadtium para medir esta cantidad sería poco práctico, y la muestra decaería rápidamente.
El exterior configuración electrónica de darmstadtium se calcula para ser 6d 8 7s 2, que obedece a las Principio de Aufbau y no sigue configuración electrónica externa de platino de 5d 9 6s 1. Esto es debido a la estabilización relativista de la pareja 7s 2 electrones durante todo el período séptimo, por lo que ninguno de los elementos 104 a 112 tienen configuraciones electrónicas que violan el principio de Aufbau. Se espera que el radio atómico de darmstadtium estar alrededor de 118 pm.
Química Experimental
Determinación inequívoca de las características químicas de darmstadtium aún tiene que se han establecido debido a la corta vida media de los isótopos darmstadtium y un número limitado de compuestos volátiles probables que podrían estudiarse en una escala muy pequeña. Uno de los pocos compuestos darmstadtium que son propensos a ser suficientemente volátil es darmstadtium hexafluoruro (DSF 6), como su homólogo más ligero platino hexafluoruro (PTF 6) es volátil por encima de 60 ºC y por lo tanto el compuesto análogo de darmstadtium también podría ser suficientemente volátil; un octafluoride volátil (DSF 8) también podría ser posible. Para los estudios químicos que se llevarán a cabo en un transactinide, al menos cuatro átomos deben ser producidos, la vida media del isótopo utilizado debe ser de al menos 1 segundo, y la tasa de producción deben ser de al menos un átomo por semana. A pesar de que la vida media de 281 Ds, el más estable de isótopos darmstadtium confirmado, es 11 segundos, el tiempo suficiente para llevar a cabo estudios químicos, otro obstáculo es la necesidad de aumentar la tasa de producción de isótopos darmstadtium y permitir experimentos para continuar durante semanas o meses para que se pueden obtener resultados estadísticamente significativos. Separación y detección deben llevarse a cabo de manera continua para separar los isótopos darmstadtium y los sistemas automatizados pueden entonces experimentar en la fase gaseosa y la solución química de darmstadtium como los rendimientos de los elementos más pesados se predicen a ser más pequeñas que las de los elementos más ligeros; algunas de las técnicas de separación utilizadas para bohrium y hassium podrían ser reutilizados. Sin embargo, la química experimental de darmstadtium no ha recibido tanta atención como la de los elementos más pesados copernicium y flerovium .
Los más neutrones isótopos darmstadtium Ricos son los más estables y son por lo tanto más prometedor para estudios químicos; Sin embargo, sólo se pueden producir indirectamente de la desintegración alfa de elementos más pesados, y métodos de síntesis indirectos no son favorables para estudios químicos. Cuanto más ricos en neutrones isótopos 276 y 277 Ds Ds podría ser producido directamente en la reacción entre el torio y -232 Se espera que el calcio-48, pero el rendimiento a ser baja. Además, esta reacción ya ha sido probado sin éxito, y los experimentos más recientes que han sintetizado con éxito 277 Ds utilizando métodos indirectos muestran que tiene una vida media corta de 5,7 ms, no el tiempo suficiente para realizar los estudios químicos.


