
Sal (química)
Antecedentes de las escuelas de Wikipedia
SOS Children han producido una selección de artículos de la Wikipedia para escuelas desde 2005. Haga clic aquí para obtener más información sobre SOS Children.

Una sal, en la química , se define como el producto formado a partir de la reacción de neutralización de ácidos y bases. Las sales son compuestos iónicos compuestos por cationes (positivamente cargados iones) y aniones (iones negativos) para que el producto es eléctricamente neutra (sin carga neta). Estos iones componentes pueden ser inorgánico , tal como cloruro (Cl -), así como orgánicos tales como de etilo (CH 3 COO -) y iones monoatómicos tales como fluoruro (F -), así como iones poliatómicos como el sulfato (SO 4 2-).
Hay varias variedades de sales. Las sales que producen hidróxido de iones cuando se disuelve en agua son sales básicas y sales que producen iones hidronio en el agua son sales de ácidos. Las sales neutras son aquellos que no son ni ácido ni sales básicas. Zwitteriones contienen un centro aniónico y un centro catiónico en la misma molécula , pero no se consideran sales. Los ejemplos incluyen aminoácidos , muchos metabolitos, péptidos y proteínas .
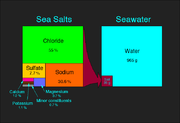
Cuando las sales se disuelven en agua, se les llama electrolitos, y son capaces de conducir la electricidad , una propiedad que se comparte con sales fundidas. Las mezclas de muchos iones diferentes en solución como en el citoplasma de las células , en sangre , orina, Jugos de plantas y mineral Waters por lo general no forman sales definidas después de la evaporación del agua. Por lo tanto, su contenido de sal se da para los iones respectivos.
Propiedades

Color
Las sales se parecen ser claras y transparente ( cloruro de sodio ), opaca, e incluso metálica y brillante ( disulfuro de hierro ). En muchos casos el aparentes opacidad o la transparencia sólo están relacionadas con la diferencia en tamaño del individuo monocristales. Dado que la luz se refleja en la límites de grano (límites entre cristalitos), grandes cristales tienden a ser transparente, mientras que agregados policristalinos ven como polvos blancos. Por supuesto, algunas sales son inherentemente opaca.
Las sales existen en todos los diferentes colores , por ejemplo, amarillo (sodio cromato), naranja ( dicromato de potasio), rojo ( sulfuro de mercurio), malva ( cloruro de cobalto hexahidratado), azul ( sulfato de cobre pentahidratado, hexacianoferrato férrico), verde ( óxido de níquel), incoloro ( sulfato de magnesio), blanco, y negro ( dióxido de manganeso). La mayoría de los minerales inorgánicos y pigmentos así como muchos orgánica sintética colorantes son sales.
Sabor
Diferentes sales pueden provocar los cinco sabores básicos, por ejemplo salada ( cloruro de sodio ), dulce ( diacetato de plomo; pero lo que provocará envenenamiento por plomo si se ingiere), agrio ( bitartrato de potasio), amargo ( sulfato de magnesio), y umami o salado ( glutamato monosódico).
Olor
Las sales de ácidos y bases fuertes (" sales fuertes ") son no- volátil e inodoro, mientras que las sales de cualquiera de los ácidos débiles o bases débiles (" sales débiles ") pueden oler después de la ácido conjugado (por ejemplo acetatos como el ácido acético ( vinagre) y cianuros como el cianuro de hidrógeno ( almendras ) o la base conjugada (por ejemplo, sales de amonio como amoniaco ) de los iones de componentes. Eso, descomposición parcial lenta por lo general se acelera por la presencia de agua, ya la hidrólisis es la otra mitad de la ecuación de la reacción reversible de formación de sales débiles.
Nomenclatura

El nombre de una sal comienza con el nombre del catión (por ejemplo, sodio o amonio), seguido por el nombre del anión (por ejemplo, cloruro o acetato). Las sales se refieren a menudo sólo por el nombre del catión (por ejemplo, sal de sodio o sal de amonio) o por el nombre del anión (por ejemplo, cloruro o acetato).
Cationes formadores de sales comunes incluyen:
- amonio NH 4 +
- calcio Ca 2+
- hierro Fe 2+ y Fe 3+
- magnesio Mg 2+
- de potasio K +
- piridinio C 5 H 5 + NH
- NR amonio cuaternario 4 +
- de sodio Na +
Aniones formadores de sal común (y el nombre de los ácidos precursores entre paréntesis) son:
- acetato de CH 3 COO - ( ácido acético )
- carbonato de CO 3 2- ( ácido carbónico)
- cloruro Cl - ( ácido clorhídrico )
- HOC citrato (COO -) (CH2 COO -) 2 ( ácido cítrico)
- C≡N cianuro - ( cianuro de hidrógeno )
- hidróxido OH - ( agua )
- nitrato NO 3 - ( ácido nítrico )
- NO nitrito 2 - ( ácido nitroso)
- óxido O 2- ( agua )
- fosfato PO 4 3- ( ácido fosfórico )
- sulfato SO 4 2- ( ácido sulfúrico )
Formación
Las sales se forman por una reacción química entre:
- Las sales también se pueden formar si se mezclan soluciones de sales diferentes, sus iones se recombinan, y la nueva sal es insoluble y precipita (ver: equilibrio de solubilidad), por ejemplo:
Pb (NO 3) 2 (aq) + Na 2 SO 4 (aq) → PbSO 4 (s) + NaNO3 (aq)


