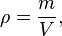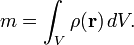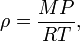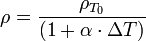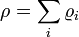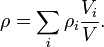Densité
Saviez-vous ...
Cette sélection se fait pour les écoles par la charité pour enfants lire la suite . Cliquez ici pour plus d'informations sur les enfants SOS.
La densité de masse ou de densité d'un matériau est sa masse par unité de volume . Le symbole le plus souvent utilisé pour la densité est ρ (la lettre grecque minuscule rho). Mathématiquement, la densité est définie comme la masse divisée par le volume:
où ρ est la masse volumique, m est la masse, et V est le volume. Dans certains cas (par exemple, aux États-Unis de l'industrie du pétrole et du gaz), la densité est également définie comme sa poids par unité de volume , bien que cette quantité est plus correctement appelé poids spécifique.
Différents matériaux ont généralement des densités différentes, et la densité peuvent être pertinents pour flottabilité, la pureté et emballage. osmium et l'iridium sont les éléments les plus denses connus à conditions normales de température et de pression, mais certains composés chimiques peuvent être plus dense.
Fluides moins denses flottent sur les fluides plus denses se ils ne se mélangent pas. Ce concept peut être étendu, avec une certaine prudence, à des solides moins denses flottant sur les liquides plus denses. Si la densité moyenne (y compris l'air au-dessous de la ligne de flottaison) d'un objet est inférieure à l'eau elle flotte dans l'eau et si elle est supérieure à l'eau, il se enfoncer dans l'eau.
La densité est parfois exprimée par le grandeur sans dimension " gravité spécifique "ou" densité relative ", ce est à dire le rapport de la densité de la matière à celle d'un matériau standard, généralement de l'eau. Ainsi, une gravité spécifique inférieure à un signifie que la substance flotte dans l'eau.
La densité d'un matériau varie avec la température et la pression. Cette variation est généralement faible pour les solides et liquides, mais beaucoup plus pour les gaz. L'augmentation de la pression sur un objet diminue le volume de l'objet et augmente ainsi sa densité. L'augmentation de la température d'une substance (avec quelques exceptions) diminue sa densité en augmentant son volume. Dans la plupart des matériaux, le chauffage de la partie inférieure d'un fluide dans résultats convection de la chaleur du bas vers le haut, en raison de la diminution de la densité du fluide chauffé. Cela provoque de se élever par rapport à la matière non chauffé plus dense.
L'inverse de la densité d'une substance est parfois appelé son volume spécifique, un terme parfois utilisé dans la thermodynamique . La densité est un propriété intensive en ce que l'augmentation de la quantité d'une substance ne augmente pas sa densité; plutôt elle augmente sa masse.
Histoire
Dans un conte bien connu mais probablement apocryphe, Archimède a été donné la tâche de déterminer si Roi Hiéron de orfèvre détournait l'or au cours de la fabrication d'un or couronne dédiée aux dieux et son remplacement par une autre, moins cher alliage. Archimède savait que la couronne de forme irrégulière pourrait être écrasé dans un cube dont le volume pourrait être calculé facilement et par rapport à la masse; mais le roi n'a pas approuvé de cette. Perplexe, Archimède est dit avoir pris un bain d'immersion et observé à partir de la montée de l'eau à l'entrée qu'il ne pouvait calculer le volume de la couronne d'or à travers le déplacement de l'eau. Après cette découverte, il sauta de son bain et a couru nu à travers les cris des rues, "Eureka! Eureka!" (Εύρηκα! Grec "je l'ai trouvé"). En conséquence, le terme " eureka "est entré dans le langage courant et est utilisé aujourd'hui pour indiquer un moment d'illumination.
L'histoire est apparue sous forme écrite dans Vitruve ' livres d'architecture, deux siècles après censément eu lieu. Certains chercheurs ont mis en doute l'exactitude de ce récit, en disant entre autres que la méthode aurait nécessité des mesures précises qui auraient été difficile de faire à l'époque.
De l'équation pour la densité (ρ = m / V), la densité de masse a des unités de masse divisée par le volume. Comme il ya de nombreuses unités de masse et de volume couvrant de nombreux grandeurs différentes il ya un grand nombre d'unités de densité de masse en cours d'utilisation. Le Unité SI de kilogrammes par mètre cube (kg / m 3) et le unité CGS de gramme par centimètre cube (g / cm 3) sont probablement les unités les plus couramment utilisés pour la densité. (Le centimètre cube peut être appelé alternativement un millilitre ou un cc.) 1000 kg / m 3 une g / cm 3 est égal. Dans l'industrie, d'autres unités plus ou moins de la masse et le volume sont souvent plus pratique et Unités de mesure américaines peuvent être utilisés. Voir ci-dessous une liste de certaines des unités les plus courants de densité.
Mesure de la densité
La densité à tous les points d'une objet homogène est égale à sa masse totale divisée par son volume total. La masse est normalement mesurée avec un échelle ou de l'équilibre; le volume peut être mesuré directement (à partir de la géométrie de l'objet) ou par le déplacement d'un fluide. Pour déterminer la densité d'un liquide ou d'un gaz, un densimètre ou dasymeter peut être utilisée, respectivement. De même, pesée hydrostatique utilise le déplacement de l'eau due à un objet immergé pour déterminer la densité de l'objet.
Si le corps ne est pas homogène, sa densité varie entre les différentes régions de l'objet. Dans ce cas, la densité autour de ne importe quel emplacement donné est déterminée par le calcul de la densité d'un petit volume autour de cet emplacement. Dans la limite d'un volume infinitésimal la densité d'un objet hétérogène à un point devient: ρ (r) = dm / DV, où dV est un volume élémentaire à la position r. La masse du corps peut alors être exprimé sous la forme
La densité du matériau granulaire peut être ambiguë, selon exactement comment son volume est définie, ce qui peut causer de la confusion dans la mesure. Un exemple courant est le sable: si elle est doucement versé dans un récipient, la densité sera faible; si le même sable est ensuite compacté, il occupera moins de volume et par conséquent présentent une plus grande densité. Ce est parce que le sable, comme toutes les poudres et solides granulaires, contient beaucoup de l'espace aérien entre les grains individuels. La densité de la matière, y compris les espaces d'air est le densité apparente, qui diffère sensiblement de la densité d'un grain individuel de sable sans air inclus.
Les changements de densité
En général, la densité peut être modifiée en changeant, soit la la pression ou la température . L'augmentation de la pression augmente toujours la densité d'un matériau. Augmentation de la température diminue généralement la densité, mais il ya des exceptions notables à cette généralisation. Par exemple, la densité de l'eau augmente entre son point de fusion à 0 ° C et 4 ° C; comportement similaire est observé en silicium à basse température.
L'effet de la pression et de la température sur la densité des liquides et des solides est faible. Le compressibilité pour un liquide ou un solide typique est de 10 -6 -1 bar (1 bar = 0,1 MPa) et un typique dilatation thermique est de 10 -5 K -1. Cela se traduit grosso modo en avoir besoin autour de dix mille fois la pression atmosphérique afin de réduire le volume d'une substance par un pour cent. (Bien que les pressions nécessaires peuvent être environ un millier de fois plus petit pour le sol de sable et certaines argiles.) Une expansion d'un pour cent du volume nécessite généralement une augmentation de température de l'ordre de milliers de degrés Celsius .
En revanche, la densité du gaz est fortement affectée par la pression. La densité d'un gaz parfait est
où M est la masse molaire , P est la pression, R est le constante universelle des gaz et T est la température absolue . Cela signifie que la densité d'un gaz parfait peut être doublée en doublant la pression, ou par réduction de moitié de la température absolue.
Dans le cas de dilatation thermique volumique à pression constante et de petits intervalles de température la dépendance en température de la masse volumique est la suivante:
où 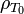 est la densité à une température de référence,
est la densité à une température de référence,  est le coefficient de dilatation thermique du matériau à des températures proches
est le coefficient de dilatation thermique du matériau à des températures proches 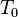 .
.
Densité de solutions
La densité d'une solution est la somme de masse (massique) concentrations des composants de cette solution.
Masse (massique) concentration de chaque composant ρ i donné dans une solution à des sommes densité de la solution.
Exprimé en fonction des densités des composants purs du mélange et leur la participation de volume, on peut lire:
à condition qu'il n'y ait pas d'interaction entre les composants.
Densités
Eau
Densité de l'eau à 1 la pression atm:
| Temp (° C) | Densité (kg / m 3) |
|---|---|
| 100 | 958,4 |
| 80 | 971,8 |
| 60 | 983,2 |
| 40 | 992,2 |
| 30 | 995.6502 |
| 25 | 997.0479 |
| 22 | 997.7735 |
| 20 | 998.2071 |
| 15 | 999.1026 |
| 10 | 999.7026 |
| 4 | 999.9720 |
| 0 | 999.8395 |
| -10 | 998,117 |
| -20 | 993,547 |
| -30 | 983,854 |
| Les valeurs inférieures à 0 ° C se réfèrent à eau en surfusion. | |
Air
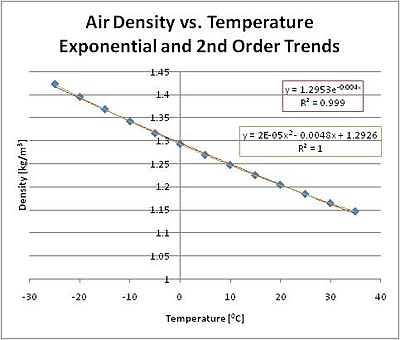
Densité de l'air à pression de 1 atm:
| T (° C) | ρ (kg / m 3) |
|---|---|
| -25 | 1,423 |
| -20 | 1,395 |
| -15 | 1,368 |
| -10 | 1,342 |
| -5 | 1,316 |
| 0 | 1,293 |
| 5 | 1,269 |
| 10 | 1,247 |
| 15 | 1,225 |
| 20 | 1,204 |
| 25 | 1,184 |
| 30 | 1,164 |
| 35 | 1,146 |
Divers matériaux
Sauf indication contraire, toutes les densités sont donnés au conditions normales de température et de pression, ce est-à 273,15 K (0,00 ° C) et 100 kPa (0,987 atm).
| Matériel | ρ (kg / m 3) | Remarques |
|---|---|---|
| Air | 1.2 | Au niveau de la mer |
| Aérographite | 0,2 | * |
| Microlattice Metallic | 0,9 | * |
| Aérogel | 1.0 | * |
| Styrofoam | 75 | Env. |
| un atome d'hydrogène liquide | 70 | A ~ -255 ° C |
| Liège | 240 | Env. |
| Lithium | 535 | |
| Bois | 700 | Assaisonné, typique |
| Potassium | 860 | |
| Sodium | 970 | |
| Glace | 916,7 | A température <0 ° C |
| Eau (fraîche) | 1000 | |
| De l'eau (sel) | 1030 | |
| Plastiques | 1175 | Environ .; pour polypropylène et PETE / PVC |
| Tétrachloroéthène | 1622 | |
| Magnésium | 1740 | |
| Béryllium | 1850 | |
| Glycérol | 1261 | |
| Silicium | 2330 | |
| Aluminium | 2700 | |
| Diiodométhane | 3325 | liquide à température ambiante |
| Diamant | 3500 | |
| Titane | 4540 | |
| Sélénium | 4800 | |
| Vanadium | 6100 | |
| Antimoine | 6690 | |
| Zinc | 7000 | |
| Chrome | 7200 | |
| Manganèse | 7325 | Env. |
| Étain | 7310 | |
| Fer | 7870 | |
| Niobium | 8570 | |
| Cadmium | 8650 | |
| Cobalt | 8900 | |
| Nickel | 8900 | |
| Cuivre | 8940 | |
| Bismuth | 9750 | |
| Molybdène | 10220 | |
| Argent | 10500 | |
| Plomb | 11340 | |
| Thorium | 11700 | |
| Rhodium | 12410 | |
| Mercure | 13546 | |
| Tantale | 16600 | |
| Uranium | 18800 | |
| Tungstène | 19300 | |
| Or | 19320 | |
| Plutonium | 19840 | |
| Platine | 21450 | |
| Iridium | 22420 | |
| Osmium | 22570 |
* Air exclu lors du calcul de la densité
Autres
| Entité | ρ (kg / m 3) | Remarques |
|---|---|---|
| Milieu interstellaire | 1 × 10 -19 | En supposant que 90% de H, 10% He; variable T |
| La Terre | 5515 | Densité moyenne. |
| Le Noyau interne de la Terre | 13000 | Env., Selon la liste figurant dans la Terre . |
| Le noyau du Soleil | 33,000-160,000 | Env. |
| Un trou noir supermassif | 9 × 10 5 | Densité d'un trou noir de 4,5 millions de masses solaires rayon d'horizon de l'événement est 13.500.000 kilomètres. |
| Naine blanche étoiles | 2,1 × 10 9 | Env. |
| Les noyaux atomiques | 2,3 × 10 17 | Ne dépend pas fortement de la taille de noyau |
| Étoile à neutrons | 1 × 10 18 | |
| Stellar-messe Trou noir | 1 × 10 18 | Densité d'un trou noir quatre-masse solaire rayon d'horizon de l'événement est à 12 km. |
Autres unités communes
Le Unité SI de la densité est:
- kg par mètre cube (kg / m 3)
Litres tonnes et ne font pas partie de l'IS, mais sont acceptables pour une utilisation avec elle, conduisant à des unités suivantes:
- kg par litre (kg / L)
- grammes par millilitre (g / ml)
- tonnes par mètre cube (t / m 3)
Densités en utilisant les unités métriques suivantes ont toutes exactement la même valeur numérique, un millième de la valeur (kg / m 3). Liquid eau a une densité d'environ 1 kg / dm 3, rendant l'une de ces unités SI numérique facile à utiliser que la plupart des solides et des liquides ont des densités entre 0,1 et 20 kg / dm 3.
- kilogrammes par décimètre cube (kg / dm 3)
- gramme par centimètre cube (g / cc, g / cc ou g / cm 3)
- 1 g / cm 3 = 1000 kg / m 3
- mégagrammes (tonnes métriques) par mètre cube (mg / m 3)
En Unité de mesure US densité peut être indiqué dans:
- once avoirdupoids par cubic inch (oz / cu in)
- livres avoirdupoids par pouce cube (lb / po cu)
- livres par pied cube (lb pi / cu)
- livres par verge cube (lb / cu m)
- livres par Gallon liquide américain (lb / gal)
- livres par US boisseau (lb / boisseau)
- limaces par pied cube
Unités impériales différentes de ce qui précède (le gallon impérial et le boisseau diffèrent des unités américaines) dans la pratique sont rarement utilisés, bien trouvé dans les documents anciens. La densité de métaux précieux pourraient éventuellement être fondées sur Onces troy et livres, une cause possible de confusion.