
Calcita
Fundo para as escolas Wikipédia
Esta seleção Wikipedia está offline disponível a partir de Crianças SOS, para distribuição no mundo em desenvolvimento. Patrocínio da criança ajuda as crianças uma a uma http://www.sponsor-a-child.org.uk/ .
| Calcita | |
|---|---|
 A calcita de uma polegada losango que mostra a propriedade dupla refração imagem | |
| Geral | |
| Categoria | Mineral de carbonato |
| Fórmula (Unidade de repetição) | CaCO3 |
| Classificação Strunz | 05.AB.05 |
| Cristal simetria | Trigonal 3 2 / m |
| Unidade celular | a = 4,9896 (2) A, C = 17,0610 (11) A; Z = 6 |
| Identificação | |
| Cor | Incolor ou branco, também cinza, amarelo, verde, |
| Hábito de Cristal | Cristalino, granular, stalactitic, concretionary, maciço, rhombohedral. |
| Sistema cristalino | Escalenoédrica hexagonal trigonal (3 2 / m), Grupo de espaço (2 3 R / c) |
| Geminação | Comum por quatro leis gêmeas |
| Clivagem | Perfeito em [10 1 1] três direções com ângulo de 74 ° 55 ' |
| Fratura | Conchoidal |
| Tenacidade | Quebradiço |
| Escala de Mohs dureza | 3 (mineral definindo) |
| Brilho | Vítreo a nacarado em superfícies de clivagem |
| Risca | Branco |
| Diaphaneity | Transparente a translúcido |
| Peso específico | 2.71 |
| Propriedades ópticas | Uniaxial (-) |
| Índice de refração | n ω = 1,640-1,660 n ε = 1,486 |
| Birefringence | δ = 0,154-0,174 |
| Solubilidade | Solúvel em ácidos diluídos |
| Outras características | Pode fluorescer cores vermelhas, azuis, amarelos, e outros sob qualquer SW e LW UV; fosforescente |
| Referências | |
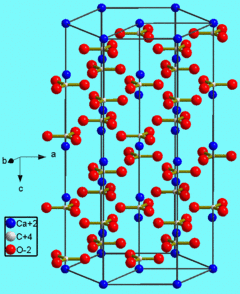
A calcite é uma mineral de carbonato e o mais estável polimorfo de carbonato de cálcio ( Ca C O 3). Os outros polimorfos são os minerais aragonita e vaterite. Aragonite mudará para calcite de 380-470 ° C, e vaterite é ainda menos estáveis.
Propriedades
Calcite cristais são trigonal-romboédrica, embora calcite real rhombohedra são raros como cristais naturais. No entanto, eles mostram uma variedade notável de hábitos aguda incluindo a rhombohedra obtuso, formas tabulares, prismas, ou várias scalenohedra. Exposições de calcita vários geminação tipos adicionando à variedade de formas observadas. Pode ocorrer como fibrosa e granular, lamelar, ou compacto. A clivagem é geralmente em três direcções paralelas à forma rhombohedron. Sua fratura é conchoidal, mas difícil de obter.
Ele tem uma definição de dureza de Mohs de 3, uma peso específico de 2,71, e o seu brilho é vítreo em variedades cristalizados. A cor é branca ou nenhum, embora tons de cinza, vermelho, laranja, amarelo, verde, azul, violeta, marrom, preto ou até mesmo pode ocorrer quando o mineral é acusado de impurezas.
Calcita é transparente para opaco e pode ocasionalmente mostrar fosforescência ou fluorescência. Uma variedade transparente chamada Islândia Spar é usado para fins ópticos. Cristais escalenoédrica agudas são muitas vezes referidos como "spar dogtooth" enquanto a forma romboédrica é por vezes referido como "spar nailhead".
Cristais de calcita individuais exibir uma propriedade óptica chamada birrefringência (dupla refração). Esta forte birrefringência faz com que os objetos vistos através de um pedaço de calcita clara apareça em dobro. O efeito birefringent (usando calcite) foi descrita pela primeira vez pelo dinamarquês cientista Rasmus Bartholin em 1669. Em um comprimento de onda de 590 nm ~ calcite tem ordinária e extraordinária índices de refração de 1,658 e 1,486, respectivamente. Entre 190 e 1700 nm, o índice de refracção varia mais ou menos comum entre 1,9 e 1,5, enquanto que o índice de refracção extraordinária varia entre 1,6 e 1,4.
Calcita, como a maioria dos carbonatos, dissolverá com a maioria das formas de ácido. A calcite pode ser tanto dissolvidos por águas subterrâneas ou precipitado por águas subterrâneas, dependendo de vários factores, incluindo a temperatura da água, pH , e dissolveu-se iões de concentrações. Apesar de calcite é bastante insolúvel em água fria, a acidez pode causar a dissolução de calcite e liberação de dióxido de carbono. O dióxido de carbono ambiente, devido à sua acidez, tem um ligeiro efeito solubilizante sobre a calcite. Calcite exibe uma característica invulgar chamada solubilidade retrógrada em que se torna menos solúvel em água quando a temperatura aumenta. Quando as condições são adequadas para a precipitação, formulários de calcita revestimentos minerais que cimentam os grãos de rocha existentes em conjunto ou pode preencher fraturas. Quando as condições são adequadas para a dissolução, a remoção de calcite pode aumentar drasticamente a e porosidade a permeabilidade da rocha, e se continua por um longo período de tempo pode provocar a formação de cavernas . Em uma escala de paisagem, continuou dissolução do cálcio rico em rochas carbonáticas pode levar à expansão e eventual colapso de sistemas de cavernas, resultando em várias formas de carste topografia.
Uso e aplicações
Alto grau de calcite óptica foi usado na Segunda Guerra Mundial para a mira da arma, especificamente na mira de bomba e armamento anti-aéreo. Além disso, as experiências foram realizadas para utilizar calcite para uma manto de invisibilidade. Microbiologicamente calcite precipitada tem uma ampla gama de aplicações, tais como remidiation solo, estabilização de solos e reparação de betão.
Ocorrência natural
Os cristais únicos maior documentados de calcite originado Islândia, medida 7 × 7 × 2 m e 6 × 6 × 3 m e pesava cerca de 250 toneladas.

Calcita é um componente comum de rochas sedimentares , calcário, em particular, grande parte da qual é formada a partir de conchas de organismos marinhos mortos. Aproximadamente 10% das rochas sedimentares é o calcário.
Calcita é o principal mineral em metamórfica mármore. Também ocorre como um veia minerais nos depósitos de nascentes de água quente, e ela ocorre em cavernas como estalactites e estalagmites.
Lublinite é uma forma fibrosa, efflorescent de calcita.
A calcite pode também ser encontrado em vulcânica ou rochas derivados do manto, tal como carbonatites, kimberlitos, ou raramente em peridotites.
A calcite é muitas vezes o principal constituinte do conchas de organismos marinhos, por exemplo, plâncton (tal como cocólitos e planctônicos foraminíferos), as partes duras de vermelho algas , alguns esponjas, braquiópodes, equinodermes, alguns serpulids, mais Bryozoa, e partes de conchas de alguns bivalves (tal como ostras e rudists). Calcita é encontrado em forma espectacular na Snowy River Cave of Novo México, como mencionado acima, na qual os microrganismos são creditados com formações naturais. Trilobites, que são agora extinto, tinha olhos compostos exclusivos. Eles usaram cristais de calcita claras para formar as lentes dos seus olhos.
Processos de formação de calcita
Formas de calcita de um precursor mal ordenada (carbonato de cálcio amorfo, ACC). O processo de cristalização ocorre em duas etapas; Em primeiro lugar, as nanopartículas ACC desidratar rapidamente e cristalizar para formar as partículas individuais de vaterite; Em segundo lugar, o vaterite transforma a calcite através de uma dissolução e reprecipitação mecanismo com a taxa de reacção controlada pela área da superfície de calcite. A segunda fase da reacção é cerca de 10 vezes mais lento do que os primeiros. No entanto, a cristalização de calcite foi observado para ser dependente do pH de partida e a presença de Mg na solução. Um pH de partida neutro durante a mistura promove a transformação directa de ACC em calcite. Por outro lado, quando se forma uma solução de ACC em que se inicia com um pH inicial de base, a transformação ocorre através de calcita vaterite metastável, que se forma por meio de um mecanismo de crescimento esferulítico. Numa segunda fase, este transforma-se em calcite vaterite através de uma dissolução e recristalização mecanismo controlado-superfície. Mg tem um efeito notável sobre a estabilidade tanto da ACC e a sua transformação para cristalino CaCO3, resultando na formação de calcita directamente a partir de ACC, tal como este ião desestabiliza a estrutura de vaterite.
Calcita na história da Terra
Mares calcite existiu na história da terra quando o precipitado inorgânico primário de carbonato de cálcio em águas marinhas foi calcite baixo-magnésio (LMC), em oposição à aragonita e calcita de alto magnésio (HMC) precipitou hoje. Mares de calcita alternado com mares de aragonita sobre o Phanerozoic, sendo mais proeminente no Ordoviciano e Jurassic . Linhagens evoluíram para utilizar a metamorfose de carbonato de cálcio foi favorável no oceano no momento em que se tornou mineralizada, e manteve essa mineralogia para o restante de sua história evolutiva. Provas Petrográfica para estas condições de mar calcite consiste em calcítico ooids, cimentos lmc, hardgrounds e rápida do fundo do mar no início aragonite dissolução. A evolução de organismos marinhos com conchas de carbonato de cálcio podem ter sido afetados pela calcita e ciclo mar aragonite.

