
Reparo do DNA
Você sabia ...
Crianças SOS, que corre cerca de 200 sos escolas no mundo em desenvolvimento, organizado esta selecção. Patrocinar uma criança para fazer uma diferença real.
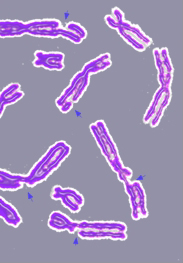
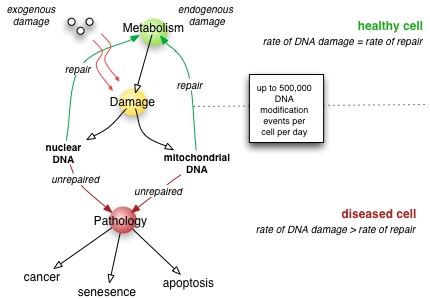
De reparação do ADN é uma colecção de processos pelos quais um células identifica e corrige danos para os ADN que codificam moléculas sua genoma. Em células humanas, normais atividades metabólicas e fatores ambientais, tais como UV e luz radiação pode causar danos no DNA, resultando em até 1 milhões indivíduo lesões moleculares por célula por dia. Muitas destas lesões causar danos estruturais para a molécula de DNA e pode alterar ou eliminar a capacidade da célula para transcrever o do gene que codifica a ADN afectada. Outras lesões induzir potencialmente prejudiciais mutações no genoma da célula, que afectam a sobrevivência das suas células filhas após ele sofre mitose. Como conseqüência, o processo de reparo de DNA é constantemente ativo, uma vez que responde a danos na estrutura do DNA. Quando os processos de reparação normais falhar, e quando celular apoptose não ocorre, danos irreparáveis DNA pode ocorrer, incluindo quebras de cadeia dupla e ligações cruzadas de DNA (ligações cruzadas intercadeias ou CIET).
A taxa de reparação do ADN está dependente de muitos factores, incluindo o tipo de célula, da idade da célula, e para o ambiente extracelular. Uma célula que tem acumulado uma grande quantidade de danos no DNA, ou um que reparações que já não efetivamente danos sofridos ao seu DNA, pode entrar em um dos três estados possíveis:
- um estado irreversível de dormência, conhecido como senescência
- suicídio celular, também conhecido como apoptose ou morte celular programada
- divisão celular desregulado, o que pode levar à formação de um tumor que é canceroso
A capacidade de reparação do ADN de uma célula é vital para a integridade do seu genoma e, portanto, para o seu funcionamento normal e que do organismo. Muitos genes que inicialmente foram mostrados para influenciar tempo de vida têm acabou por ser envolvido no DNA reparar danos e proteção. A falha para corrigir as lesões moleculares em células que formam gâmetas podem introduzir mutações no genoma da prole e, assim, influenciar a taxa de evolução .
Danos no DNA
Danos de ADN, devido a factores ambientais e normal processos metabólicos no interior da célula, ocorre a uma taxa de 1.000 a 1.000.000 de lesões moleculares por célula por dia. Enquanto isto constitui apenas 0.000165% dos cerca de 6 bilhões de bases do genoma humano (3 bilhões de pares de bases), lesões não reparados em genes críticos (como supressor de tumor genes) pode impedir a capacidade de uma célula para realizar a sua função e sensivelmente aumentar a probabilidade de a formação de tumores.
A grande maioria dos danos no ADN afecta a estrutura primária da dupla hélice; isto é, as próprias bases são modificados quimicamente. Essas modificações podem, por sua vez perturbar estrutura helicoidal normal das moléculas através da introdução de ligações químicas não-nativos ou adutos volumosos que não cabem na dupla hélice padrão. Ao contrário de proteínas e ARN, ADN normalmente carece estrutura terciária e, portanto, danos ou perturbação não ocorre a esse nível. ADN é, no entanto, proteínas "embalagem" super-enrolados e enroladas em torno chamados histonas (em eucariotas), e ambas as superstruturas são vulneráveis aos efeitos dos danos no ADN.
Tipos de danos
Existem cinco tipos principais de danos ao ADN, devido a processos celulares endógenos:
- oxidação de bases [por exemplo, 8-oxo-7,8-di-dihydroguanine (8-oxoG)] e geração de ADN de cadeia interrupções de espécies reactivas de oxigénio,
- alquilação de bases (geralmente metilação), tais como a formação de 7-metilguanina, 1-metiladenina, 6-O-metilguanina
- hidrólise de bases, tais como deamination, despurinação, e depyrimidination.
- "Formação de adutos volumosos" (ou seja, benzo [a] pireno diol epóxido-dG aducto, aristolactam aducto I-DA)
- descasamento de bases, devido a erros na Replicação do DNA, em que a base de DNA errado é costurada no lugar em uma cadeia de DNA em formação, ou uma base de DNA é pulado ou equivocadamente inserido.
Danos causados por agentes exógenos vem em muitas formas. Alguns exemplos são os seguintes:
- Luz UV-B provoca reticulação entre citosina adjacente e bases de timina criação dímeros de pirimidina. Isto é chamado danos no DNA direto.
- Luz UV-A cria radicais livres em sua maioria. Os danos causados por radicais livres é chamada danos no ADN indirecta.
- A radiação ionizante, como a criada pelo decaimento radioativo ou em raios cósmicos provoca rupturas no DNA vertentes. Radiação ionizante de baixo nível pode induzir dano ao DNA irreparável (levando a erros de transcrição e replicational necessários para neoplasia ou pode desencadear interações virais), levando a pré-maturidade envelhecimento e câncer.
- Perturbação térmica, a temperatura elevada aumenta a taxa de despurinação (perda de bases de purina a partir da espinha dorsal do ADN) e quebras de cadeia simples. Por exemplo, depurinação hidrolítica é visto na bactérias termófilas, que crescem em Hot Springs em 40-80 ° C. A taxa de depurinação (300 resíduos de purina por genoma por geração) é muito alto nessas espécies de ser reparado por máquinas reparação normal, portanto, a possibilidade de um resposta adaptativa não pode ser descartada.
- Produtos químicos industriais, tais como cloreto de vinilo e de peróxido de hidrogénio , e produtos químicos ambientais, tais como hidrocarbonetos aromáticos policíclicos encontrados na fumaça, fuligem e alcatrão criar uma enorme diversidade de DNA adducts- ethenobases, bases oxidadas, fosfotriésteres alquilados e A reticulação do ADN apenas para citar alguns.
Danos UV, alquilação / metilação, danos de raios-X e os danos oxidativos são exemplos de dano induzido. Danos espontânea pode incluir a perda de uma base, desaminação, pregueamento do anel de açúcar e deslocamento tautomérica.
Nuclear contra danos no ADN mitocondrial
Em células humanas, e eucarióticas células em geral, o ADN é encontrado em dois locais celulares - no interior da núcleo e no interior das mitocôndrias . ADN nuclear (DNAn) existe como cromatina durante as fases não-replicativos do ciclo celular e é condensado em estruturas agregadas conhecidos como cromossomas durante divisão celular. Em qualquer estado o DNA é altamente compactada e acabou em torno das proteínas do grânulo-como chamadas histonas. Sempre que uma célula precisa para expressar a informação genética codificada no seu DNAn a região cromossómica requerida é desvendado, os genes aí localizadas estão expressos, e, em seguida, a região é condensado de volta à sua conformação de repouso. DNA mitocondrial (mtDNA) está localizado dentro de mitocôndrias organelas, existe em múltiplas cópias, e é também fortemente associado com um número de proteínas para formar um complexo conhecido como o nucleóide. Dentro mitocôndrias, espécies reativas de oxigênio (ROS), ou os radicais livres, produtos secundários da produção constante de adenosina trifosfato (ATP) através fosforilação oxidativa, criar um ambiente altamente oxidativo, que é conhecida por danificar mtDNA. Uma enzima crítica para neutralizar a toxicidade destas espécies é superóxido dismutase, que está presente em ambos os mitocôndrias e citoplasma de células eucarióticas.
Senescência e apoptose
A senescência, um estado irreversível em que a célula deixa divide, é uma resposta protectora para o encurtamento do cromossoma termina. Os telômeros são longas de regiões repetitivas DNA não-codificante que cap cromossomos e sofrem degradação parcial cada vez que uma célula sofre divisão (ver Limite de Hayflick). Em contraste, quietude é um estado reversível de dormência celular que não está relacionado ao genoma danos (ver ciclo celular). A senescência em células podem servir como uma alternativa funcional à apoptose nos casos em que a presença física de uma célula por razões espaciais é exigido pelo organismo, o qual serve como um mecanismo de "último recurso" para evitar uma célula com DNA danificado de se replicar de forma inadequada na ausência de crescimento pró- sinalização celular. Divisão celular desregulada pode levar à formação de um tumor (ver o cancro ), que é potencialmente letal a um organismo. Por conseguinte, a indução de apoptose e senescência é considerado como parte de uma estratégia de protecção contra o cancro.
Danos no DNA e mutação
É importante distinguir entre a danos no ADN e mutação, os dois principais tipos de erros no DNA. Danos de DNA e mutação são fundamentalmente diferentes. Danos são anormalidades físicas no DNA, tais como quebras simples e de cadeia dupla, Resíduos de 8-hidroxideoxiguanosina, e de hidrocarbonetos aromáticos policíclicos aductos. Danos do ADN podem ser reconhecidos por enzimas, e, assim, eles podem ser reparados correctamente se a informação redundante, tal como a sequência intacta na cadeia de ADN complementar ou homóloga num cromossoma, está disponível para cópia. Se uma célula mantém danos no ADN, a transcrição de um gene pode ser evitada, e, assim, a tradução numa proteína também será bloqueado. A replicação pode também ser bloqueados e / ou a célula pode morrer.
Em contraste com danos no DNA, uma mutação é uma alteração na sequência de base do ADN. Uma mutação não pode ser reconhecida por enzimas uma vez que a mudança de base está presente em ambas as cadeias de ADN, e, assim, uma mutação não pode ser reparada. Ao nível celular, mutações podem causar alterações na função da proteína e regulação. As mutações são replicados quando a célula se replica. Em uma população de células, as células mutantes irá aumentar ou diminuir a frequência de acordo com os efeitos da mutação sobre a capacidade da célula para sobreviver e reproduzir-se. Embora muito diferentes uns dos outros, danos de DNA e as mutações estão relacionados porque muitas vezes causar danos de ADN erros de síntese de ADN durante a replicação ou reparação; esses erros são uma importante fonte de mutação.
Tendo em conta estas propriedades de danos no DNA e mutação, pode ser visto que os danos de DNA são um problema em especial não se dividem ou células, em que os danos não reparados tenderá a acumular-se ao longo do tempo lentamente dividindo. Por outro lado, em células que se dividem rapidamente, danos não reparados de ADN que não matam as células através do bloqueio da replicação tenderá a causar erros de replicação e, portanto, a mutação. A grande maioria das mutações que não estão no seu efeito neutro são prejudiciais à sobrevivência da célula. Assim, numa população de células compreendendo um tecido com a replicação das células, as células mutantes tende a ser perdida. No entanto, as mutações raras que proporcionam uma vantagem de sobrevivência tende a expandir clonalmente em detrimento das células no tecido vizinho. Esta vantagem para a célula é uma desvantagem para todo o organismo, uma vez que tais células mutantes podem dar origem a cancro. Assim, os danos no DNA em células em divisão frequentemente, porque eles dão origem a mutações, são uma causa importante de câncer. Em contraste, os danos no DNA em células raramente são susceptíveis dividindo uma causa importante de envelhecimento.
Mecanismos de reparo do DNA
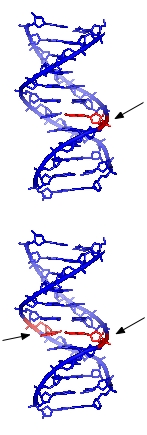
Células não pode funcionar se o dano ao DNA corrompe a integridade e acessibilidade da informação essencial na genoma (mas células permanecem superficialmente funcional quando os chamados genes "não essenciais" estão em falta ou danificado). Dependendo do tipo de danos infligidos na estrutura de dupla hélice do ADN, uma variedade de estratégias de reparo ter evoluído para restaurar a informação perdida. Se possível, as células usam a cadeia complementar não modificada do ADN ou a irmã chromatid como um modelo para recuperar a informação original. Sem acesso a um modelo, as células usam um mecanismo passível de erro de recuperação conhecido como síntese translesão como um último recurso.
Danos ao DNA altera a configuração espacial da hélice, e tais alterações podem ser detectadas pela célula. Uma vez que o dano é localizada, moléculas específicas de reparação do ADN se ligam a ou perto do local do dano, induzindo a outras moléculas para se ligar e formar um complexo, que permite a reparação real ocorra.
Reversão direta
As células são conhecidos para eliminar três tipos de danos para o seu ADN quimicamente por invertendo-o. Estes mecanismos não necessitam de um molde, uma vez que os tipos de danos que neutralizam pode ocorrer em apenas uma das quatro bases. Tais mecanismos de reversão diretos são específicos para o tipo de dano sofrido e não envolvem quebra da espinha dorsal fosfodiéster. A formação de dímeros de pirimidina sob irradiação com luz UV resultados em uma ligação covalente anormal entre bases de pirimidina adjacentes. O fotorreativação processo inverte este dano directamente pela acção da enzima fotoliase, cuja ativação é obrigatoriamente dependente da energia absorvida luz azul / UV (300-500 nm comprimento de onda) para promover catálise. Um outro tipo de dano, metilação de bases de guanina, está directamente revertida pela proteína metil-transferase metil guanina (MGMT), o equivalente bacteriana dos quais é chamado ogt. Este é um processo caro porque cada molécula de MGMT pode ser utilizada apenas uma vez; isto é, a reacção é estequiométrica em vez de catalítica . Uma resposta generalizada para agentes de metilação em bactérias é conhecido como o resposta adaptativa e confere um nível de resistência aos agentes alquilantes após exposição prolongada por supra-regulação de enzimas de reparação de alquilação. O terceiro tipo de danos no ADN revertida por células é determinada metilação da citosina e bases de adenina.
Danos de cadeia simples
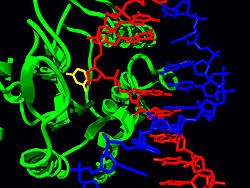
Quando apenas uma das duas cadeias de uma hélice dupla tem um defeito, a outra cadeia pode ser usado como um molde para orientar a correcção da cadeia danificado. A fim de reparar o dano a uma das duas moléculas de DNA emparelhadas, existe uma série de mecanismos de reparação de excisão de nucleótidos que removem o danificada e substituí-lo por um nucleótido não danificado complementar à encontrada na cadeia de ADN não danificado.
- Reparação de excisão de bases (BER), que repara os danos para uma única base provocada pela oxidação, alquilação, hidrólise, ou desaminação. A base danificada é removida por um Glicosilase de ADN. O "dente" é, em seguida, reconhecido por uma enzima chamada Endonuclease AP, que corta a Fosfodiéster vínculo. A parte que falta é então resynthesized por um A polimerase de ADN, e um A ligase de ADN efectua a etapa final de nick-selagem.
- Reparo por excisão de nucleotídeos (NER), que reconhece, lesões que distorcem hélice volumosos, como dímeros de pirimidina e 6,4 fotoprodutos. Uma forma especializada de NER conhecido como reparo acoplado à transcrição implanta enzimas NER para genes que estão sendo ativamente transcritas.
- Reparo incompatível (MMR), que corrige erros de A replicação do ADN e recombinação que resultam em nucleótidos mispaired (mas não danificadas).
Quebras de cadeia dupla
Quebras de cadeia dupla, em que ambas as vertentes da dupla hélice são cortadas, são particularmente perigosos para a célula, porque eles podem levar a rearranjos genômicos. Existem três mecanismos para reparar quebras de cadeia dupla (DSBs): extremidade não-homóloga de união (NHEJ), extremidade de união (MMEJ), e mediada por microhomology recombinação homóloga. PVN Acharya observou que quebras de cadeia dupla e uma "ligação transversal que une ambos os fios no mesmo ponto é irreparável porque nem vertente pode, então, servir como um modelo para o reparo. A célula vai morrer na próxima mitose ou, em alguns casos raros, mutar . "
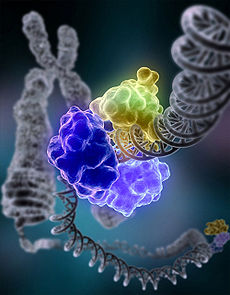
Em NHEJ, ADN-ligase IV, um especializado A ligase de ADN que forma um complexo com o cofactor XRCC4, junta-se diretamente nas duas extremidades. Para orientar reparação precisa, NHEJ depende de sequências homólogas curtos chamados microhomologies presente nas caudas de cadeia simples do ADN de extremidades a serem unidas. Se essas projeções são compatíveis, reparação é normalmente precisos. NHEJ também pode introduzir mutações durante a reparação. Perda de nucleotídeos danificados, no sítio ruptura pode levar a exclusões, e juntando-se de não correlação formas Termini translocações. NHEJ é especialmente importante antes de a célula foi replicado seu DNA, uma vez que não há um modelo disponível para a reparação por recombinação homóloga. Há "backup" em vias de NHEJ maiores eucariotas . Além de seu papel como um zelador genoma, NHEJ é necessário para unir quebras de cadeia dupla cobertas de hairpin induzidos durante V (D) J recombinação, o processo que gera diversidade em De células B e Receptores das células T no vertebrado sistema imunitário .
A recombinação homóloga é necessária a presença de uma sequência idêntica ou quase idêntica para ser usado como um modelo para a reparação da ruptura. A maquinaria enzimática responsável por este processo de reparação é quase idêntico ao da máquina responsável pela cruzamento cromossômica durante a meiose. Esta via permite que um cromossomo danificado para ser reparado com uma irmã os cromatídeos (disponível em G2 após a replicação do ADN) ou um cromossoma homóloga como um modelo. DSBs causados pela maquinaria de replicação de tentar sintetizar em uma única vertente pausa ou unrepaired causa lesão colapso da forquilha de replicação e normalmente são reparadas por recombinação.
Topoisomerases introduzir ambas as quebras simples e dupla vertente no curso de mudança de estado do DNA supercoiling, o que é especialmente comum em regiões próximas uma forquilha de replicação aberto. Tais rupturas não são considerados danos no ADN porque são um intermediário natural do mecanismo bioquímico de topoisomerase e é imediatamente reparada por as enzimas que eles criados.
Uma equipe de pesquisadores franceses bombardearam Deinococcus radiodurans para estudar o mecanismo de reparo do DNA ruptura de fita dupla nesse organismo. Pelo menos duas cópias do genoma, com quebras de DNA aleatório, podem formar fragmentos de DNA através de recozimento. Parcialmente fragmentos sobrepostos são então utilizados para a síntese de regiões homólogas através de um movimento D-loop que pode continuar extensão até se encontrar fios de parceiros complementares. No passo final, há cruzado por meio de RecA-dependente recombinação homóloga.
Síntese translesão
Síntese translesão (TLS) é um processo de tolerância aos danos de DNA que permite o Maquinaria de replicação de DNA de replicar DNA lesões passadas, tais como dímeros de timina ou Sítios AP. Trata-se de trocar as regulares As polimerases de ADN-polimerases para especializados translesão (isto é, ADN polimerase IV ou V, a partir da família da Polimerase Y), muitas vezes com sítios activos maiores, que podem facilitar a inserção das bases opostas nucleótidos danificados. A polimerase de comutação é pensado para ser mediada por, entre outros factores, a modificação pós-traducional da replicação fator de processabilidade PCNA. Polimerases de síntese translesão muitas vezes têm uma baixa fidelidade (alta propensão para inserir bases erradas) em modelos de não danificadas em relação ao polimerases regulares. No entanto, muitos são extremamente eficientes para a inserção de bases de correcção opostas tipos específicos de danos. Por exemplo, Pol η medeia desvio livre de erros de lesões induzidas por radiação UV , enquanto Pol ι introduz mutações nesses locais. Pol η é conhecido adicionar a primeira adenina através da Photodimer T ^ T usando Watson- Crick e a segunda base de adenina será adicionado na sua conformação syn usando Base emparelhamento Hoogsteen. Do ponto de vista celular, arriscando a introdução de mutações pontuais durante a síntese translesão pode ser preferível recorrer a mecanismos mais drásticas de reparação do DNA, que podem causar aberrações cromossómicas brutas ou a morte celular. Em suma, o processo envolve especializada polimerases ou ignorando ou reparação de lesões em locais de replicação do DNA parado. DNA polimerase eta pode ignorar DNA lesões complexas demais por exemplo guanina-timina reticulação intra-fio, G [8,5-Me] T, embora podem causar mutações alvo e semi-alvo. A toxicidade e mutagênese desta lesão foi estudada por replicar uma G plasmídeo [8,5-Me] T-modificado de Escherichia coli com nocautes DNA polimerase específicas. A viabilidade foi muito baixo em uma estirpe sem pol II, pol IV, V e pol, as polimerases de ADN de três-SOS indutiveis, indicando que a síntese translesão é conduzido principalmente por estas polimerases de ADN. Uma plataforma de bypass é fornecido a essas polimerases por Antígeno nuclear de proliferação celular (PCNA). Em circunstâncias normais, PCNA obrigado a replica o DNA polimerases. Num local de lesão, PCNA é ubiquitinadas, ou modificada pelo RAD6 / RAD18 proteínas para fornecer uma plataforma para as polimerases especializados para ignorar a lesão e retomar a replicação do DNA. Após a síntese translesão, a extensão é necessária. Esta extensão pode ser levada a cabo por uma polimerase replicativa se o TLS é livre de erros, como no caso de Pol η, ainda se TLS resulta em uma incompatibilidade, uma polimerase especializada é necessária a estendê-la; Ζ Pol. Pol ζ é o único que pode se estender descasamentos de terminais, enquanto polimerases mais processive não pode. Assim, quando uma lesão é encontrado, a forquilha de replicação irá parar, PCNA vai mudar de uma polimerase processive para uma polimerase de TLS como Pol ι para corrigir a lesão, então PCNA pode mudar para Pol ζ para estender a incompatibilidade, e PCNA última mudará para a polimerase processiva para continuar a replicação.
Resposta global a danos no DNA
As células expostas a radiação ionizante, luz ultravioleta ou produtos químicos são propensas a adquirir vários sites de DNA lesões volumosas e quebras de cadeia dupla. Além disso, agentes que danificam o ADN podem danificar outros biomoléculas tais como proteínas , carboidratos , lipídios , e ARN. O acúmulo de danos, para ser, quebras ou adutos parando a dupla vertente específica forquilhas de replicação, estão entre os sinais de estimulação conhecidos para uma resposta global a danos no DNA. A resposta global aos danos é um acto dirigido a própria preservação das células e desencadeia múltiplas vias de reparação macromolecular, contorno de lesão, tolerância, ou apoptose. As características comuns de resposta global são indução de múltipla genes, a paragem do ciclo celular, e a inibição de divisão celular.
DNA danos checkpoints
Depois de danos no ADN, ciclo celular postos de controle são ativados. Activação do ponto de verificação faz uma pausa no ciclo celular e fornece o tempo de células para reparar o dano antes de continuar a dividir. Postos de controle de danos no DNA ocorrem no G1 / S e G2 / M limites. Um intra- S checkpoint também existe. Ativação Checkpoint é controlado por dois mestre quinases, ATM e ATR. ATM responde a DNA quebras de cadeia dupla e rupturas na estrutura da cromatina, enquanto ATR responde principalmente para parado garfos de replicação. Estas quinases fosforilar alvos a jusante de um cascata de transdução de sinal, acabou levando a parada do ciclo celular. A classe de proteínas mediadoras checkpoint incluindo BRCA1, MDC1, e 53BP1 também foi identificado. Estas proteínas parecem ser necessários para transmitir o sinal de activação do ponto de verificação para proteínas a jusante.
Um alvo a jusante importante da ATM e ATR é p53, uma vez que é necessária para induzir apoptose após danos no DNA. O ciclina dependente de inibidores de quinase p21 é induzido por ambos os mecanismos dependentes de p53 e independentes de p53 e pode prender o ciclo celular em G1 / S e G2 / M, desactivando ciclina / complexos de quinase dependente de ciclina.
A resposta SOS procariótica
O Resposta SOS é as alterações na a expressão do gene em Escherichia coli e outras bactérias em resposta aos danos de DNA. O sistema SOS procariótica é regulado por duas proteínas-chave: LexA e RecA. O LexA é um homodímero transcricional repressor que se liga a sequências operadoras comumente referido como caixas SOS. Em Escherichia coli é sabido que regula a transcrição de LexA de cerca de 48 genes, incluindo os genes de lexA e recA. A resposta SOS é conhecido por ser difundido no domínio das bactérias, mas é quase ausente em alguns filos bacteriana, como o Espiroquetas. Os sinais celulares mais comuns de activação da resposta SOS são regiões de ADN de cadeia simples (ssDNA), decorrente parado forquilhas de replicação ou quebras de cadeia dupla, que são processados por DNA helicase para separar as duas cadeias de ADN. Na etapa de iniciação, a proteína liga-se a RecA ADNcs numa Hidrólise de ATP conduzido reacção criar filamentos de RecA-ADNcs. Filamentos de RecA-ssDNA activar LexA auto a actividade da protease, o que conduz finalmente à clivagem do dímero de LexA e subsequente degradação de LexA. A perda de LexA repressora induz a transcrição dos genes de SOS e permite uma maior indução de sinal, a inibição da divisão celular e um aumento nos níveis de proteínas responsáveis pelo processamento danos.
Em Escherichia coli, caixas SOS são 20 longas sequências de nucleotídeos perto de promotores com estrutura palindrómica e um elevado grau de conservação da sequência. Em outras classes e filos, a sequência de caixas SOS varia consideravelmente, com o comprimento e composição diferente, mas é sempre altamente conservada e um dos mais fortes sinais curtos no genoma. O alto teor de informação das caixas SOS permite diferencial de ligação de LexA de diferentes promotores e permite a temporização da resposta SOS. Os genes de reparo de lesão são induzidos no início da resposta SOS. As polimerases translesão sujeitas a erros, por exemplo, UmuCD'2 (também chamado de DNA polimerase V), são induzidos, mais tarde, como um último recurso. Uma vez que o dano do DNA ser reparado ou contornado utilizando polimerases ou através de recombinação, a quantidade de ADN de cadeia simples em células é reduzida, reduzindo as quantidades de filamentos de RecA diminui a actividade de clivagem de homodímero de LexA, o que, em seguida, liga-se as caixas SOS próximos promotores e restaurações a expressão do gene normal.
Respostas de transcrição eucariótico para danos de DNA
Eucarióticas células expostas a agentes danificadores do ADN também ativam vias defensivas importantes por induzir várias proteínas envolvidas no reparo do DNA, controle do ciclo celular checkpoint, tráfico e degradação de proteínas. Tal genoma ampla resposta transcricional é muito complexa e bem regulada, permitindo, assim, a resposta global coordenada a danos. Exposição de levedura Saccharomyces cerevisiae a agentes danificadores do ADN resulta na sobreposição mas os perfis de transcrição distintos. Semelhanças com ambiental resposta de choque que indica uma via de resposta de tensão geral global existem no nível de activação da transcrição. Em contraste, diferentes tipos de células humanas responder aos danos de forma diferente, indicando uma ausência de uma resposta global comum. A explicação provável para esta diferença entre células humanas e de levedura podem ser na heterogeneidade de mamíferos células. Em um animal diferentes tipos de células são distribuídas entre os diferentes órgãos que evoluíram diferentes sensibilidades a danos no ADN.
Em resposta global geral para danos de DNA envolve a expressão de múltiplos genes responsáveis pela reparação postreplication, recombinação homóloga, nucleotídeo reparo por excisão, DNA danos checkpoint, a ativação global de transcrição, genes que controlam decadência mRNA, e muitos outros. Uma grande quantidade de dano a uma célula deixa-lo com uma decisão importante: sofrer apoptose e morrer, ou sobreviver no custo de vida com um genoma modificado. Um aumento na tolerância a danos pode levar a um aumento da taxa de sobrevivência, que irá permitir que uma maior acumulação de mutações. Rev1 levedura e polimerase humana η são membros [DNA translesão família Y polimerases presentes durante resposta global aos danos de DNA e são responsáveis por mutagênese reforçada durante uma resposta global a danos no DNA em eucariotos.
Reparo do DNA e envelhecimento
Efeitos patológicos da pobre de reparo de DNA
Animais experimentais com deficiências genéticas no reparo do DNA, muitas vezes mostram diminuição tempo de vida e aumento da incidência de câncer. Por exemplo, camundongos deficientes na via NHEJ dominante e em mecanismos de manutenção dos telômeros chegar linfoma e infecções mais frequentemente, e, como conseqüência, têm expectativa de vida mais curtos do que camundongos selvagens. De modo semelhante, os ratinhos deficientes em proteína reparação e transcrição chave que se desenrola hélices de DNA têm início precoce de doenças relacionadas com o envelhecimento e consequente encurtamento da vida útil. No entanto, nem toda deficiência de reparo do DNA cria exatamente os efeitos previstos; camundongos deficientes na via NER exibiram reduzido tempo de vida sem taxas correspondentemente mais elevados de mutação.
Se a taxa de danos de ADN excede a capacidade das células para reparar, a acumulação de erros pode sobrecarregar a célula e resultar no início de senescência, apoptose, ou cancro. Doenças associadas com a reparação do ADN defeituosa resultado funcionando em envelhecimento prematuro Inherited, aumento da sensibilidade a agentes cancerígenos, e, correspondentemente, aumento do risco do cancro (ver abaixo ). Por outro lado, os organismos com sistemas de reparo de ADN melhoradas, tais como Deinococcus radiodurans, o organismo mais resistente à radiação conhecido, apresentam uma resistência notável para os efeitos indutores de ruptura de fita dupla de radioatividade, provavelmente devido à maior eficiência de reparo de DNA e especialmente NHEJ.
Longevidade e restrição calórica
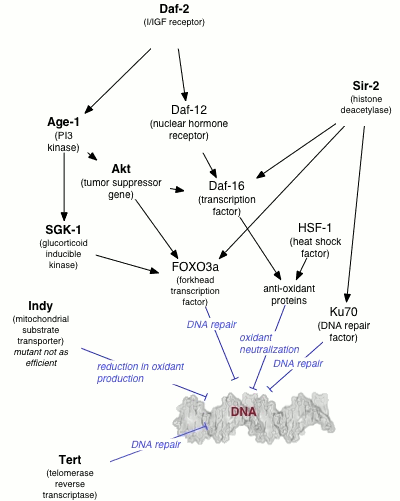
Uma série de genes individuais foram identificados como influenciando as variações no tempo de vida dentro de uma população de organismos. Os efeitos destes genes é fortemente dependente do ambiente, em particular, na dieta do organismo. A restrição calórica resulta em reprodutivelmente tempo prolongado numa variedade de organismos, provavelmente através vias sensoriais nutrientes e diminuiu taxa metabólica. Os mecanismos moleculares pelos quais tais resultados de restrição na vida alongada estão ainda por definir (ver, por alguma discussão); no entanto, o comportamento de vários genes conhecidos por estarem envolvidos na reparação do ADN é alterado em condições de restrição calórica.
Por exemplo, aumentando o dosagem de gene do gene SIR-2, o qual regula a embalagem do ADN nas verme nemátodo Caenorhabditis elegans, pode prolongar significativamente a vida útil. O homólogo de mamífero da SIR-2 é conhecida por induzir factores de reparação de ADN a jusante envolvidos na NHEJ, uma actividade que é especialmente promovido em condições de restrição calórica. A restrição calórica tem sido intimamente ligada à taxa de reparo por excisão de bases no DNA nuclear de roedores, embora os efeitos semelhantes não foram observados no DNA mitocondrial.
É interessante notar que a C. elegans gene AGE-1, um efector a montante das vias de reparo de DNA, confere vida dramaticamente ampliada em condições de alimentação de livre, mas leva a uma diminuição da aptidão reprodutiva em condições de restrição calórica. Esta observação apoia a pleiotropy da teoria origens biológicas do envelhecimento, o que sugere que os genes que conferem uma grande vantagem de sobrevivência no início da vida serão selecionados para até mesmo se eles carregam uma desvantagem correspondente tarde na vida.
Medicina e reparo do DNA modulação
Distúrbios hereditários de reparo de DNA
Defeitos no mecanismo NER são responsáveis por várias doenças genéticas, incluindo:
- Xeroderma pigmentoso: hipersensibilidade à luz solar / UV, resultando num aumento da incidência do cancro da pele e envelhecimento prematuro
- Síndrome de Cockayne: hipersensibilidade a UV e agentes químicos
- Tricotiodistrofia: pele sensível, cabelos quebradiços e unhas
Retardo mental muitas vezes acompanha os dois últimos distúrbios, sugerindo o aumento da vulnerabilidade dos neurônios de desenvolvimento.
Outros distúrbios de reparação de ADN incluem:
- Síndrome de Werner: envelhecimento prematuro e retardo de crescimento
- Luz solar hipersensibilidade, maior incidência de síndrome de Bloom malignidades (especialmente leucemias).
- Ataxia Telangiectasia: sensibilidade à radiação ionizante e alguns agentes químicos
Todas as doenças acima referidas são frequentemente chamados "segmentar progerias "(" acelerada doenças do envelhecimento ") porque suas vítimas parecem idosos e sofrem de doenças relacionadas com o envelhecimento numa idade anormalmente jovem, enquanto não manifestar todos os sintomas da velhice.
Outras doenças associadas com a função de reparação do ADN incluem reduzida Anemia de Fanconi, hereditária câncer de mama e hereditária câncer de cólon.
Reparo do DNA e câncer
Devido às limitações inerentes aos mecanismos de reparo do DNA, se os seres humanos viveram tempo suficiente, todos iriam eventualmente desenvolver câncer. Há pelo menos 34 Herdado mutações do gene de reparo do DNA humano que aumentam o risco de câncer. Muitas destas mutações causar a reparação do ADN a ser menos eficaz do que o normal. Em particular, Hereditário sem polipose câncer colorretal (HNPCC) está fortemente associada com mutações específicas no DNA de reparo incompatível via. BRCA1 e BRCA2, dois genes cujas mutações famosos conferem um risco extremamente aumentado de câncer de mama em suportes, são ambos associados com um grande número de vias de reparo de DNA, especialmente NHEJ e recombinação homóloga.
Procedimentos terapêuticos câncer, como quimioterapia e radioterapia trabalho por esmagadora a capacidade da célula para reparar danos no DNA, resultando na morte celular. Células que se dividem mais rápido - mais tipicamente células de câncer - são preferencialmente afetados. O efeito colateral é que outras células não-cancerosas, mas que se dividem rapidamente, tais como células estaminais na medula óssea são também afectados. Tratamentos modernos de cancro tentar localizar o dano de DNA para células e tecidos unicamente associados com o cancro, ou por meios físicos (concentração do agente terapêutico na região do tumor) ou por meios bioquímicos (exploram uma característica única de células cancerosas no corpo) .
Reparo do DNA e evolução
Os processos básicos de reparo de DNA são altamente conservada entre ambos os procariotas e eucariotas e mesmo entre bacteriófago ( vírus que infectam bactérias ); No entanto, os organismos mais complexos, com mais genomas complexos têm mecanismos de reparo correspondentemente mais complexos. A capacidade de um grande número de proteínas motivos estruturais para catalisar reacções químicas relevantes tem desempenhado um papel significativo na elaboração de mecanismos de reparação durante a evolução. Para uma avaliação extremamente detalhada das hipóteses relativas à evolução do reparo do DNA, ver.
O registro fóssil indica que a vida de uma única célula começaram a proliferar no planeta em algum momento durante o Pré-Cambriano período, embora exatamente quando reconhecidamente moderna vida surgiu pela primeira vez não é clara. Os ácidos nucleicos se tornou o meio única e universal de codificar informação genética, exigindo a reparação do ADN mecanismos que, em sua forma básica foram herdadas por todas as formas de vida existentes de seu ancestral comum. O surgimento de atmosfera rica em oxigénio da Terra (conhecida como o " catástrofe oxigénio "), devido à fotossintéticos organismos, bem como a presença de potencialmente nocivos de radicais livres na célula devido à fosforilação oxidativa, exigiu a evolução de mecanismos de reparação de ADN que actuam especificamente para combater os tipos de danos induzidos por estresse oxidativo.
Taxa de mudança evolutiva
Em algumas ocasiões, danos no ADN não é reparado, ou seja reparado por um mecanismo propensa a erro que resulta numa alteração da sequência original. Quando isto ocorre, as mutações podem propagar-se nos genomas da progenia da célula. Caso tal evento ocorrer numa célula germinal que irá, eventualmente, produzir um gameta, a mutação tem o potencial para ser passado para a descendência do organismo. A taxa de evolução de uma espécie em particular (ou, em um gene particular) é uma função da taxa de mutação. Como consequência, a taxa de precisão e de mecanismos de reparo de DNA têm uma influência sobre o processo de mudança evolutiva.

