
Vidro
Você sabia ...
Os artigos desta seleção Escolas foram organizados por tópico currículo graças a voluntários Crianças SOS. Você quer saber sobre o patrocínio? Veja www.sponsorachild.org.uk



O vidro é um amorfo (não cristalino ) o material sólido que apresenta uma de transição vítrea. Os vidros são tipicamente quebradiço e pode ser opticamente transparente.
O tipo mais conhecido de vidro, usada há séculos em janelas e vasos de beber, é vidro de soda-cal, composto por cerca de 75% de sílica (SiO2) mais óxido de sódio (Na2O) a partir de carbonato de sódio, cal (CaO), e vários aditivos menores. Muitas vezes, o vidro termo é utilizado num sentido restrito para se referir a esta utilização específica.
Na ciência, contudo, o termo vidro é geralmente definida num sentido mais amplo, incluindo todos os sólidos que possui um não cristalino (isto é, estrutura amorfa) e que exibe um transição vítrea quando aquecido para o estado líquido. Neste sentido mais amplo, vidros podem ser feitos de bastante diferentes classes de materiais: metálico ligas, derrete iónicos, soluções aquosas, líquidos, e moleculares polímeros. Para muitas aplicações ( garrafas, vidros de óculos) polímero ( vidro acrílico, policarbonato, tereftalato de polietileno) são uma alternativa mais leve para vidros de sílica tradicionais.
Vidro de silicato
Sílica (o composto químico de SiO 2) é um componente fundamental comum de vidro. Natural, a vitrificação de quartzo ocorre quando raio atinge areia , formando, estruturas rootlike ramificação ocos chamados fulgurite.
História
A história da criação de vidro pode ser rastreada até 3500 aC na Mesopotâmia . O vidro termo desenvolvido no final do Império Romano . Foi no Centro de fabricação de vidro romano em Trier, agora na Alemanha moderno, que o late-Latina glesum termo se originou, provavelmente a partir de um Palavra germânica para um transparente, substância lustrosa.
Ingredientes de vidro

Enquanto quartzo fundido (principalmente composto por SiO 2) é usado para algumas aplicações especiais, não é muito comum, devido ao seu elevado vidro temperatura de transição de mais de 1200 ° C (2192 ° F). Normalmente, outras substâncias são adicionadas para simplificar o processamento. Um é carbonato de sódio (Na 2 CO 3, "refrigerante"), o que reduz a temperatura de transição vítrea. No entanto, o refrigerante torna o vidro solúvel em água, o que é geralmente indesejável, assim Lima ( óxido de cálcio [CaO], geralmente obtida a partir de calcário), alguns óxido de magnésio (MgO) e óxido de alumínio (Al 2 O 3) são adicionados para proporcionar uma melhor durabilidade química. O vidro resultante contém cerca de 70 a 74% em peso de sílica e é chamado um vidro de soda-cal. Representam vidros de soda-cal para cerca de 90% do vidro fabricado.
A maioria dos vidros comum contém outros ingredientes adicionados para alterar suas propriedades. Vidro de chumbo ou sílex vidro é mais "brilhante" porque o aumento índice de refracção causa visivelmente mais reflexão especular e aumentou dispersão óptica. A adição de bário também aumenta o índice de refracção. Óxido de tório dá vidro alto índice de refração e baixa dispersão e antigamente era usada na produção de lentes de alta qualidade, mas devido à sua radioactividade foi substituído por óxido de lantânio em óculos modernos. O ferro pode ser incorporado em vidro para absorver energia infravermelha, por exemplo, na absorção de calor filtros para projetores de cinema, enquanto de cério (IV) de óxido pode ser usado para o vidro que absorve UV comprimentos de onda.
O que se segue é uma lista dos tipos mais comuns de óculos de silicato, e seus ingredientes, propriedades e aplicações:
- Vidro, sílica fundida, vidro de sílica vítrea: sílica (SiO2). Tem muito baixo de expansão térmica, é muito difícil e resiste temperaturas elevadas (1000-1500 ° C). Ele é também o mais resistente contra a intempérie (iões alcalinos lixiviação do vidro, enquanto que a coloração). Ele é usado para aplicações de alta temperatura, tais como tubos de fornos, cadinhos de fusão, etc.
- Soda-cal-sílica de vidro, vidro de janela: sílica 72% + óxido de sódio (Na2O) + 14,2% de magnésia (MgO) 2,5% + cal (CaO) 10,0% de alumina + (Al 2 O 3) 0,6%. É transparente, facilmente formado e mais adequado para vidro de janela. Ele tem uma expansão térmica de alta e baixa resistência ao calor (500-600 ° C). Usado para janelas, recipientes, lâmpadas, utensílios de mesa.
- Vidro de borosilicato de sódio, Pyrex: sílica 81% + óxido bórico (B 2 O 3) 12 +% de soda (Na 2 O) + 4,5% de alumina (Al 2 O 3) 2,0%. Stands expansão térmica muito melhor do que o vidro da janela. Usado para produtos vidreiros químicos, cozinhar vidro, lâmpadas de cabeça carro, etc. Vidros de borosilicato (p.ex. Pyrex) têm como principais constituintes de sílica e óxido de boro. Eles têm bastante baixos coeficientes de expansão térmica (CTE Pyrex 7740 é de 3,25 x 10 -6 / ° C, em comparação com cerca de 9 x 10 -6 / ° C durante um vidro de soda-cal típico), o que os torna mais estável dimensionalmente. O CTE inferior também os torna menos sujeito a estresse causado por de expansão térmica, portanto, menos vulnerável a craqueamento de choque térmico. Eles são comumente usados para frascos de reagentes, componentes ópticos e utensílios domésticos.
- Conduz-óxido de vidro, vidro de cristal: sílica 59% + sódio (Na2O) + 2,0% de óxido de chumbo (PbO) + 25% de óxido de potássio (K2O) + 12% de alumina 0,4% + óxido de zinco (ZnO), 1,5% . Tem um alto índice de refração, tornando o visual de objectos de vidro mais brilhante (cristal). Ele também tem uma elevada elasticidade, tornando-copos 'anel'. Também é mais viável na fábrica, mas não suporto a aquecer muito bem.
- Vidro de aluminossilicato: sílica 57% + 16% de alumina + óxido bórico (B 2 O 3) + 4,0% de óxido de bário (BaO) + 6,0% MgO 7,0% + 10% de cal. Amplamente utilizado para fibra de vidro, utilizados para fabricação de plástico reforçado com vidro (barcos, varas de pesca, etc.). Também para lâmpada de halogéneo de vidro.
- Vidro de óxido: de alumina de 90% de óxido de germânio + (GeO2) 10%. Vidro extremamente clara, usado para guias de onda de fibra óptica em redes de comunicação. Luz perde apenas 5% de sua intensidade através de 1 km de fibra de vidro.
Outro ingrediente vidro comum é "cullet" ( vidro reciclado). O vidro reciclado economiza em matérias-primas e energia; no entanto, as impurezas no casco pode levar a falha do produto e equipamentos.
Agentes de colagem, tais como sulfato de sódio , cloreto de sódio , ou óxido de antimónio pode ser adicionado para reduzir o número de bolhas de ar na mistura de vidro. Cálculo do lote de vidro é o método pelo qual a mistura de matérias-primas correcta é determinada para obter a composição de vidro desejada.
Produção de vidro contemporâneo

Seguindo preparação do lote de vidro e de mistura, as matérias-primas são transportadas para o forno. Vidro sodo-cálcico para produção em massa é derretido em gás unidades. Fornos de menor escala para óculos especiais incluem aparelhos de fusão elétricos, fornos de cadinho e tanques diários.
Após a fusão, homogeneização e de refinação (remoção de bolhas), o copo está formado. O vidro plano para janelas e aplicações semelhantes é formado pela processo de vidro float, desenvolvido entre 1953 e 1957 por Sir Alastair Pilkington e Kenneth Bickerstaff da Pilkington irmãos do Reino Unido, que criou uma fita contínua de vidro usando um banho de estanho fundido no qual o vidro fundido flui sem entraves sob a influência da gravidade. A superfície superior do vidro é submetido a azoto sob pressão para se obter um acabamento polido. Vidro de embalagem para garrafas e frascos comuns é formada por sopro e métodos de prensagem. Outras técnicas de formação de vidro encontram-se resumidos na tabela Formando vidro técnicas.
Uma vez que a forma desejada é obtida, o vidro é geralmente recozido para a remoção de tensões. Tratamento de Superfícies, revestimentos ou laminação pode seguir para melhorar a durabilidade química ( revestimentos de recipiente de vidro, vidro de embalagem tratamento interno), força ( vidro temperado, vidro à prova de balas, pára-brisas), ou propriedades ópticas ( vidraça isolante, revestimento anti-reflexo).
Arquitetura
O uso de vidro em edifícios é uma característica transparente para permitir a entrada de luz em salas e pisos, iluminando espaços fechados e enquadrar vista para o exterior através de um janela. É também um material para as divisórias internas e externas revestimento.
Vidraria em laboratório
Novas composições de vidro química ou novas técnicas de tratamento podem inicialmente ser investigados em experiências laboratoriais de pequena escala. As matérias-primas para derreter vidro de laboratório escala são muitas vezes diferentes das que são utilizadas na produção em massa porque o factor de custo, tem uma prioridade baixa. No laboratório principalmente puro produtos químicos são utilizados. Deve ser tomado cuidado de que as matérias-primas não tenham reagido com a humidade ou outros produtos químicos no meio ambiente (por exemplo, alcalina ou alcalino-terroso e óxidos de metais ou hidróxidos, óxido de boro), ou que as impurezas são quantificados (perda de ignição). As perdas por evaporação durante a fusão de vidro deve ser considerado quando da escolha das matérias-primas, por exemplo, selenito de sódio pode ser preferido em relação facilmente evaporando SeO2. Além disso, reagem mais prontamente matérias-primas podem ser preferidos em relação relativamente os inertes, tais como Al (OH) 3 sobre Al 2 O 3 . Normalmente, os fundidos são realizadas em cadinhos de platina para reduzir a contaminação a partir do material do cadinho. Vidro a homogeneidade é conseguida por homogeneização da mistura de matérias-primas ( fornada de vidro), por agitação à massa fundida, e por esmagamento e re-fusão do primeiro material fundido. O vidro obtido é geralmente recozido para impedir a ruptura durante o processamento.
A fim de fazer o vidro a partir de materiais com fraca formação de vidro tendências, novas técnicas são usadas para aumentar a velocidade de arrefecimento, ou reduzir os gatilhos de nucleação de cristais. Exemplos destas técnicas incluem levitação aerodinâmica (o arrefecimento do fundido enquanto ele flutua em uma corrente de gás), têmpera splat (pressionando a fusão entre duas bigornas de metal) e extinção de rolo (a fundição por rolos).
Veja também: Design de lentes ópticas, Fabrico e teste de componentes ópticos
Outros vidros
Óculos de rede

Alguns vidros que não incluem a sílica como um dos principais constituintes podem ter propriedades físico-químicas úteis para a sua aplicação em fibras ópticas e outras aplicações técnicas especializadas. Estes incluem vidros de fluoretos, aluminossilicatos, vidros de fosfato, vidros de borato, e vidros calcogenetos.
Existem três classes de componentes para óculos de óxido: formadores de rede, intermediários, e modificadores. Os formadores de rede (silício, boro, germânio) formar uma rede altamente reticulada de ligações químicas. Os intermediários (de titânio, alumínio, zircónio, berílio, magnésio, zinco) podem actuar como ambos os formadores e modificadores da rede, de acordo com a composição do vidro. Os modificadores (cálcio, chumbo, lítio, sódio, potássio) alterar a estrutura da rede; elas estão geralmente presentes como iões, compensada por átomos de oxigénio não vizinhos, ligados em ponte por uma ligação covalente com a rede de vidro e segurando uma carga negativa para compensar o ião positivo nas proximidades. Alguns elementos podem desempenhar múltiplos papéis; por exemplo, o chumbo pode actuar tanto como uma rede anterior (Pb 4+ 4+ substituindo Si), ou como um modificador.
A presença de átomos de oxigénio não-ponte reduz o número relativo de ligações fortes no material e interrompe a rede, diminuindo a viscosidade do fundido e diminuir a temperatura de fusão.
Os iões de metal alcalino são pequenos e móvel; a sua presença no vidro permite um grau de condutividade eléctrica, especialmente em estado derretido ou a temperatura elevada. A sua mobilidade, no entanto, diminui a resistência química do vidro, o que permite a lixiviação pela água e facilitando a corrosão. Íons alcalino-terrosos, com suas duas cargas positivas e exigência de dois íons de oxigênio não-ponte para compensar sua carga, são a difusão muito menos móvel si e também impedir de outros íons, especialmente os álcalis. Os óculos comerciais mais comuns contêm íons alcalinos e alcalino-terrosos (geralmente sódio e cálcio), para o processamento mais fácil e satisfatória resistência à corrosão. A resistência à corrosão de vidro pode ser obtida por dealkalization, remoção dos iões alcalinos da superfície do vidro, por reacção com por exemplo compostos de enxofre ou de flúor. A presença de iões de metais alcalinos também tem efeito prejudicial para o perda tangente do vidro, e a sua resistência eléctrica ; vidros para eletrônica (vedação, tubos de vácuo, lâmpadas ...) tem que levar isso em conta.
A adição de conduzir (II) óxido reduz o ponto de fusão, abaixa viscosidade da massa fundida, e aumentos índice de refração. Óxido de chumbo também facilita a solubilidade de outros óxidos metálicos e, por conseguinte, é utilizado em vidros coloridos. A diminuição da viscosidade de fusão de vidro de chumbo é muito significativas (cerca de 100 vezes em comparação com óculos de refrigerante); isso permite uma fácil remoção de bolhas e trabalhar a temperaturas mais baixas, daí o seu uso frequente como aditivo na esmaltes vítreos e soldas de vidro. A alta raio iónico de iões de Pb 2+ torna altamente imobilizado na matriz, e impede o movimento de outros iões; levar vidros, portanto, têm alta resistência elétrica, cerca de duas ordens de grandeza maior do que o vidro de soda-cal (10 vs 8,5 10 6,5 ohm · cm, DC a 250 ° C). Para mais detalhes, consulte vidro de chumbo.
A adição de flúor diminui o constante dieléctrica de vidro. O flúor é altamente eletronegativo e atrai os elétrons na rede, diminuindo a polarizabilidade do material. Tal silício-dióxido de fluoreto é utilizado no fabrico de circuitos integrados como um isolante. Altos níveis de dopagem de flúor levar à formação de voláteis SiF 2 O e em seguida, tal vidro é termicamente instável. Camadas estáveis foram conseguidos com constante dielétrica para cerca de 3,5-3,7.
Metais amorfos

No passado, os pequenos lotes de metais amorfos com configurações de alta superfície de área (fitas, fios, filmes, etc.) foram produzidos através da implementação de taxas extremamente rápidas de arrefecimento. Este foi inicialmente chamado de "arrefecimento splat" pelo estudante de doutorado no Caltech W. Klement, que mostrou que as taxas de resfriamento da ordem de milhões de graus por segundo é suficiente para impedir a formação de cristais, e os átomos metálicos ficarem "presos" em um estado vítreo. Fios de metal amorfos têm sido produzidos por pulverização catódica de metal fundido sobre um disco rotativo de metal. Mais recentemente, um número de ligas têm sido produzidas em camadas com espessura superior a 1 milímetro. Estes são conhecidos como os vidros metálicos a granel (BMG). Liquidmetal Technologies vender um número de BMGs à base de zircônio. Os lotes de aço amorfo também foram produzidos que demonstram propriedades mecânicas muito superiores aos encontrados nas ligas de aço convencionais.
Em 2004, Os investigadores do NIST apresentou provas de que um isotrópico fase metálica não cristalino (apelidado de "q-glass") poderiam ser cultivadas a partir da fusão. Esta fase é a primeira fase, ou fase "primário", para formar no sistema Al-Fe-Si durante um arrefecimento rápido. Curiosamente, a evidência experimental indica que formas essa fase por uma transição de primeira ordem. A microscopia electrónica de transmissão (TEM) imagens mostram que as nucleia-q de vidro a partir do fundido na forma de partículas discretas, que crescem esfericamente, com uma taxa de crescimento uniforme em todas as direcções. O padrão de difração mostra que ela é uma fase vítrea isotrópico. No entanto, há uma barreira nucleação, o que implica uma descontinuidade interfacial (ou superfície interna) entre o vidro e o material fundido.
Eletrólitos
Os electrólitos ou fundidos sais são misturas de diferentes iões . Numa mistura de três ou mais espécies iónicas de um tamanho e forma diferentes, a cristalização pode ser tão difícil que o líquido pode ser facilmente supercooled em um vidro. O melhor exemplo é estudado Ca 0,4 K 0,6 (NO 3) 1.4.
As soluções aquosas
Algumas soluções aquosas pode ser super-arrefecida em um estado vítreo, por exemplo, LiCl: R H2O na gama de composição 4 <R <8.
Líquidos moleculares
Um líquido molecular é constituída por moléculas que não formam uma rede covalente mas interagem apenas através fraco forças de van der Waals ou através transiente ligações de hidrogênio. Muitos líquidos moleculares podem ser super-resfriado em um copo; alguns são excelentes formadores de vidro que, normalmente, não cristalizam.
Um exemplo é amplamente conhecido vidro açúcar.
Sob condições extremas de pressão e temperatura de sólidos pode apresentar grandes modificações estruturais e físicas que podem levar a transições de fase polyamorphic. Em 2006, cientistas italianos criaram uma fase amorfa de dióxido de carbono usando a pressão extrema. A substância foi nomeado carbonia amorfo (a-CO 2) e apresenta uma estrutura atómica semelhante a de sílica.
Polímeros
Vidros coloidais
Concentrado As suspensões coloidais podem apresentar uma transição vítrea distinta como função da concentração de partículas ou densidade.
De vitrocerâmica
Materiais de vidro e de cerâmica compartilham muitas propriedades, com tanto de vidro não cristalino e cristalino cerâmica. Eles são formados como um copo, e, em seguida, parcialmente cristalizado por tratamento térmico. Por exemplo, a microestrutura da cerâmica de porcelana, faiança contém frequentemente tanto e amorfo fases cristalinas. Grãos cristalinos são frequentemente incorporados dentro de uma fase intergranular não cristalina de limites de grão. Quando aplicado a cerâmicas de mesa, vítreo significa que o material tem um extremamente baixo permeabilidade aos líquidos, muitas vezes, mas nem sempre de água, quando determinado por um regime de ensaio especificada.
O termo refere-se principalmente a uma combinação de lítio e aluminossilicatos que produz uma variedade de materiais com propriedades termomecânicas interessantes. O mais importante comercialmente destes tem a distinção de ser impermeável ao choque térmico. Assim, de vitrocerâmica tornaram-se extremamente útil para a bancada de cozinha. O negativo coeficiente de expansão térmica (CET) da fase cerâmica cristalino pode ser equilibrada com o CTE positivo da fase vítrea. Em um certo ponto (~ 70% cristalino) o vidro cerâmico tem uma CTE líquido próximo de zero. Este tipo de exibe vidro-cerâmica excelentes propriedades mecânicas e podem sustentar repetido e rápida de temperatura altera-se a 1000 ° C.
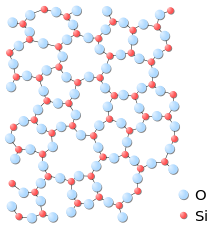
Estrutura
Como em outra sólidos amorfos, a estrutura atômica de um copo carece de qualquer longo alcance periodicidade translacional. No entanto, devido a ligação química características vidros que possuem um elevado grau de ordem de curto alcance com respeito ao atómica locais poliedros .
Vidro contra líquido super-resfriado
Na física, a definição padrão de um copo (ou sólido vítreo) é um sólido formado por uma rápida extinção de fusão. No entanto, o vidro termo é frequentemente usado para descrever qualquer sólido amorfo que apresenta uma temperatura de transição vítrea Tg. Se o arrefecimento for suficientemente rápido (em relação à característica tempo de cristalização), em seguida, a cristalização é impedido e em vez disso a configuração atómica desordenada do líquido super-resfriado é congelada no estado sólido a T g. Geralmente, a estrutura de um vidro existe numa estado metaestável em relação ao seu forma cristalina, embora em certas circunstâncias, por exemplo em polímeros atácticos, não há análogo cristalino da fase amorfa.
Algumas pessoas consideram vidro para ser um líquido devido à sua falta de uma primeira ordem transição de fase em que certas termodinâmico variáveis, tais como o volume , entropia e entalpia são descontínuas através da gama de transição para vidro. No entanto, o de transição vítrea pode ser descrita como semelhante a uma transição de fase de segunda ordem em que as variáveis termodinâmicas intensivos, tais como o expansividade térmica e capacidade de calor são descontínuos. Apesar disso, a teoria do equilíbrio de transformações de fase não inteiramente segurar para o vidro, e, consequentemente, a transição de vidro não pode ser classificada como uma das transformações de fase de equilíbrio clássicos em sólidos.
| Qual é a natureza do de transição entre a forma de um sólido ou fluido regular e uma fase vítrea? "O problema não resolvido mais profundo e mais interessante em teoria do estado sólido é, provavelmente, a teoria da natureza do vidro e da transição vítrea". PW Anderson |
O vidro é um sólido amorfo. Ele exibe uma estrutura atómica perto ao observado na fase líquida mas supercooled mostra todas as propriedades mecânicas de um sólido. A noção de que o vidro flui de forma apreciável durante longos períodos de tempo não é suportado pela pesquisa empírica ou análise teórica (veja viscosidade de materiais amorfos). Medidas de laboratório de fluxo de vidro temperatura ambiente mostram um movimento consistente com um material de viscosidade da ordem de 10 17 -10 18 Pa s.
Embora a estrutura atómica de vidro partes características da estrutura numa supercooled líquido, vidro tende a comportar-se como um sólido abaixo da sua temperatura de transição vítrea. Um líquido sobrearrefecido se comporta como um líquido, mas é inferior ao ponto de congelação do material, e, em alguns casos irá cristalizar quase imediatamente se um cristal é adicionado como um núcleo. A mudança na capacidade de aquecer a uma transição vítrea e uma transição em fusão de materiais comparáveis são normalmente da mesma ordem de grandeza, indicando que a alteração na activa graus de liberdade é comparável também. Tanto num copo e em um cristal que é principalmente apenas o graus de liberdade vibracionais que permanecem ativos, ao passo que e rotacional movimento de translação é preso. Isso ajuda a explicar por que tanto cristalina e não cristalina sólidos exibem rigidez em escalas de tempo mais experimentais.
Comportamento de vidro antigo
A observação de que janelas antigas são encontrados às vezes a ser mais espessa na parte inferior do que no topo é muitas vezes oferecido como elementos de prova para a vista que o vidro flui sobre uma escala de tempo de séculos. O pressuposto é que o vidro foi uma vez uniforme, mas fluiu para a sua nova forma, que é uma propriedade de um líquido. No entanto, essa suposição é incorreta; uma vez solidificado, vidro não flui mais. A razão para a observação é que, no passado, quando os painéis de vidro foram feitos geralmente por vidreiros, a técnica utilizada foi a girar o vidro fundido, de modo a criar um círculo, predominantemente plano e mesmo prato (o processo vidro coroa, descrito acima). Esta placa foi então cortado para se ajustar de uma janela. As peças não foram, no entanto, absolutamente plana; as bordas do disco tornou-se uma espessura diferente como o vidro de girar. Quando instalado num quadro de janela, o vidro será colocado com o lado mais grosso para baixo, tanto por uma questão de estabilidade e para evitar que a água que se acumula no chumbo cames na parte inferior da janela. Ocasionalmente, tal vidro foi encontrado lado mais fino ou mais espesso para baixo em ambos os lados da borda da janela, o resultado da falta de cuidado durante a instalação.
A produção em massa dos vidros das janelas de vidro no início do século XX causou um efeito semelhante. Em fábricas de vidro, o vidro fundido foi vertida numa mesa de arrefecimento grande e deixou-se espalhar. O vidro resultante é mais espessa no local do derrame, localizado no centro da grande folha. Estas folhas foram cortadas em pequenos painéis de janela com espessura não uniforme, tipicamente com a localização do vazamento centrado em um dos painéis (conhecido como "olhos de boi") para efeito decorativo. Vidro moderno destinado a janelas é produzido como flutuar vidro e é muito uniforme em espessura.
Vários outros pontos se pode considerar que contradizem a teoria do "fluxo de vidro catedral":
- Escrevendo no American Journal of Physics, engenheiro de materiais Edgar D. Zanotto afirma "... o previsto tempo de relaxamento para GeO2 em temperatura ambiente é 10 32 anos. Assim, o período de relaxamento (tempo de fluxo característico) de óculos catedral seria ainda mais ". (10 32 anos é muitas vezes mais do que o estimado idade do Universo .)
- Se o vidro medieval fluiu perceptivelmente, em seguida, romano antigo e objetos egípcios devem ter fluído proporcionalmente mais - mas isso não é observado. Da mesma forma, pré-histórico lâminas de obsidiana deveria ter perdido sua borda; Isto não é observado quer (embora obsidiana podem ter uma diferente viscosidade do vidro da janela).
- Se o vidro flui a uma velocidade que permite que as alterações para ser visto a olho nu, depois de séculos, em seguida, o efeito deve ser visível em antigas telescópios . Qualquer ligeira deformação nas lentes telescópicas antigas levaria a uma diminuição drástica do desempenho óptico, um fenômeno que não é observado.
- Há muitos exemplos de séculos de idade, prateleiras de vidro que não tenha dobrados, mesmo que ele está sob estresse muito maior de cargas gravitacionais do que a janela de vidro vertical.
A descrição acima não se aplica a materiais que têm uma temperatura de transição vítrea próxima da temperatura ambiente, tais como certos plásticos usados na vida diária, como poliestireno e polipropileno.
Propriedades físicas
Propriedades ópticas
O vidro é usado em larga escala devido, em grande parte à produção de composições de vidro que são transparentes aos comprimentos de onda visíveis de luz. Em contraste, materiais policristalinos não fazer em transmissão geral de luz visível. Os cristais individuais podem ser transparente, mas as suas facetas ( limites de grão) reflectem ou dispersão da luz resultante em reflexão difusa. O vidro não contêm as subdivisões internas associadas com contornos de grão em policristais e, portanto, não dispersam a luz da mesma maneira como um material policristalino. A superfície do vidro é muitas vezes uma suave uma vez que durante a formação de vidro as moléculas do líquido sobrearrefecido não são forçados a dispor em geometrias de cristal rígidas e pode seguir a tensão superficial , o que impõe uma superfície lisa ao microscópio. Essas propriedades, que dão vidro sua clareza, pode ser mantida, mesmo que o vidro é parcialmente de absorção de luz ou seja colorido.
O vidro tem a capacidade de refratar, refletir e transmitir luz seguinte ótica geométrica, sem espalhando-lo. É utilizado no fabrico de lentes e janelas. Vidro comum tem um índice de refracção de cerca de 1,5. Conforme Equações de Fresnel, o reflectividade de uma folha de vidro é de cerca de 4% por superfície (em incidência normal no ar), e o transmissividade de um elemento (duas superfícies) é de cerca de 90%. O vidro também encontra aplicação em optoelectrónica por exemplo, para a transmissão de luz de fibras ópticas .
Cor
Cor em vidro pode ser obtido através da adição de iões electricamente carregados (ou centros de cor) que são distribuídos de forma homogénea, e por precipitação de partículas finamente dispersas (como em óculos fotossensíveis). Ordinário vidro de soda-cal aparece incolor para o olho nu quando é fina, embora ferro (II) de óxido de (FeO) impurezas de até 0,1% em peso de produzir uma tonalidade verde, que pode ser visto em pedaços grossos ou com o auxílio de instrumentos científicos. Além disso FeO e Cr 2 O 3 adições podem ser utilizados para a produção de garrafas verdes. enxofre , em conjunto com o carbono e sais de ferro, é utilizado para formar polissulfuretos de ferro e produzir vidro âmbar que vão desde amarelada a quase preto. A fusão de vidro também pode adquirir uma cor âmbar de uma atmosfera de combustão reduzindo. O dióxido de manganês pode ser adicionado em pequenas quantidades para remover a coloração verde dada por óxido de ferro (II). Quando usado em arte em vidro ou vidro estúdio de vidro é colorido usando receitas bem guardados que envolvem combinações específicas de óxidos metálicos, temperaturas de fusão e tempos de 'cozinhar'. A maioria vidro colorido usado no mercado de arte é fabricado no volume por fornecedores que atuam neste mercado, embora existam alguns fabricantes de vidro com a capacidade de fazer a sua própria cor de matérias-primas.
Arte em vidro

A partir do século 19, vários tipos de vidro fantasia começou a se tornar sucursais importantes do artes decorativas. Vidro Cameo foi revivido pela primeira vez desde os romanos, inicialmente usado principalmente para peças de um neo-clássico estilo. O Art Nouveau movimento em particular fez grande uso de vidro, com René Lalique, Émile Gallé, e Daum Nancy de nomes importantes da primeira onda francesa do movimento, produzindo vasos coloridos e peças semelhantes, muitas vezes em vidro cameo, e também utilizando técnicas de brilho. Louis Comfort Tiffany na América especializada em vitrais secular, na maior parte dos indivíduos de plantas, tanto em painéis e as suas lâmpadas famosas. A partir do século 20, alguns artistas de vidro começaram a se classe como no efeito escultores que trabalham em vidro, e como parte das artes plásticas .
Várias das técnicas mais comuns para a produção de arte em vidro incluem: soprando, forno de fundição, fusão, caindo, pate-de-verre, chama-working, hot-esculpir e frio de trabalho. Trabalho a frio inclui vitrais trabalho tradicional, bem como outros métodos de modelagem de vidro à temperatura ambiente. O vidro também pode ser cortado com uma serra de diamante, ou rodas de cobre incorporado com abrasivos, e polido para dar reluzente facetas; a técnica utilizada na criação Cristal Waterford. Art às vezes é gravado em vidro através do uso de substâncias ácidas, cáusticas, ou abrasivos. Tradicionalmente isso foi feito depois que o vidro foi soprado ou elenco. Na década de 1920 um novo processo molde-etch foi inventada, em que a arte foi gravado directamente no molde, de modo que cada peça fundida emergiu a partir do molde com a imagem já na superfície do vidro. Isso reduziu os custos de produção e, combinadas com uma maior utilização de vidro colorido, levaram a vidraria barato em 1930, que mais tarde se tornou conhecida como Depressão vidro. Como os tipos de ácidos usados neste processo são extremamente perigosos, métodos abrasivos ganharam popularidade.
Objetos feitos de vidro incluem não apenas os objetos tradicionais, tais como vasos ( tigelas, vasos, garrafas e outros recipientes), identificativas, mármores, grânulos, mas uma gama infinita de escultura e arte de instalação também. Vidro colorido é muitas vezes utilizado, embora, por vezes, o vidro é pintado, existem inúmeros exemplos do uso de vitrais.
Museus
Além de coleções históricas em museus gerais, obras de arte moderna em vidro pode ser visto em uma variedade de museus, incluindo o Museu Chrysler, a Museum of Glass, em Tacoma, o Metropolitan Museum of Art, o Museu de Arte de Toledo, e Corning Museum of Glass, em Corning, NY, que abriga a maior coleção do mundo de arte em vidro e história, com mais de 45.000 objetos em sua coleção. Em Fevereiro de 2000, a Smith Museum of Stained Glass Windows, localizado em Chicago de Navy Pier, inaugurado como o primeiro museu da América dedicado exclusivamente para vitrais. O museu apresenta obras de Louis Comfort Tiffany e John Lafarge, e está aberto diário gratuito ao público.
O Harvard Museu de História Natural tem uma coleção de modelos extremamente detalhadas de flores feitas de vidro pintado. Estes eram lampworked por Leopold Blaschka e seu filho Rudolph, que nunca revelou o método que ele usou para fazê-los. O Blaschka Flores de vidro ainda é uma inspiração para glassblowers hoje.








