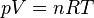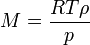Massa molar
Sobre este escolas selecção Wikipedia
SOS acredita que a educação dá uma chance melhor na vida de crianças no mundo em desenvolvimento também. Crianças SOS tem cuidado de crianças na África por 40 anos. Você pode ajudar o seu trabalho na África ?
Massa molar, o símbolo M, representa a massa de uma mole de uma substância ( elemento químico ou composto químico ). É um propriedade física que é característica de cada substância pura. A base Unidade SI para a massa é o quilograma , mas, por razões práticas e históricas, massas molares são quase sempre citado em gramas por mole (g / mol ou g mol -1), especialmente em química .
Massa molar está intimamente relacionado com o peso da fórmula (FW) ou parente massa molar (M r) de um composto, e ao massas atómicas relativas ou a pesos atômicos padrão de seus elementos constitutivos. No entanto, deve ser distinguida da massa molecular , que é a massa de uma molécula (de qualquer composição isotópica único) e não está directamente relacionada com o massa atómica, a massa de um átomo (de um único isótopo). O Dalton, Da símbolo, também é por vezes utilizado como uma unidade de massa molar, especialmente em bioquímica , com a definição 1 da = 1 g / mol, não obstante o facto de que é estritamente uma unidade de massa molecular (1 Da = 1,660 538 782 (83) -27 × 10 kg).
Massas molares quase nunca são medidos diretamente. Eles podem ser calculadas a partir dos pesos atómicos padrão, e muitas vezes são listados em catálogos de produtos químicos e em folhas de dados de segurança (FDS). Massas molares tipicamente variar entre:
- 1-238 g / mol de átomos de elementos de ocorrência natural;
- 10-1000 g / mol para os compostos químicos simples;
- 1000-5,000,000 g / mol para polímeros, proteínas , DNA fragmentos, etc.
Massas molares dos elementos
A massa molar de átomos de um elemento é dada pela peso atómico do elemento padrão multiplicado pela constante de massa molar, M u = 1 × 10 -3 kg / mol = 1 g / mol:
- M (H) = 1,007 97 (7) 1 × g / mole = 1,007 94 (7) g / mol
- H (S) = 32,065 (5) 1 × g / mol = 32,065 (5) g / mol
- H (Cl) = 35,453 (2) 1 × g / mol = 35,453 (2) g / mol
- H (Fe) = 55,845 (2) 1 × g / mol = 55,854 (2) g / mol
Multiplicando por a massa molar constante assegura que o cálculo é dimensionalmente correto: pesos atômicos são quantidades adimensionais (ou seja, números puros), enquanto massas molares têm unidades (neste caso, g / mol).
Alguns elementos normalmente são encontrados como moléculas , por exemplo, hidrogénio (H2), enxofre (S 8), cloro (Cl 2). A massa molar de moléculas desses elementos é a massa molar dos átomos multiplicado pelo número de átomos em cada molécula:
- H (H 2) = 2 × 1,007 97 (7) 1 × g / mol = 2,015 88 (14) g / mol
- H (S 8) = 8 × 32,065 (5) 1 × g / mol = 256,52 (4) g / mol
- H (Cl 2) = 2 × 35,453 (2) 1 × g / mol = 70,906 (4) g / mol
Massas molares dos compostos
A massa molar de um composto é dada pela soma da pesos atómicos padrão dos átomos que formam o composto multiplicado pela constante de massa molar, M u:
- M (NaCl) = [22,989 769 28 (2) + 35,453 (2)] x 1 g / mol = 58,443 (2) g / mol
- H (C 12 H 22 O 11) = ([12 × 12,0107 (8)] + [22 × 1,007 94 (7)] + [11 × 15,9994 (3)]) 1 × g / mol = 486,424 (10) g / mol
Uma massa molar média pode ser definido para as misturas de compostos. Isto é particularmente importante em ciência de polímeros, em que diferentes moléculas de polímero podem conter diferentes números de unidades de monómero (polímero não-uniformes).
Propriedades relacionadas
Peso molecular (MW) e peso fórmula (FW) são termos mais velhos para o que é agora mais corretamente chamado de relação de massa molar (M r). Isto é um quantidade adimensional (isto é, um número puro, sem unidades) igual a massa molar dividida pela constante de massa molar.
Massa molecular
A massa molecular (m) é a massa de uma dada molécula: ela é medida em dalton (Da) ou unidades de massa atómica (u), onde 1 Da = 1 u = 538 1.660 782 (83) -27 × 10 kg). Moléculas diferentes de um mesmo composto pode ter diferentes massas moleculares, porque eles contêm diferentes isótopos de um elemento. A massa molar é uma medida da massa molecular média de todas as moléculas numa amostra, e é geralmente a medida mais apropriada quando se lida com macroscópicas (pesáveis) as quantidades de uma substância.
As massas moleculares são calculados a partir da massas atómicas relativas de cada nuclídeo, enquanto massas molares são calculados a partir da pesos atômicos de cada elemento . O peso atómico leva em conta a distribuição isotópica do elemento numa dada amostra (normalmente assumido como sendo "normal"). Por exemplo, a água tem uma massa molar de 18,0153 (3) g / mol, mas as moléculas de água individuais têm massas moleculares que variam entre 18,010 564 6863 (15) L (1 H 2 O) e 16 22,027 7,364 (9) u (2 18 H 2 O).
A distinção entre a massa molar e massa molecular é importante, porque as massas moleculares relativas podem ser medidos directamente por espectrometria de massa , muitas vezes com uma precisão de poucos partes por milhão. Isto é suficientemente precisa para determinar directamente a fórmula química de uma molécula.
Precisão e incertezas
A precisão com a qual uma massa molar é conhecido depende da precisão do massas atómicas a partir da qual foi calculada. A maioria dos pesos atômicos são conhecidos com uma precisão de, pelo menos, uma parte em dez mil, muitas vezes muito melhor (o peso atômico do lítio é um notável, e sério, exceção). Isto é adequado para quase todos os usos normais em química: é mais preciso do que a maioria análises químicas , e excede a pureza da maioria dos reagentes de laboratório.
A precisão do atomicismo pesos, e, consequentemente, de massas molares, é limitado pelo conhecimento da distribuição isotópica do elemento. Se é necessário um valor mais preciso da massa molar, que é necessário para determinar a distribuição isotópica da amostra em questão, que pode ser diferente do padrão de distribuição utilizado para calcular o peso atómico padrão. As distribuições isotópicas dos diferentes elementos de uma amostra não são necessariamente independentes um do outro: por exemplo, uma amostra que tenha sido destilada será enriquecido no acendedor isótopos de todos os elementos presentes. Isto complica o cálculo do incerteza padrão na massa molar.
Uma convenção útil para o trabalho de laboratório normal é de citar massas molares para dois casas decimais para todos os cálculos. Este é mais preciso do que é geralmente necessária, mas evita arredondamento erros durante os cálculos. Quando a massa molecular é superior a 1000 g / mol, que é raramente adequado utilizar mais do que uma casa decimal. Estas convenções são seguidas em valores mais tabulados de massas molares.
Medição
Enquanto massas molares são quase sempre, na prática, calculado a partir dos pesos atómicos, eles podem também ser medido em certos casos. Tais medições são muito menos precisos do que modernas de espectrometria de massa medições de pesos atômicos e massas moleculares, e são de interesse principalmente histórico. Todos os procedimentos dependem propriedades coligativas, e qualquer dissociação do composto devem ser tidas em conta.
Densidade do vapor
A medição da massa molar por densidade de vapor invoca o princípio, enunciado pela primeira Amadeo Avogadro, que volumes iguais de gases em condições idênticas contêm números iguais de partículas. Este princípio encontra-se incluído no equação do gás ideal:
onde n é o quantidade de substância. A densidade de vapor (ρ) é dada por
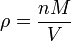 .
.
Combinando estas duas equações dá uma expressão para a massa molar em termos de densidade de vapor para as condições de conhecida pressão e temperatura .
Abaixamento do ponto de fusão
O ponto de congelação de uma solução é menor do que a do puro solvente , e a depressão do ponto de congelação (Δ t) é directamente proporcional à a concentração da quantidade para soluções diluídas. Quando a concentração de quantidade é expressa como um molalidade, a constante de proporcionalidade é conhecido como o crioscópicos constante (K F) e é característica para cada solvente. Se W representa o fracção de massa do soluto na solução, e assumindo que não há dissociação do soluto, a massa molar é dada pela
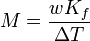 .
.
Elevação do ponto de ebulição
O ponto de ebulição de uma solução de um não volátil soluto é maior do que a do puro solvente , e a elevação do ponto de ebulição (Δ t) é directamente proporcional à a concentração da quantidade para soluções diluídas. Quando a concentração de quantidade é expressa como um molalidade, a constante de proporcionalidade é conhecido como o ebulioscópica constante (K b) e é característica para cada solvente. Se W representa o fracção de massa do soluto na solução, e assumindo que não há dissociação do soluto, a massa molar é dada pela
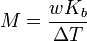 .
.