
Fixation de l'azote
Renseignements généraux
Arrangeant une sélection Wikipedia pour les écoles dans le monde en développement sans internet était une initiative de SOS Enfants. Pour comparer les organismes de bienfaisance de parrainage ce est le meilleur lien de parrainage .
Fixation de l'azote est le processus par lequel de l'azote est extrait de sa forme moléculaire naturel, relativement inerte (N 2) dans l' atmosphère et converti en composés azotés (tels que l'ammoniac , le nitrate et dioxyde d'azote).
Fixation de l'azote est effectuée naturellement par un certain nombre de différents procaryotes, y compris les bactéries , Actinobacteria, et certains types de les bactéries anaérobies. Les micro-organismes qui fixent l'azote sont appelés diazotrophes. Certaines plantes supérieures, et certains animaux ( termites ), ont formé des associations avec diazotrophes.
Fixation de l'azote se produit également en raison de procédés non biologiques. Il se agit notamment la foudre, industriellement par la Procédé Haber-Bosch, et la combustion.
La fixation biologique de l'azote a été découvert par le microbiologiste néerlandais Martinus Beijerinck.
La fixation biologique de l'azote

Fixation de l'azote (BNF) se produit lorsque l'azote atmosphérique est converti en ammoniac par une paire d'enzymes bactériennes appelée nitrogénase. La formule pour BNF est:
- N 2 + 8H + + 8e - + 16 ATP → 2NH 3 + H 2 + 16 ADP + 16 P i
Bien que l'ammoniac (NH 3) est le produit direct de cette réaction, il est rapidement protoné en ammonium (NH 4 +). Dans diazotrophes vivant en liberté, l'ammonium nitrogénasique généré est assimilé dans glutamate à travers la voie de la glutamine synthetase synthase / glutamate.
Dans la plupart des bactéries, des enzymes de nitrogénase sont très sensibles à la destruction par l'oxygène (et de nombreuses bactéries cesser la production de l'enzyme en présence d'oxygène). Faible tension en oxygène est obtenue par des bactéries différentes par: vivant dans des conditions anaérobies, respirant à puiser dans les niveaux d'oxygène, ou la liaison de l'oxygène avec une protéine telle que Leghémoglobine - également orthographié leghémoglobine ..
Les plantes les plus connus qui contribuent à la fixation de l'azote dans la nature, sont sous la famille des légumineuses - Fabaceae, qui comprend tels taxons trèfle, la luzerne, les haricots, les lupins et les arachides. Ils contiennent bactéries symbiotiques appelées rhizobiums sein nodules dans leur systèmes racinaires, produisant des composés azotés qui aident la plante à croître et rivaliser avec d'autres plantes. Lorsque la plante meurt, l'azote fixé est libéré, le rendant disponible à d'autres plantes et cela contribue à fertiliser le sol La grande majorité des légumineuses ont cette association, mais quelques genres (par exemple, Styphnolobium) ne le font pas. Dans de nombreuses pratiques traditionnelles et organiques agricoles, les champs sont tournées à travers différents types de cultures, qui comprend habituellement un composé principalement ou entièrement du trèfle ou de sarrasin (famille Polygonaceae), qui ont été souvent désigné comme «engrais vert», puisque l'autre façon naturelle de l'ajout de l'azote au sol est par l'intermédiaire des produits de déchets animaux. La plante entière est souvent réinvesti dans le domaine, donc non seulement ajouter plus d'azote, mais aussi améliorer le contenu et le volume organique du sol.
Plantes fixatrices d'azote non-légumineuses


Bien que la grande majorité des plantes fixatrices d'azote sont dans la famille des légumineuses Fabaceae, il ya quelques plantes non légumineuses qui peut également fixer l'azote. Ces plantes, dénommées plantes actinorhiziennes, se composent de 22 genres d'arbustes ligneuses ou des arbres dispersés dans huit familles de plantes. La capacité de fixer l'azote ne est pas universellement présente dans ces familles. Par exemple, de 122 genres dans le Rosaceae, seulement quatre genres sont capables de fixer l'azote.
Famille: Genera
Betulaceae (Birch): Alnus (Aulne)
Cannabaceae: Trema
Casuarinaceae (elle-chênes):
- Allocasuarina
- Casuarina
- Gymnostoma
Coriariaceae: Coriaria
Datiscaceae: Datisca
Elaeagnaceae (oleaster):
- Elaeagnus (silverberry)
- Hippophae (argousier)
- Shepherdia (shépherdie)
Myricaceae:
- Morella arborea
- Myrica
- Comptonia
Rhamnaceae (argousier):
- Ceanothus
- Colletia
- Discaria
- Kentrothamnus
- Retanilla
- Trevoa
Rosaceae (rose):
- Cercocarpus (acajou de montagne)
- Chamaebatia (de la misère de la montagne)
- Purshia (bitterbrush ou falaise rose)
- Dryas
Il ya aussi plusieurs associations symbiotiques fixatrices d'azote qui impliquent cyanobactéries (comme Nostoc). Il se agit notamment des lichens tels que Lobaria et Peltigera:
- Mosquito fougère ( espèces Azolla)
- Cycads
- Gunnera
Les micro-organismes qui fixent l'azote
- Diazotrophes
- Cyanobactéries
- Azotobacteraceae
- Rhizobiums
- Frankia
Fixation de l'azote par les cyanobactéries
Les cyanobactéries habitent presque tous les environnements éclairés sur la Terre et jouent un rôle clé dans le carbone et le cycle de l'azote de la biosphère . Généralement, cyanobactéries sont capables d'utiliser une variété de sources inorganiques et organiques d'azote combiné, comme le nitrate , nitrite, ammonium, l'urée ou des acides aminés . Plusieurs souches de cyanobactéries sont également capables de diazotrophes croissance. Le séquençage du génome a fourni une grande quantité d'informations sur la base génétique du métabolisme de l'azote et de son contrôle dans les cyanobactéries différente. La génomique comparative, ainsi que des études fonctionnelles, a conduit à une avancée significative dans ce domaine au cours des dernières années. 2-oxoglutarate se est avéré être la molécule de signalisation central reflétant l'équilibre carbone / azote de cyanobactéries. Acteurs centraux de contrôle d'azote sont le facteur de transcription NtcA mondiale, qui contrôle l'expression de nombreux gènes impliqués dans le métabolisme de l'azote, ainsi que la protéine de signalisation P II, quelles activités peaufine cellulaire en réponse à l'évolution des conditions C / N. Ces deux protéines sont des capteurs de niveau 2-oxoglutarate cellulaire et ont été conservés dans tous les cyanobactéries. En revanche, l'adaptation à la privation d'azote implique réponses hétérogènes dans les différentes souches.
Fixation de l'azote chimique
L'azote peut également être fixé artificiellement pour une utilisation dans les engrais , les explosifs, ou dans d'autres produits. La méthode la plus populaire est par le Procédé Haber. Cette production d'engrais chimiques a atteint une telle ampleur qu'il est maintenant la plus grande source d'azote fixé dans la terre de l ' écosystème.
Le procédé Haber nécessite des pressions élevées et des températures très élevées et de la recherche active est engagée dans le développement de systèmes de catalyseurs qui transforment l'azote en ammoniac à des températures ambiantes. De nombreux composés peuvent réagir avec de l'azote atmosphérique dans des conditions ambiantes (par exemple le lithium fait nitrure de lithium se il est laissé exposé), mais les produits de ces réactions ne sont pas facilement convertis en sources d'azote biologiquement accessibles. Après la première diazote complexe a été découvert en 1965 sur la base de l'ammoniac coordonnée de ruthénium ([Ru (NH 3) 5 (N 2)] 2+), la recherche dans la fixation chimique concentré sur des complexes de métaux de transition. Depuis ce temps, un grand nombre de composés de métaux de transition qui contiennent en tant que ligand diazote ont été découverts. Le ligand de diazote peut être lié soit à une seule deux (ou plusieurs) des métaux métallique ou d'un pont. La chimie de coordination de diazote est riche et l'étude intense. Cette recherche pourrait mener à de nouvelles façons d'utiliser diazote dans la synthèse et à l'échelle industrielle.
Le premier exemple de clivage homolytique de diazote dans des conditions douces a été publié en 1995. Deux équivalents d'une molybdène complexe mis à réagir avec un équivalent de diazote, créant un triple complexe MoN collé. Depuis ce complexe délimitée triple a été utilisé pour faire nitriles. Le premier système catalytique de conversion de l'azote de l'ammoniac à la température ambiante et 1 atmosphère a été découvert en 2003 et est basé sur un autre composé de molybdène, une source de protons et un fort agent réducteur. Malheureusement, la réduction catalytique ne subit quelques revirements avant le décès de catalyseur.
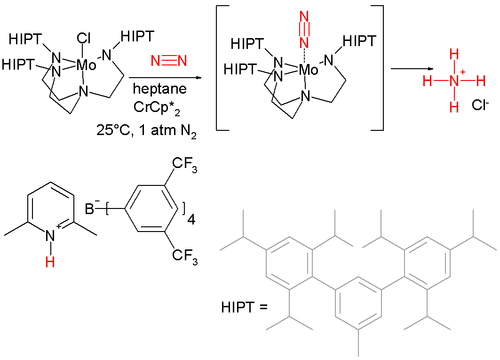
Contrairement au graphique illustré ci-dessus, le principal produit de cette réaction est de l'ammoniac (NH3) et non un sel d'ammonium ([NH4] [X]). En fait, environ 75% de l'ammoniac produit peut être éliminé par distillation à partir de la cuve de réaction (ce qui suggère l'ammoniac ne est pas protonée) dans un récipient contenant du HCl en tant que piège. Cette méthode de piégeage est sans doute le NH3 choisi parce qu'il rend le produit plus facile à manipuler. Notez également que parce que seulement 1 équivalent de l'anion Cl est disponible dans des conditions catalytiques (par réduction du chlorure de molbdenum précatalyseur, représentée) par conséquent, il est peu probable que le sel d'ammonium produit aurait toujours cette contre-ion.
Notez également que même si le complexe de diazote est indiqué entre parenthèses cette espèce peuvent être isolés et caractérisés. Ici, les crochets ne indiquent pas que l'intermédiaire ne est pas observée.

