
appauvrissement de l'ozone
Saviez-vous ...
Cette sélection se fait pour les écoles par la charité pour enfants lire la suite . SOS Enfants a regardé des enfants en Afrique depuis quarante ans. Pouvez-vous aider dans leur travail en Afrique ?
| |||||||||||||||||||||||
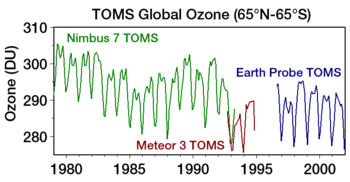
appauvrissement de l'ozone décrit deux observations distinctes, mais liées: une lente, déclin constant d'environ 4 pour cent par décennie dans le montant total de l'ozone dans la Terre stratosphère depuis la fin des années 1970; et un beaucoup plus grand, mais de saison, diminution de l'ozone stratosphérique au-dessus des régions polaires de la Terre au cours de la même période. Ce dernier phénomène est couramment désigné sous le trou d'ozone. En plus de cette diminution de l'ozone stratosphérique bien connu, il ya aussi événements appauvrissement de l'ozone troposphérique, qui se produisent près de la surface dans les régions polaires au cours du printemps.
Le mécanisme détaillé par lequel la polaire sous forme de trous d'ozone est différent de celui de l'amincissement des latitudes moyennes, mais le processus le plus important dans les deux tendances est catalytique destruction de l'ozone par le chlore et le brome atomique. La principale source de ces halogènes atomes dans la stratosphère est photodissociation de chlorofluorocarbones (CFC) composés, communément appelés fréons, et bromofluorocarbure composés connue sous le nom halons. Ces composés sont transportés dans la stratosphère après avoir été émise à la surface. Les deux mécanismes d'appauvrissement de l'ozone renforcées que les émissions de CFC et de halons ont augmenté.
CFC et d'autres substances contributives sont communément appelés substances appauvrissant l'ozone (SAO). Depuis la couche d'ozone empêche longueurs d'onde UVB plus nocifs (270-315 nm) de la lumière ultraviolette (lumière UV) de passer à travers l' atmosphère de la Terre , les baisses observées et projetées de l'ozone ont suscité des préoccupations dans le monde entier conduisant à l'adoption de la Protocole de Montréal interdisant la production de CFC et de halons ainsi que de produits chimiques appauvrissant l'ozone connexes tels que le tétrachlorure de carbone et trichloroéthane. On soupçonne que une variété de conséquences biologiques tels que l'augmentation cancer de la peau, des dommages aux plantes, et la réduction du populations de plancton dans l'océan de zone photique peut résulter de l'exposition aux UV augmenté en raison de la couche d'ozone.
aperçu du cycle de l'ozone
Trois formes (ou allotropes ) d'oxygène sont impliqués dans le Cycle ozone-oxygène: oxygène . atomes (O ou d'oxygène atomique), de gaz d'oxygène (O 2 ou de l'oxygène diatomique), et le gaz d'ozone (O 3 ou de l'oxygène triatomique) L'ozone est formé dans la stratosphère où les molécules d'oxygène photodissociate après absorption d'un rayonnement ultraviolet dont la longueur d'onde des photons est inférieure à 240 nm. Ceci produit deux atomes d'oxygène. L'oxygène atomique se combine ensuite avec O 2 pour créer O 3. Les molécules d'ozone absorbent la lumière ultraviolette entre 310 et 200 nm, après quoi l'ozone se décompose en une molécule de O 2 et un atome d'oxygène. L'atome d'oxygène rejoint ensuite avec une molécule d'oxygène pour régénérer l'ozone. Ce est un processus continu qui se termine quand un atome d'oxygène "se recombine" avec une molécule d'ozone pour faire deux molécules de O 2 O 3 + O 2 O 2 →
Le montant global de l'ozone dans la stratosphère est déterminée par un équilibre entre la production photochimique et la recombinaison.
L'ozone peut être détruit par un certain nombre de catalyseurs de radicaux libres, les plus importants sont la radical hydroxyle (OH ·), le oxyde nitrique radicale (NO ·) et atomique de chlore (Cl ·) et le brome (Br ·). Tous ces éléments ont deux (d'origine humaine) sources naturelles et anthropiques; à l'heure actuelle, la plupart des OH et NO · · dans la stratosphère est d'origine naturelle, mais l'activité humaine a considérablement augmenté le haut dans le chlore et le brome d'oxygène. Ces éléments se trouvent dans certains composés organiques stables, en particulier chlorofluorocarbones (CFC), qui peuvent trouver leur chemin vers le stratosphère sans être détruit dans la troposphère en raison de leur faible réactivité. Une fois dans la stratosphère, les atomes de Cl et Br sont libérés à partir des composés de base par l'action de la lumière ultraviolette, par exemple ('h' est Constant, 'ν' de Planck est fréquence de rayonnement électromagnétique )
CFCI3 + hv → CFCl 2 + Cl
Les atomes Cl et Br peuvent ensuite détruire les molécules d'ozone à travers une variété de catalytiques cycles. Dans l'exemple le plus simple d'un tel cycle, un atome de chlore réagit avec une molécule d'ozone, en un atome d'oxygène avec elle (ClO formation) et laissant une molécule d'oxygène normale. Un atome d'oxygène libre prend alors une distance l'oxygène de l'ClO, et le résultat final est une molécule d'oxygène et un atome de chlore, qui réinitialise ensuite le cycle. L'abréviation chimique de ces réactions en phase gazeuse est la suivante:
Cl + O 3 → ClO + O 2
ClO + O → Cl + O 2
La réaction nette est: O O 3 + O 2 → 2, la réaction de "recombinaison" donnée ci-dessus.
L'effet global est d'augmenter le taux de recombinaison, conduisant à une diminution globale de la quantité d'ozone. Pour que ce mécanisme particulier de fonctionnement il doit y avoir une source d'atomes de O, qui est principalement de la photo dissociation O 3; donc ce mécanisme ne est important que dans la haute stratosphère où ces atomes sont abondants. Des mécanismes plus complexes ont été découverts qui conduisent à la destruction de l'ozone dans la basse stratosphère ainsi.
Un seul atome de chlore serait continuer à détruire l'ozone jusqu'à deux ans (l'échelle de temps pour le transport vers le bas à la troposphère) si ce ne était pour les réactions qui les éliminent de ce cycle en formant des espèces réservoirs tels que du chlorure d'hydrogène (HCl) et nitrate de chlore (ClONO 2). Sur une base par atome, le brome est encore plus efficace que le chlore pour détruire l'ozone, mais il ya beaucoup moins de brome dans l'atmosphère à l'heure actuelle. En conséquence, à la fois du chlore et du brome contribuent de manière significative à la diminution globale d'ozone. Des études en laboratoire ont montré que les atomes de fluor et d'iode participent à cycles catalytiques analogues. Cependant, dans la stratosphère de la terre, des atomes de fluor réagissent rapidement avec l'eau et le méthane pour former fortement lié HF, tandis que les molécules organiques qui contiennent de l'iode réagissent si rapidement dans la basse atmosphère qu'ils ne atteignent pas la stratosphère en quantités importantes. En outre, un seul atome de chlore peut réagir avec 100 000 molécules d'ozone. Ce fait, plus la quantité de chlore libéré dans l'atmosphère par les chlorofluorocarbures (CFC) démontre chaque année combien dangereux CFC sont à l'environnement.
Compréhension quantitative du processus de perte d'ozone chimique
De nouvelles recherches sur la répartition d'une molécule clé dans ces produits chimiques appauvrissant l'ozone, le peroxyde dichlorine (Cl2O2), remet en question l'exhaustivité des présentes modèles atmosphériques de la couche d'ozone polaire. Plus précisément, les chimistes du Jet Propulsion Laboratory de la NASA à Pasadena, en Californie, a constaté en 2007 que les températures, et le spectre et l'intensité de rayonnement présente dans la stratosphère ont créé des conditions suffisantes pour permettre au taux de produits chimiques ventilation requis pour libérer des radicaux de chlore dans le volume nécessaire pour expliquer les taux observés de la couche d'ozone. Au lieu de cela, des tests de laboratoire, visant à être le reflet plus précis des conditions stratosphériques à ce jour, ont montré la dégradation de la molécule cruciale presque une grandeur plus faible que le pensait auparavant.
Observations sur la couche d'ozone
La diminution la plus marquée de l'ozone a été dans le bas stratosphère. Toutefois, le trou d'ozone est le plus souvent mesurée non pas en termes de concentrations d'ozone à ces niveaux (qui sont typiquement de quelques parties par million), mais par la réduction de la colonne d'ozone totale, au-dessus d'un point sur la surface de la Terre, qui est normalement exprimé en Unités Dobson, en abrégé "Du". Diminutions marquées dans la colonne d'ozone dans la Printemps antarctique et début de l'été par rapport à début des années 1970 et avant ont été observées en utilisant des instruments tels que le Total spectromètre imageur de l'ozone (TOMS).
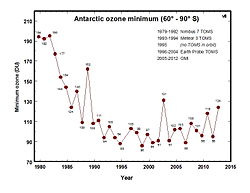
Des réductions allant jusqu'à 70% dans la colonne d'ozone observée dans le austral (hémisphère sud) ressort sur l'Antarctique et rapportées en 1985 (Farman et al 1985) se poursuivent. Dans les années 1990, l'ozone total de la colonne en Septembre et Octobre ont continué à 40-50% de moins que les valeurs du trou d'ozone pré-. Dans l' Arctique, la quantité perdue est l'année pour l'exercice à plus variable que dans l'Antarctique. Les plus fortes baisses, jusqu'à 30%, sont en hiver et au printemps, lorsque la stratosphère est plus froid.
Réactions qui ont lieu sur les nuages stratosphériques polaires (PSC) jouent un rôle important dans le renforcement de la couche d'ozone. PSC forment plus facilement dans le froid extrême de stratosphère antarctique. Ce est pourquoi les trous d'ozone d'abord formés, et sont plus profondes, dessus de l'Antarctique. Les premiers modèles ont omis de prendre en compte les CSP et a prédit une diminution globale progressive, ce est pourquoi le trou d'ozone antarctique soudaine était une surprise pour beaucoup de scientifiques.
Dans les latitudes moyennes, il est préférable de parler de la couche d'ozone plutôt que des trous. Les baisses sont environ 3% en dessous des valeurs pré-1980 pour 35-60 ° N et environ 6% pour les 35-60 ° S. Dans les tropiques, il n'y a pas de tendances significatives.
appauvrissement de l'ozone explique aussi beaucoup de la réduction observée stratosphérique et supérieure températures de la troposphère. La source de la chaleur de la stratosphère est l'absorption du rayonnement UV par l'ozone, l'ozone réduit donc conduit à un refroidissement. Certains refroidissement de la stratosphère est également prédit des augmentations de gaz à effet de serre tels que le CO 2 ; Cependant le refroidissement induite ozone semble être dominante.
Les prévisions de niveaux d'ozone restent difficiles. Le Projet de recherche et de surveillance de l'ozone mondial Organisation météorologique mondiale - Rapport n ° 44 vient fermement en faveur du Protocole de Montréal, mais note qu'un PNUE évaluation 1994 surestimé la perte d'ozone pour la période 1994-1997.
Les produits chimiques dans l'atmosphère
CFC dans l'atmosphère
Chlorofluorocarbures ( CFC) ont été inventé par Thomas Midgley dans les années 1920. Ils ont été utilisés dans les unités de climatisation / refroidissement, comme propulseurs aérosol avant les années 1980, et dans les processus de nettoyage de l'équipement électronique délicate. Ils produisent également des sous-produits de certains procédés chimiques. Aucun sources naturelles importantes ont déjà été identifiés pour ces composés - leur présence dans l'atmosphère est presque entièrement attribuable à la fabrication humaine. Comme mentionné dans la liste de cycle de l'ozone au-dessus, lorsque ces produits chimiques destructeurs d'ozone atteignent la stratosphère, ils sont dissociés par la lumière ultraviolette pour libérer des atomes de chlore. Les atomes de chlore agissent comme un catalyseur , et chacun peut briser des dizaines de milliers de molécules d'ozone avant de disparaître de la stratosphère. Compte tenu de la longévité des molécules de CFC, les temps de récupération sont mesurées en décennies. Il est calculé qu'une molécule de CFC prend une moyenne de 15 ans pour passer du niveau sol jusqu'à la haute atmosphère, et il peut y rester pendant environ un siècle, détruisant jusqu'à une centaine de milliers de molécules d'ozone pendant ce temps.
Vérification des observations
Les scientifiques ont été de plus en plus en mesure d'attribuer l'appauvrissement de l'ozone observé à l'augmentation des anthropiques halogènes composés des CFC par l'utilisation de modèles de transport de chimie complexes et leur validation par rapport à des données d'observation (par exemple, SLIMCAT, Palourdes). Ces modèles fonctionnent en combinant mesures par satellite des concentrations chimiques et les champs météorologiques avec les constantes de vitesse de réaction chimique obtenus dans des expériences de laboratoire. Ils sont capables d'identifier non seulement les réactions chimiques clés, mais aussi les processus de transport qui apportent CFC produits de la photolyse en contact avec de l'ozone.
Le trou d'ozone et de ses causes
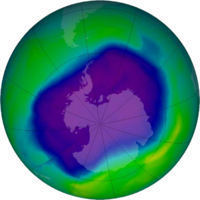
Le trou d'ozone antarctique est une zone de la stratosphère antarctique où les niveaux d'ozone dernières ont chuté aussi bas que 33% de leurs valeurs pré-1975. Le trou d'ozone se produit au cours du printemps de l'Antarctique, de Septembre à Décembre début, comme forts vents d'ouest commencent à circuler autour du continent et de créer un récipient atmosphérique. Dans ce vortex polaire, plus de 50% de l'ozone stratosphérique inférieure est détruite au cours du printemps de l'Antarctique.
Comme expliqué ci-dessus, la cause globale de la couche d'ozone est la présence de gaz contenant du chlore sources (principalement les CFC et les halocarbures connexes). En présence de lumière UV, ces gaz se dissocient, libérant des atomes de chlore, qui vont ensuite pour catalyser la destruction de l'ozone. L'appauvrissement de l'ozone catalysée par Cl peut avoir lieu dans la phase gazeuse, mais il est considérablement améliorée en présence de nuages stratosphériques polaires (PSC).
Ces nuages stratosphériques polaires forment pendant l'hiver, dans le froid extrême. Hivers polaires sont sombres, composée de 3 mois sans rayonnement solaire (lumière du soleil). Non seulement manque de lumière contribue à une diminution de la température mais aussi la pièges à vortex polaires et des frissons air. Températures tournent autour ou en dessous de -80 ° C. Ces basses températures forment des particules de nuages et sont composés soit de l'acide nitrique (Type I CFP) ou de la glace (Type II CFP). Les deux types fournissent des surfaces pour des réactions chimiques qui conduisent à la destruction de l'ozone.
Le processus photochimiques impliqués sont complexes, mais bien compris. L'observation clé est que, généralement, la plupart du chlore dans la stratosphère réside dans «réservoir» des composés stables, principalement du chlorure d'hydrogène (HCl) et du nitrate de chlore (ClONO 2). Au cours de l'hiver antarctique et au printemps, cependant, les réactions à la surface des particules de nuages stratosphériques polaires convertir ces composés "réservoir" en radicaux libres réactifs (Cl et CLO). Les nuages peuvent également supprimer NO 2 dans l'atmosphère en le convertissant en acide nitrique, ce qui empêche le ClO nouvellement formé d'être reconverti en ClONO 2.
Le rôle de la lumière du soleil dans la couche d'ozone est la raison pour laquelle l'appauvrissement de l'ozone de l'Antarctique est plus grand au printemps. Pendant l'hiver, même si les PSC sont à leur plus abondant, il n'y a pas de lumière sur le pôle de conduire les réactions chimiques. Au cours du printemps, cependant, le soleil sort, fournissant de l'énergie à conduire des réactions photochimiques, et faire fondre les nuages stratosphériques polaires, la libération des composés piégés.
La plupart de l'ozone qui est détruit dans la stratosphère est inférieure, à la différence de l'appauvrissement de l'ozone beaucoup plus petites par des réactions en phase gazeuse homogène, ce qui se produit principalement dans la stratosphère supérieure.
Le réchauffement des températures près de la fin du printemps briser le vortex vers la mi-Décembre. Comme l'air chaud, riche en ozone se écoule dans des latitudes plus basses, les CSP sont détruits, le processus de destruction de l'ozone se arrête, et les guérit de trou d'ozone.
L'intérêt pour la couche d'ozone
Bien que l'effet du trou d'ozone antarctique dans la diminution de la couche d'ozone global est relativement faible, estimé à environ 4% par décennie, le trou a suscité beaucoup d'intérêt parce que:
- La diminution de la couche d'ozone a été prédite dans les années 1980 à à peu près 7% sur une période de soixante ans.
- La reconnaissance soudaine en 1985 qu'il y avait un "trou" substantielle a été largement rapporté dans la presse. L'appauvrissement de l'ozone particulièrement rapide dans l'Antarctique avait déjà été rejetée comme une erreur de mesure.
- Beaucoup étaient inquiets que les trous d'ozone pourraient commencer à apparaître sur les autres régions du globe, mais à ce jour le seul autre appauvrissement grande échelle est un ozone "fossette" faible observé au cours du printemps de l'Arctique sur le pôle Nord. Ozone aux latitudes moyennes a diminué, mais dans une bien moindre mesure (environ 4-5% de baisse).
- Si les conditions sont devenues plus sévères (températures stratosphériques plus fraîches, des nuages stratosphériques plus, chlore plus actif), puis l'ozone globale peut diminuer à un rythme beaucoup plus. Norme réchauffement climatique théorie prédit que la stratosphère se refroidira.
- Lorsque le trou d'ozone antarctique se brise, l'air appauvri en ozone dérive sortir dans les zones avoisinantes. La diminution du niveau de jusqu'à 10% de l'ozone ont été signalés en Nouvelle-Zélande dans le mois suivant la rupture du trou d'ozone antarctique.
Conséquences de la couche d'ozone
Depuis la couche d'ozone absorbe les UVB de la lumière ultraviolette du Soleil, est prévu la couche d'ozone pour augmenter les niveaux d'UVB de surface, ce qui pourrait causer des dommages, y compris l'augmentation des cancer de la peau. Ce est la raison pour le Protocole de Montréal. Bien que des diminutions de l'ozone stratosphérique sont bien liés à CFC et il ya de bonnes raisons théoriques de croire qu'une diminution de l'ozone va entraîner une augmentation des UVB de surface, il ne existe aucune preuve observation directe reliant la couche d'ozone à l'incidence plus élevée de cancer de la peau des êtres humains. Ceci est partiellement dû au fait que UVA, qui a également été impliquée dans certaines formes de cancer de la peau, ne est pas absorbée par l'ozone, et il est presque impossible de contrôler les statistiques pour les changements de mode de vie à la population.
UV accrue
L'ozone, tandis qu'un constituant minoritaire dans l'atmosphère de la terre, est responsable de la plupart de l'absorption du rayonnement UVB. La quantité de rayonnement UVB qui pénètre à travers la couche d'ozone diminue de façon exponentielle avec le chemin oblique épaisseur / densité de la couche. De manière correspondante, une diminution de l'ozone atmosphérique devrait donner lieu à une augmentation significative des niveaux d'UVB proches de la surface.
Les augmentations de surface UVB en raison de la trou d'ozone peuvent être partiellement déduites par calculs de modèle de transfert radiatif, mais ne peuvent pas être calculées à partir de mesures directes en raison de l'absence de données (trou d'ozone pré-) surface UV fiables historiques, bien que les programmes plus de surface récente de mesure d'observation UV existent (par exemple à Lauder, Nouvelle-Zélande ).
Parce que ce est ce même rayonnement UV qui crée l'ozone dans la couche d'ozone à partir de O 2 (oxygène ordinaire) en premier lieu, une diminution de l'ozone stratosphérique serait effectivement tendance à augmenter la production photochimique de l'ozone à des niveaux inférieurs (dans le troposphère), bien que les tendances observées ensemble dans la colonne d'ozone totale montrent encore une baisse, en grande partie parce que l'ozone produit plus bas a une durée de vie photochimique naturellement plus courte, de sorte qu'il est détruit avant que les concentrations pourraient atteindre un niveau qui compenserait pour la réduction de l'ozone plus haut .
Les effets biologiques des rayonnements UV et une augmentation de micro-ondes à partir d'une couche d'ozone appauvri
La principale préoccupation du public concernant le trou d'ozone a été les effets des UV de surface sur la santé humaine. Jusqu'à présent, la couche d'ozone dans la plupart des endroits a été généralement quelques pour cent et, comme indiqué ci-dessus, aucune preuve directe de dommages pour la santé est disponible dans la plupart des latitudes. Ont été les niveaux élevés d'épuisement vu dans le trou d'ozone jamais être communs à travers le monde, les effets pourraient être beaucoup plus dramatique. Comme le trou d'ozone sur l'Antarctique a, dans certains cas pris tellement d'envergure pour atteindre les régions méridionales de l'Australie et de la Nouvelle-Zélande , les écologistes ont été concerné que l'augmentation des UV de surface pourrait être significatif.
Effets de la couche d'ozone sur les humains
UVB (le rayonnement UV énergétique supérieur absorbée par l'ozone) est généralement considéré comme un facteur contributif à cancer de la peau. En outre, l'accroissement des UV de surface entraîne une augmentation de l'ozone troposphérique, qui est un risque pour la santé humaine. L'augmentation des UV de surface représente également une augmentation de la vitamine D synthétique de la capacité de la lumière du soleil.
Les effets préventifs du cancer de la vitamine D représentent un possible effet bénéfique de la couche d'ozone. En termes de coûts de santé, les avantages possibles d'augmentation du rayonnement UV peuvent l'emporter sur le fardeau.
1. carcinomes basocellulaire et squameux carcinomes - Les formes les plus courantes de cancer de la peau chez l'homme, basal et les carcinomes épidermoïdes, ont été fortement liée à l'exposition aux UVB. Le mécanisme par lequel ces cancers UVB induit est bien entendu - absorption de rayons UVB provoque les bases de pyrimidine dans la molécule d'ADN pour former dimères, qui entraîne des erreurs de transcription lorsque l'ADN se réplique. Ces cancers sont relativement doux et rarement fatale, bien que le traitement du carcinome à cellules squameuses nécessite parfois très étendue chirurgie reconstructive. En combinant les données épidémiologiques avec les résultats des études sur les animaux, les scientifiques ont estimé qu'une baisse de un pour cent de l'ozone stratosphérique augmenterait l'incidence de ces cancers de 2%.
2. mélanome malin - Une autre forme de cancer de la peau, le mélanome malin, est beaucoup moins commun, mais beaucoup plus dangereux, étant mortelle dans environ 15% - 20% des cas diagnostiqués. La relation entre le mélanome malin et l'exposition aux ultraviolets ne est pas encore bien compris, mais il semble que les rayons UVB et UVA sont impliqués. Les expériences sur les poissons suggèrent que 90 à 95% des mélanomes malins peut être dû aux UVA et visible que les expérimentations menées sur les opossums suggèrent un rôle plus important pour les UVB. En raison de cette incertitude, il est difficile d'estimer l'impact de la raréfaction de l'ozone sur l'incidence du mélanome. Une étude a montré qu'une augmentation de 10% des rayons UVB a été associée à une augmentation de 19% des mélanomes chez les hommes et 16% pour les femmes. Une étude des personnes dans Punta Arenas, à l'extrémité sud du Chili , a montré une augmentation de 56% dans le mélanome et d'une augmentation de 46% dans le cancer non mélanique de la peau sur une période de sept ans, avec une baisse des niveaux de l'ozone et l'augmentation des UVB.
3. cataractes corticales - Des études sont évocateurs d'une association entre corticales oculaires cataractes et exposition aux UV-B, en utilisant des approximations grossières de l'exposition et les diverses techniques d'évaluation de la cataracte. Une évaluation détaillée de l'exposition oculaire aux UV-B a été réalisée dans une étude sur la baie de Chesapeake Watermen, où les augmentations dans l'exposition oculaire moyenne annuelle ont été associés à une augmentation du risque d'opacité corticale. Dans ce groupe très exposé des hommes à prédominance blanche, la preuve reliant opacités corticales à l'exposition au soleil est la plus forte à ce jour. Toutefois, les données suivantes d'une étude basée sur une population à Beaver Dam, WI suggéré le risque peut être limité aux hommes. Dans l'étude Beaver Dam, les expositions chez les femmes ont été plus faibles que les expositions chez les hommes, et aucune association n'a été observée. En outre, il n'y avait pas de données reliant l'exposition au soleil au risque de cataracte chez les Afro-Américains, bien que d'autres maladies oculaires ont des prévalences entre les différents groupes raciaux, et l'opacité corticale semble être plus élevée dans les Afro-Américains par rapport aux blancs.
4. Augmentation de l'ozone troposphérique - Augmentation UV de surface conduit à une augmentation ozone troposphérique. ozone troposphérique est généralement reconnu comme un risque pour la santé, que l'ozone est toxique en raison de sa forte propriétés oxydantes. A ce moment, l'ozone au niveau du sol est principalement produite par l'action du rayonnement UV sur gaz de combustion de gaz d'échappement des véhicules.
Effets sur les cultures
On se attendrait à une augmentation du rayonnement UV à affecter les cultures. Un certain nombre d'espèces économiquement importantes de plantes, telles que le riz , dépendra de cyanobactéries résidant sur leurs racines pour la rétention de l'azote . Les cyanobactéries sont sensibles à la lumière UV et qu'ils seraient affectés par l'augmentation.
Effets sur le plancton
La recherche a montré une extinction généralisée de plancton ya 2 millions d'années qui a coïncidé avec une proximité supernova . Il ya une différence dans l'orientation et la motilité des planctons quand l'excès de rayons UV atteignent la Terre. Les chercheurs supposent que l'extinction a été causé par un affaiblissement significatif de la couche d'ozone à l'époque où le rayonnement de la supernova produit oxydes d'azote qui catalysées la destruction de l'ozone (plancton sont particulièrement sensibles aux effets de la lumière UV, et sont d'une importance vitale pour marine réseaux trophiques).
Les politiques publiques en réponse au trou d'ozone
L'ampleur des dégâts que les CFC ont causés à la couche d'ozone ne est pas connue et ne seront pas connus depuis des décennies; Cependant, des diminutions marquées dans la colonne d'ozone ont déjà été observés (comme expliqué ci-dessus).
Après un rapport de 1976 par le US National Academy of Sciences a conclu que la preuve scientifique crédible soutenu l'hypothèse la couche d'ozone, quelques pays, dont les États-Unis, le Canada, la Suède et la Norvège, se installe à éliminer l'utilisation des CFC dans les aérosols. Au moment où ce était largement considéré comme un premier pas vers une politique de régulation plus globale, mais les progrès dans ce sens a ralenti au cours des années suivantes, en raison d'une combinaison de facteurs politiques (résistance continue de l'industrie des halocarbures et un changement général d'attitude envers l'environnement la réglementation au cours des deux premières années de l'administration Reagan) et des développements scientifiques (évaluations ultérieures National Academy qui indiquaient que les premières estimations de l'ampleur de la couche d'ozone avaient été trop grande). La Communauté européenne a rejeté des propositions visant à interdire les CFC dans les bombes aérosols tandis que même aux États-Unis, les CFC ont continué à être utilisés comme réfrigérants et pour le nettoyage des cartes de circuits. La production mondiale de CFC a fortement chuté après l'interdiction d'aérosol-Unis, mais en 1986, était revenu près de son niveau de 1976. En 1980, DuPont a fermé son programme de recherche sur les halocarbures de remplacement.
L'attitude du gouvernement américain a commencé à changer à nouveau en 1983, lorsque William Ruckelshaus remplacé Anne M. Burford en tant qu'administrateur de la Environmental Protection Agency des États-Unis. Sous Ruckelshaus et son successeur, Thomas Lee, l'EPA a poussé pour une approche internationale pour les halocarbures. En 1985 20 nations, y compris la plupart des grands producteurs de CFC, signé la Convention de Vienne qui a établi un cadre pour la négociation des réglementations internationales sur les substances appauvrissant l'ozone. Cette même année, la découverte du trou d'ozone antarctique a été annoncé, provoquant un regain d'attention du public sur la question. En 1987, des représentants de 43 pays ont signé la Protocole de Montréal. Pendant ce temps, l'industrie des halocarbures déplacé sa position et a commencé à soutenir un protocole de limiter la production de CFC. Les raisons en étaient explique en partie par "Dr Mostafa Tolba, ancien chef du Programme des Nations Unies pour l'environnement, qui a été cité dans le 30 juin 1990 L'édition du New Scientist, «... l'industrie chimique a soutenu le Protocole de Montréal en 1987, car il a mis en place un programme mondial pour l'élimination des CFC, qui [ont été] ne est plus protégé par des brevets. Cela a fourni aux entreprises une chance égale de commercialiser de nouveaux composés, plus rentables. "
À Montréal, les participants ont convenu de geler la production de CFC au niveau de 1986 et de réduire la production de 50% en 1999. Après une série d'expéditions scientifiques en Antarctique produites des preuves convaincantes que le trou d'ozone a effectivement été causé par le chlore et le brome de organohalogènes artificielles , le Protocole de Montréal a été renforcée lors d'une réunion à Londres 1990. Les participants ont convenu d'éliminer les CFC et les halons entièrement (à part une très petite quantité marquée pour certains «essentiel» utilise, comme inhalateurs pour l'asthme) par 2000. Lors d'une réunion à Copenhague 1992, la phase la date de départ a été déplacé jusqu'en 1996.
Dans une certaine mesure, les CFC ont été remplacés par les hydro-chloro-fluoro-carbones (moins dommageables HCFC), mais des problèmes subsistent en ce qui concerne les HCFC également. Dans certaines applications, Hydro-fluoro-carbones ( HFC) ont été utilisés pour remplacer les CFC. HFC, qui ne contiennent pas de chlore ou de brome, ne contribuent pas du tout à la couche d'ozone mais ils sont de puissants gaz à effet de serre. La plus connue de ces composés est probablement HFC-134a ( R-134a), qui, dans les Etats-Unis a largement remplacé les CFC-12 ( R-12) dans les climatiseurs d'automobile. Dans l'analyse de laboratoire (un ancien de l'utilisation «essentielle») l'substances appauvrissant l'ozone peut être remplacé par d'autres solvants.
Diplomatie de l'ozone, par Richard Benedick (Harvard University Press, 1991) donne un compte rendu détaillé du processus de négociation qui a conduit au Protocole de Montréal. Pielke et Betsill fournissent un examen approfondi des premières réponses du gouvernement américain à la science émergente de la couche d'ozone par les CFC.
L'actualité et les perspectives d'avenir de la couche d'ozone
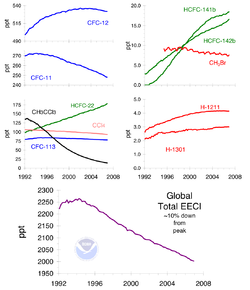
Depuis l'adoption et le renforcement du Protocole de Montréal a conduit à des réductions dans les émissions de CFC, les concentrations atmosphériques des composés les plus importants ont été en baisse. Ces substances sont progressivement éliminées de l'atmosphère. En 2015, le trou d'ozone antarctique aurait réduit de seulement 1 million de km² sur 25 (Newman et al., 2004); récupération complète de la couche d'ozone de l'Antarctique aura pas lieu avant l'année 2050 ou plus tard. Les travaux ont suggéré qu'une détectable (et statistiquement significative) la récupération ne se produira pas jusqu'à environ 2024, les niveaux d'ozone se remettent aux niveaux de 1980 d'environ 2068.
Il ya une légère mise en garde à cela, cependant. réchauffement de la planète à partir de CO 2 est prévu pour refroidir la stratosphère. Ceci, à son tour, entraînerait une augmentation relative de la couche d'ozone et la fréquence des trous d'ozone. L'effet peut ne pas être linéaire; trous d'ozone forment à cause des nuages stratosphériques polaires; la formation de nuages stratosphériques polaires a un seuil de température supérieure à laquelle ils ne feront pas; refroidissement de la stratosphère arctique pourrait conduire à des conditions Antarctique trou d'ozone semblable. Mais pour le moment ce ne est pas clair.
Même si la stratosphère dans son ensemble se refroidit, les zones de hautes latitudes peuvent devenir de plus en plus prédisposés à Springtime réchauffements stratosphériques que les conditions météorologiques changent en réponse à plus de gaz à effet de chargement. Cela risque de provoquer PSC à disparaître tôt dans la saison, et peut expliquer pourquoi l'Antarctique saisons de trou d'ozone ont tendance à terminer un peu plus tôt depuis 2000 par rapport aux trous d'ozone les plus prolongées des années 1990.
La diminution des produits chimiques appauvrissant l'ozone a également été significativement affectée par une diminution de brome contenant des produits chimiques. Les données suggèrent que les sources naturelles importantes existent pour atmosphérique le bromure de méthyle (CH 3 Br).
Le trou d'ozone 2004 a pris fin en Novembre 2004, les températures stratosphériques minimales quotidiennes dans l'Antarctique basse stratosphère a augmenté à des niveaux qui sont trop chaud pour la formation de nuages stratosphériques polaires (PSC) environ 2 à 3 semaines plus tôt que dans la plupart des dernières années.
L'hiver de l'Arctique de 2005 a été extrêmement froid dans la stratosphère; CSP étaient abondants sur de nombreuses régions de haute latitude jusqu'à dissipée par un événement de grande réchauffement, qui a commencé dans la stratosphère supérieure au cours de Février et se propage à travers la stratosphère arctique en Mars. La taille de la zone arctique de anormalement bas ozone total en 2004-2005 était plus grande que dans ne importe quelle année depuis 1997. La prédominance des valeurs anormalement faibles de l'ozone total dans la région arctique durant l'hiver 2004-2005 est attribuable à la très faible stratosphérique températures et de conditions météorologiques favorables pour la destruction de l'ozone ainsi que la présence continue de l'ozone détruire les substances chimiques dans la stratosphère.
A 2005 Résumé du GIEC questions de l'ozone observé que les observations et les calculs du modèle suggèrent que la quantité moyenne mondiale de la couche d'ozone a maintenant environ stabilisé. Bien que la variabilité considérable dans ozone devrait d'année en année, notamment dans les régions polaires, où l'épuisement est plus grand, la couche d'ozone devrait commencer à se redresser au cours des prochaines décennies en raison de la baisse des concentrations de substances appauvrissant la couche d'ozone, en supposant le plein respect du Protocole de Montréal.
Les températures pendant l'hiver arctique de 2006 sont restés assez proche de la moyenne à long terme jusqu'à la fin de Janvier, avec des lectures minimales souvent assez froide pour produire PSC. Au cours de la dernière semaine de Janvier, cependant, un événement majeur de réchauffement envoyé des températures bien supérieures à la normale - beaucoup trop chaudes pour soutenir les CSP. Au moment où les températures ont chuté de retour près de la normale en Mars, la norme saisonnière était bien au-dessus du seuil de la CFP. Cartes de l'ozone de l'instrument généré satellite préliminaire montrent l'accumulation d'ozone saison légèrement en dessous des moyens à long terme pour l'hémisphère Nord dans son ensemble, bien que certains événements d'ozone élevées ont eu lieu. Au cours de Mars 2006, la stratosphère arctique vers le pôle de 60 degrés de latitude Nord était libre de zones anormalement faibles d'ozone, sauf pendant la période de trois jours du 17 Mars to 19 ans quand la couverture totale d'ozone est tombé en dessous de 300 DU sur une partie de la région de l'Atlantique Nord, du Groenland à la Scandinavie.
La zone où la colonne d'ozone totale est inférieure à 220 DU (la définition acceptée de la frontière du trou d'ozone) était relativement faible jusqu'à environ 20 Août 2006 . Depuis lors, la zone du trou d'ozone a augmenté rapidement, atteignant un sommet de 29 millions de km² Septembre 24. En Octobre 2006, la NASA a indiqué que le trou d'ozone de l'année établi un nouveau record de la zone avec une moyenne quotidienne de 26 millions de km² entre 7 Septembre et 13 Octobre 2006 ; total des épaisseurs de la couche d'ozone ont chuté aussi bas que 85 UA sur Octobre 8. Les deux facteurs combinés, 2006 voit le pire niveau de l'appauvrissement de l'ozone dans l'histoire enregistrée. L'épuisement est attribuée à des températures au-dessus de l'Antarctique atteignant le plus bas depuis l'enregistrement des dossiers complets ont commencé en 1979.
On prévoit que le trou d'ozone antarctique se poursuivre pendant des décennies. Les concentrations d'ozone dans la basse stratosphère dessus de l'Antarctique va augmenter de 5% à 10% en 2020 et revenir à des niveaux d'avant 1980 d'environ 2060 à 2075, 10-25 ans plus tard que prévu dans les évaluations antérieures. Ceci est dû à des estimations révisées des concentrations atmosphériques de substances appauvrissant l'ozone - et une plus grande utilisation future prévue dans les pays en développement. Un autre facteur qui peut aggraver la couche d'ozone est le rabattement des oxydes d'azote au-dessus de la stratosphère en raison de l'évolution des modes de vent.
Histoire de la recherche
Les processus physiques et chimiques de base qui conduisent à la formation d'une couche d'ozone dans la stratosphère de la terre ont été découverts par Sydney Chapman en 1930. Celles-ci sont abordées dans l'article cycle de l'ozone et d'oxygène - brièvement, courte longueur d'onde rayonnement UV divise un atome d'oxygène (O 2 ) en deux molécule d'oxygène (O) atomes, qui se combinent ensuite avec d'autres molécules d'oxygène pour former de l'ozone. L'ozone est éliminé quand un atome d'oxygène et une molécule d'ozone "recombiner" pour former deux molécules d'oxygène, soit O + O 3 → 2O 2 . Dans les années 1950, David Bates et Marcel Nicolet ont présenté des preuves que divers radicaux libres, en particulier hydroxyle (OH) et de l'oxyde nitrique (NO), pourraient catalyser cette réaction de recombinaison, en réduisant le montant global de l'ozone. Ces radicaux libres sont connus pour être présents dans la stratosphère, et étaient donc considérés comme faisant partie de l'équilibre naturel - il a été estimé qu'en leur absence, la couche d'ozone serait environ deux fois plus épaisse, car elle est actuellement.
En 1970, Prof. Paul Crutzen a souligné que les émissions de nitreux oxyde (N 2 O), un gaz stable, à long terme produite par les bactéries du sol, de la surface de la terre pourraient affecter la quantité d' azote oxyde (NO) dans la stratosphère. Crutzen a montré que l'oxyde nitreux vit assez longtemps pour atteindre la stratosphère, où il est converti en NO. Crutzen a ensuite noté que l'utilisation croissante des engrais aurait pu conduire à une augmentation des émissions d'oxyde nitreux sur le fond naturel, ce qui serait à son tour entraîner une augmentation de la quantité de NO dans la stratosphère. Ainsi, l'activité humaine pourrait avoir un impact sur la couche d'ozone stratosphérique. Dans l'année suivante, et Crutzen (indépendamment) Harold Johnston a suggéré que les émissions de NO de supersonique des avions , qui volent dans la stratosphère inférieure, pourraient aussi appauvrir la couche d'ozone.
L'hypothèse Rowland-Molina
En 1974, Frank Sherwood Rowland, professeur de chimie à l'Université de Californie à Irvine, et son associé postdoctoral Mario J. Molina ont suggéré que les composés organiques halogénés à long terme, tels que les CFC, pourraient se comporter de la même façon que Crutzen avait proposée pour l'oxyde nitreux. James Lovelock (plus populairement connu comme le créateur de l' hypothèse Gaïa) avait récemment découvert, lors d'une croisière dans l'Atlantique Sud en 1971, que presque tous les composés à base de CFC fabriqués depuis leur invention en 1930 étaient encore présents dans l'atmosphère. Molina et Rowland ont conclu que, comme N 2 O, la CFC serait atteindre la stratosphère où ils seraient décomposés par la lumière UV, libérant des atomes Cl. (Un an plus tôt, Richard Stolarski et Ralph Cicerone à l'Université du Michigan ont montré que Cl est encore plus efficace que NO à catalyser la destruction de l'ozone. conclusions similaires ont été tirées par Michael McElroy et Steven Wofsy à l'Université Harvard. Aucun des deux groupes, cependant , avait réalisé que les CFC étaient une source potentiellement importante de chlore stratosphérique - à la place, ils avaient enquêté sur les effets possibles des émissions de HCl de la navette spatiale, qui sont beaucoup plus petites).
Susan Solomon, un chimiste de l'atmosphère à la National Oceanic and Atmospheric Administration (NOAA), a proposé que les réactions chimiques sur les nuages stratosphériques polaires (PSC) dans la stratosphère à froid de l'Antarctique causé un énorme, bien localisée et saisonnière, augmentation de la quantité de chlore présent dans , formes destructrices d'ozone actives. Les nuages stratosphériques polaires en Antarctique ne se forment quand il ya des températures très basses, aussi bas que -80 degrés C , et les conditions au début du printemps. Dans ces conditions les cristaux du nuage de glace fournir une surface appropriée pour la conversion de composés de chlore réactifs chlorés en composés réactifs qui peuvent facilement épuiser l'ozone.
En outre, le vortex polaire formée dessus de l'Antarctique est très serré et la réaction qui se produit sur la surface des cristaux des nuages est très différent de quand il se produit dans l'atmosphère. Ces conditions ont conduit à la formation de trous d'ozone dans l'Antarctique. Cette hypothèse a été confirmée de manière décisive, d'abord par des mesures en laboratoire et par la suite par des mesures directes, à partir du sol et des avions à haute altitude, de très fortes concentrations de monoxyde de chlore (ClO) dans la stratosphère antarctique.
D'autres hypothèses, qui avait attribuées le trou d'ozone à des variations dans le rayonnement UV solaire ou à des changements dans la circulation atmosphérique, ont également été testés et se sont révélées être intenable.
Pendant ce temps, l'analyse des mesures de l'ozone du réseau mondial de spectrophotomètres Dobson au sol mené un panel international de conclure que la couche d'ozone était en fait en voie d'épuisement, à toutes les latitudes en dehors des tropiques. Ces tendances ont été confirmées par les mesures satellitaires. En conséquence, les grandes nations productrices halocarbures ont convenu d'éliminer progressivement la production des CFC, des halons, et des composés apparentés, un processus qui a été achevé en 1996.
Depuis 1981, le Programme des Nations Unies pour l'environnement a parrainé une série de rapports sur l'évaluation scientifique de la couche d'ozone. La plus récente est à partir de 2007 où les mesures satellites ont montré que le trou dans la couche d'ozone se rétablit et est maintenant le plus petit il a été pendant une dizaine d'années .
La controverse concernant la science et la politique de l'ozone
Ce appauvrissement de l'ozone a lieu ne soit pas sérieusement contesté dans la communauté scientifique. Il ya un consensus parmi les physiciens et les chimistes de l'atmosphère que la compréhension scientifique a maintenant atteint un niveau où les contre-mesures pour contrôler les émissions de CFC sont justifiées, même si la décision est finalement un pour les décideurs politiques.
Malgré ce consensus, la science derrière la couche d'ozone reste complexe, et certains opposants à l'application de contre-mesures pointer vers certaines des incertitudes. Par exemple, bien que l'augmentation UVB a été montré pour constituer un risque de mélanome, il a été difficile pour des études statistiques pour établir un lien direct entre la couche d'ozone et l'augmentation des taux de mélanome. Bien que les mélanomes ont fait augmenter de manière significative au cours de la période 1970-1990, il est difficile de séparer de manière fiable l'effet de la couche d'ozone de l'effet des changements dans les facteurs de style de vie (par exemple, l'augmentation des taux de Voyage de l'air).
appauvrissement de l'ozone et le réchauffement climatique
Bien qu'ils soient souvent liés dans la mass media , la connexion entre le réchauffement climatique et la raréfaction de l'ozone est pas forte. Il ya quatre domaines de liaison:
- La même CO2forçage radiatif qui produit près de la surface réchauffement de la planète devrait refroidir le stratosphère.Ce refroidissement, à son tour, devrait produire un rapportaugmentationen polaireozone(O3) l'épuisement et la fréquence des trous d'ozone.

- Inversement, la couche d'ozone représente un forçage radiatif du système climatique. Il ya deux effets opposés: l'ozone réduit provoque la stratosphère à absorber le rayonnement solaire est moindre, refroidissant ainsi la stratosphère tout en réchauffant le troposphère; moins de rayonnement la stratosphère plus froide résultant émet des ondes longues vers le bas, refroidissant ainsi la troposphère. Dans l'ensemble, le refroidissement domine; le GIEC conclut que " observés stratosphériques O 3 pertes au cours des deux dernières décennies ont causé forçant un négatif du système surface-troposphère "d'environ -0,15 ± 0,10 watts par mètre carré (W / m²).
- L'une des prédictions les plus forts de l'effet de serre est que la stratosphère se refroidira. Bien que ce refroidissement a été observé, il est trivial de séparer les effets de l'évolution de la concentration de gaz à effet de serre et la couche d'ozone depuis deux mènera au refroidissement. Cependant, cela peut être fait par modélisation numérique stratosphérique. Résultats de la National Oceanic and Atmospheric Administration de géophysique Fluid Dynamics Laboratory montrent que plus de 20 kilomètres (12,4 milles), les gaz à effet de serre dominent le refroidissement.
- Appauvrissant l'ozone sont également des produits chimiques à effet de serre. Les augmentations des concentrations de ces produits chimiques ont produit 0,34 ± 0,03 W / m² de forçage radiatif, correspondant à environ 14% du forçage radiatif total des augmentations des concentrations de gaz à effet de serre bien mélangés.
- La modélisation à long terme du processus, sa mesure, l'étude, la conception et les tests des théories mettent des décennies à la fois le document, gagner une large acceptation, et finalement devenir le paradigme dominant. Plusieurs théories sur la destruction de l'ozone, ont été hyphtosized dans les années 1980, publié à la fin des années 1990, et sont actuellement prouvées. Dr Drew Schindell, et le Dr Paul Newman, Goddard de la NASA, a proposé une théorie dans les années 1990, l'aide d'un superordinateur SGI Origin 2000, que la destruction de l'ozone modélisées, représentaient 78% de l'ozone détruit. Le perfectionnement de ce modèle, a représenté 89% de l'ozone détruit, mais repoussé la reprise estimée du trou d'ozone de 75 ans à 150 ans. (Une partie importante de ce modèle est l'absence de vol staratospheric raison de l'épuisement des combustibles fossiles.)
Les idées fausses sur la couche d'ozone
Quelques-uns des malentendus les plus courantes sur la couche d'ozone sont brièvement abordé ici; des discussions plus détaillées peuvent être trouvées dans la couche d'ozone de FAQ.
Les CFC sont "trop lourd" pour atteindre la stratosphère
Il est parfois dit que puisque les molécules de CFC sont beaucoup plus lourds que l'azote ou l'oxygène, ils ne peuvent pas atteindre la stratosphère en quantités importantes. Mais gaz atmosphériques ne sont pas triés par poids; les forces de vent (turbulence) sont suffisantes pour pleinement gaz intermix dans l'atmosphère forte. Les CFC sont plus lourds que l'air, mais tout comme l'argon , le krypton et d'autres gaz lourds avec une longue durée de vie, elles sont réparties uniformément dans tout le turbosphère et atteindre la haute atmosphère.
Un trou d'ozone a été observé pour la première en 1956
GMB Dobson (Exploration de l'atmosphère, 2e édition, Oxford, 1968) a mentionné que lorsque les niveaux d'ozone au printemps plus de Halley Bay ont d'abord été mesurées, il a été surpris de constater qu'ils étaient ~ 320 DU, environ 150 DU dessous des niveaux de printemps, ~ 450 DU, dans l'Arctique. Ceux-ci, cependant, étaient les trous valeurs normales climatologiques pré-couche d'ozone. Qu'est-ce Dobson décrit est essentiellement la ligne de base à partir de laquelle le trou d'ozone est mesurée: valeurs de trou d'ozone réelle sont dans la gamme 150-100 DU.
L'écart entre l'Arctique et l'Antarctique a noté Dobson était principalement une question de timing: pendant les niveaux d'ozone de printemps de l'Arctique ont augmenté en douceur, avec un pic en Avril, alors que dans l'Antarctique ils sont restés à peu près constant au début du printemps, se levant brusquement en Novembre quand le vortex polaire est tombé en panne.
Le comportement vu dans le trou d'ozone antarctique est complètement différent. Au lieu de rester des niveaux constants, début printemps ozone chutent brusquement de leurs valeurs déjà faibles d'hiver, par autant que 50%, et les valeurs normales ne sont pas atteints à nouveau jusqu'à Décembre.
Le "trou d'ozone" est un trou dans la couche d'ozone
Lorsque les formes "trou d'ozone", la quasi-totalité de l'ozone dans la stratosphère inférieure est détruit. La stratosphère supérieure est beaucoup moins touché, cependant, de sorte que le montant global de l'ozone sur le continent diminue de 50 pour cent ou plus. Le trou d'ozone ne va pas tout le chemin à travers la couche; d'autre part, il est un pas uniforme "amincissement" de la couche non plus. Il est un "trou" dans le sens de "un trou dans le sol", une dépression, et non pas dans le sens de "un trou dans le pare-brise."
Journée de l'ozone mondial
En 1994, l'Assemblée générale des Nations Uniesa voté pour désigner16 Septembre comme "Journée de l'ozone mondiale", pour commémorer la signature duProtocole de Montréal à cette date en 1987.

