
Centre de réaction photosynthétique
Saviez-vous ...
Cette sélection écoles a été choisi par SOS Enfants pour les écoles dans le monde en développement ne ont pas accès à Internet. Il est disponible en téléchargement intranet. Mères SOS chaque regard après une une famille d'enfants parrainés .
Un centre de réaction photosynthétique (ou un centre de réaction photosynthétique) est un complexe de plusieurs protéines, des pigments et d'autres co-facteurs assemblés pour exécuter les réactions de conversion d'énergie primaires de la photosynthèse . Excitations moléculaires, soit provenant directement de la lumière du soleil ou transféré comme énergie d'excitation via systèmes d'antennes collecteurs de lumière, donnent lieu à Les réactions de transfert d'électrons le long d'une série de co-facteurs liés aux protéines. Ces co-facteurs sont absorbant la lumière molécules (également nommés chromophores ou pigments), tels que chlorophylle et phaeophytine, ainsi que quinones. L'énergie du photon est utilisé pour promouvoir un électron à un le niveau d'énergie moléculaire plus élevé d'un pigment. Le énergie libre créé est ensuite utilisé pour réduire une chaîne de proximité accepteurs d'électrons, qui ont par la suite plus redox potentiels. Ces les étapes de transfert d'électrons sont la phase initiale d'une série de réactions de conversion d'énergie, entraînant finalement la production d'énergie chimique au cours de la photosynthèse .
Transformer l'énergie lumineuse en séparation de charge
centres de réaction sont présents dans tous les verts des plantes , des algues , et de nombreuses bactéries . Bien que ces espèces sont séparées par des milliards d'années d' évolution , les centres réactionnels sont homologue pour toutes les espèces photosynthétiques. En revanche, dans une grande variété complexes collecteurs de lumière existent entre les espèces photosynthétiques. Les plantes vertes et les algues ont deux types de centres réactionnels différents qui font partie des plus grands appelés supercomplexes photosystème IP700 et photosystème II P680. Les structures de ces supercomplexes sont grandes, impliquant multiple complexes collecteurs de lumière. Le centre de réaction trouvé dans Bactéries Rhodopseudomonas est actuellement mieux compris, car il était le premier centre de réaction de structure connue et a moins chaînes de polypeptide que les exemples de plantes vertes.
Un centre de réaction est disposé de telle manière qu'il capte l'énergie d'un photon en utilisant des molécules de pigment et le transforme en une forme utilisable. Une fois que l'énergie lumineuse est absorbée directement par les molécules de pigment, ou transmis à eux par transfert de résonance à partir d'un environnante Antenne collectrice, ils libèrent deux électrons dans un chaîne de transport d'électrons.
La lumière est composée de petits paquets d'énergie appelés photons . Si un photon avec la bonne quantité d'énergie frappe un électron, il va augmenter l'électron à un niveau supérieur le niveau d'énergie. Les électrons sont plus stables à leur niveau d'énergie plus faible, ce qui est aussi appelé son état fondamental. Dans cet état, l'électron est dans l'orbite qui a le moins d'énergie possible. Les électrons dans les niveaux élevés de l'énergie peuvent revenir à l'état du sol d'une manière analogue à une chute d'une bille dans un escalier. Ce faisant, libèrent de l'énergie des électrons. Ce est le processus qui est exploité par un centre de réaction photosynthétique.
Lorsqu'un électron se élève à un niveau d'énergie supérieur, dans la diminuer potentiel de réduction de la molécule dans laquelle réside l'électron se produit. Cela signifie que la molécule a une plus grande tendance à donner des électrons, la clé de la conversion d'énergie lumineuse en énergie chimique. Dans les plantes vertes, la chaîne de transport d'électrons qui suit présente de nombreux accepteurs d'électrons, y compris phaeophytine, quinone, plastoquinone, cytochrome bf, et ferrédoxine, qui ont pour effet de réduire la molécule NADPH. Le passage de l'électron à travers la chaîne de transport d'électrons se traduit également par le pompage de protons (ions d'hydrogène) à partir de la chloroplaste de dans le stroma lumen, ce qui entraîne un gradient de protons à travers la membrane des thylakoïdes qui peut être utilisé pour la synthèse d' ATP en utilisant ATP synthase. Tant l'ATP et le NADPH sont utilisés dans le Cycle de Calvin pour fixer le dioxyde de carbone en sucres triose.
Bactéries
Structure
| Centre de réaction photosynthétique bactérienne | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| Centre de réaction photosynthétique bactérienne | |||||||||
| Identificateurs | |||||||||
| Symbole | |||||||||
| Pfam | PF00124 | ||||||||
| InterPro | IPR000484 | ||||||||
| PROSITE | PDOC00217 | ||||||||
| SCOP | 1prc | ||||||||
| SUPERFAMILLE | 1prc | ||||||||
| TCDB | 3.E.2 | ||||||||
| |||||||||
Le centre de réaction photosynthétique bactérienne a été un modèle important de comprendre la structure et la chimie du processus biologique de capturer l'énergie de la lumière. Dans les années 1960, Roderick Clayton fut le premier à purifier le complexe de centres réactionnels de bactéries pourpres. Cependant, la première structure cristalline a été déterminée en 1982 par Hartmut Michel, Johann et Deisenhofer Robert Huber pour lesquels ils ont partagé le prix Nobel en 1988. Ce était également importante, puisque ce était la première structure de tout complexe de protéines de la membrane.
Quatre sous-unités différentes sont révélés être importants pour la fonction de centre réactionnel photosynthétique. Les sous-unités L et M, en bleu et violet à l'image de la structure, à la fois couvrent le bicouche lipidique de la membrane plasmique. Ils sont de structure similaire à une autre, les deux ayant 5 transmembranaire hélices alpha. Quatre bactériochlorophylle b (BChl-b), deux molécules b molécules bacteriophaeophytin (HBP), deux molécules quinones (Q A et Q B), et un ion ferreux sont associés à la L et M sous-unités. La sous-unité H, représenté à l'or, se trouve du côté cytoplasmique de la membrane plasmique. Une sous-unité de cytochrome, ici non représenté, contient quatre hèmes de type c et se trouve sur la surface périplasmique (extérieur) de la membrane. La sous-unité-ci ne est pas un motif de structure générale dans des bactéries photosynthétiques. Les sous-unités L et M lient les cofacteurs fonctionnels et légers interagissant, montrées ici en vert.
centres de réaction provenant de différentes espèces bactériennes peuvent contenir légèrement modifié bactério-chlorophylle et chromophores bactério-phaeophytine tant que co-facteurs fonctionnels. Ces modifications entraînent des changements dans la couleur de la lumière qui peut être absorbée, créant ainsi des niches spécifiques pour la photosynthèse. Le centre de réaction contient deux pigments qui servent à collecter et transférer l'énergie de l'absorption de photons: BChl et l'HBP. BChl ressemble à peu près à la molécule de chlorophylle dans les plantes vertes, mais, en raison des différences structurelles mineures, sa longueur d'onde d'absorption maximale est décalée dans le infrarouge, de longueurs d'onde aussi longtemps que 1000 nm. Bph a la même structure que BChl, mais l'ion magnésium central est remplacé par deux protons. Cette modification fait à la fois un décalage maximum absorbance et un potentiel d'oxydoréduction réduit.
Mécanisme

Le processus commence lorsque la lumière est absorbée par deux molécules BChl (un dimère) qui se trouvent près de la côté périplasmique de la membrane. Cette paire de molécules de chlorophylle, souvent appelé la «paire spécial", absorbe les photons entre 870 nm et 960 nm, selon les espèces et, par conséquent, est appelé P870 (pour l'espèce Rhodobacter sphaeroides) ou P960 (pour Rhodopseudomonas viridis), avec P permanent pour "pigment"). Une fois P absorbe un photon, elle éjecte un électron, qui est transférée à travers une autre molécule de Bchl à la HBP aux L sous-unité. Cette première exiger la séparation donne une charge positive sur P et une charge négative sur la HBP. Ce processus se déroule dans 10 picosecondes (10 -11 secondes).
Les charges sur la specialpair + et le - BPh pourraient subir une recombinaison responsable dans cet état. Ce serait gaspiller l'électron de haute énergie et de convertir l'énergie lumineuse absorbée à la chaleur . Plusieurs facteurs de la structure du centre de réaction servent à empêcher cela. Tout d'abord, le transfert d'un électron de BPH - à + P960 est relativement lente par rapport à deux autres réactions d'oxydoréduction dans le centre de réaction. Les réactions plus rapides impliquent le transfert d'un électron de BPh - (HBP - est oxydé à l'HBP) à l'accepteur d'électrons quinone (Q A), et le transfert d'un électron à P960 + (P960 + est réduit à P960) à partir d'un hème dans la sous-unité de cytochrome-dessus du centre de réaction.
L'électron à haute énergie qui réside sur la molécule de quinone étroitement lié Q A est transféré à une quinone échangeables Q molécule B. Cette molécule est vaguement associée à la protéine et est assez facile à détacher. Deux des électrons de haute énergie sont nécessaires pour réduire complètement Q B à QH 2, prendre deux protons du cytoplasme dans le processus. La quinone réduite QH 2 diffuse à travers la membrane à un autre complexe de protéines ( bc cytochrome une -comlex) où il est oxydé. Dans le procédé le pouvoir réducteur de la QH 2 est utilisée pour pomper des protons à travers la membrane vers l'espace périplasmique. Les électrons du cytochrome bc 1-complexe sont ensuite transférés à travers une cytochrome c soluble intermédiaire, appelé cytochrome c 2, dans le périplasme de la sous-unité de cytochrome. Ainsi, le flux d'électrons dans ce système est cyclique.
Les plantes vertes
Photosynthèse Oxygenic
En 1772, le chimiste Joseph Priestley a effectué une série d'expériences relatives aux gaz impliqués dans la respiration et la combustion. Dans sa première expérience, il a allumé une bougie et l'a placé sous un pot renversé. Après une courte période de temps, la bougie brûlé. Il a réalisé une expérience similaire avec une souris dans l'espace confiné de la bougie allumée. Il a constaté que la souris est morte peu de temps après la bougie avait été éteint. Toutefois, il pourrait revivifier l'air vicié en plaçant les plantes vertes dans la région et de les exposer à la lumière. Les observations de Priestley ont été parmi les premières expériences qui ont démontré l'activité d'un centre de réaction photosynthétique.
En 1779, Jan Ingenhousz effectué plus de 500 expériences étalées sur quatre mois dans une tentative de comprendre ce qui se passait vraiment. Il a écrit ses découvertes dans un livre intitulé Expériences sur légumes. Ingenhousz a pris les plantes vertes et les immergé dans l'eau dans un réservoir transparent. Il a observé de nombreuses bulles qui montent à la surface des feuilles à chaque fois que les plantes ont été exposées à la lumière. Ingenhousz recueilli le gaz qui a été dégagée par les plantes et effectué plusieurs tests différents pour tenter de déterminer ce que le gaz était. Le test qui a finalement révélé l'identité du gaz plaçait un cône qui couve dans l'échantillon de gaz et de l'avoir rallumer. Ce test a prouvé qu'il était l'oxygène, ou, comme Joseph Priestley l'avait appelé, 'de- phlogiftiqué air '.
En 1932, le professeur Robert Emerson et un étudiant de premier cycle, William Arnold, ont utilisé une technique flash répétitif de mesurer avec précision de petites quantités d'oxygène évolué par la chlorophylle dans le algue chlorella. Leur expérience a prouvé l'existence d'une unité de photosynthèse. Gaffron et Wohl tard interprétées l'expérience et ont réalisé que la lumière absorbée par l'unité photosynthétique a été transféré. Cette réaction se produit au centre de réaction du photosystème II et se déroule dans les cyanobactéries, les algues et les plantes vertes.
Photosystème II

Photosystème II est le photosystème qui génère les deux électrons qui finira par réduire NADP + en Ferredoxin-NADP-reduktase. Photosystème II est présent sur les membranes des thylakoïdes intérieur des chloroplastes, le site de la photosynthèse des plantes vertes. La structure du photosystème II est remarquablement similaire au centre de réaction bactérien, et il est émis l'hypothèse qu'ils partagent un ancêtre commun.
Le noyau du photosystème II se compose de deux sous-unités dénommées D1 et D2. Ces deux sous-unités sont semblables à L et M sous-unités présentes dans le centre de réaction bactérien. Photosystème II diffère du centre de réaction bactérien en ce qu 'il a de nombreuses sous-unités supplémentaires qui se lient chlorophylles supplémentaires pour augmenter l'efficacité. La réaction globale catalysée par photosystème II est:
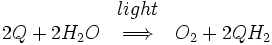
Q représente plastoquinone, la forme oxydée de Q. QH 2 représente plastoquinol, la forme réduite de Q. Ce processus de réduction de quinone est comparable à celle qui a lieu dans le centre de réaction bactérienne. Photosystème II obtient électrons par oxydation de l'eau dans un processus appelé photolyse. L'oxygène moléculaire est un sous-produit de ce processus, et ce est cette réaction qui fournit le atmosphère d'oxygène. Le fait que l'oxygène de plantes vertes provient l'eau a été déduit par le biochimiste américain né au Canada Martin David Kamen. Il a utilisé un produit naturel, l'isotope stable de l'oxygène, O 18 pour suivre le trajet de l'oxygène, de l'eau à l'oxygène moléculaire gazeux. Cette réaction est catalysée par un centre réactif dans photosystème II contenant quatre manganèse ions .
La réaction commence par l'excitation d'une paire de chlorophylle molécules similaires à celles dans le centre de réaction bactérien. En raison de la présence de chlorophylle a, par opposition à bactériochlorophylle, photosystème II absorbe la lumière à une longueur d'onde plus courte. La paire de molécules de chlorophylle dans le centre de réaction sont souvent désignés sous le nom de P680. Lorsque le photon est absorbé, l'électron à haute énergie résultante est transférée à une molécule d'phaeophytine proximité. Ce est au-dessus et à droite de la paire sur le diagramme et est de couleur grise. L'électron se déplace à partir de la molécule d'phaeophytine par deux molécules de plastoquinone, le premier étroitement liés, le deuxième faiblement liée. La molécule étroitement lié apparaît au-dessus de la molécule phaeophytine et est de couleur rouge. La molécule est lié de façon lâche à la gauche de ce et est également de couleur rouge. Ce flux d'électrons est similaire à celle du centre de réaction bactérien. Deux électrons sont nécessaires pour réduire complètement la molécule de plastoquinone vaguement lié à QH 2 ainsi que l'adoption de deux protons.
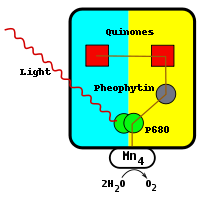
La différence entre le photosystème II et le centre de réaction bactérien est la source de l'électron qui neutralise la paire de molécules de chlorophylle a. Au centre de réaction bactérien, l'électron est obtenu à partir d'un groupe composé de l'hème réduit dans une sous-unité de cytochrome ou d'une protéine cytochrome-c soluble dans l'eau.
Une fois séparation de charge photoinduit a eu lieu, la molécule de P680 porte positif accusation . P680 est une très forte oxydantes et extraits de deux électrons eau molécules qui sont liés au centre de manganèse directement en dessous de la paire. Ce centre, en bas et à gauche de la paire dans le diagramme, contient quatre ions manganèse, un calcium , un ion chlorure et un ion résidu tyrosine. Le manganèse est efficace car il est capable d'exister sous quatre états d'oxydation: Mn 2+, Mn 3+, Mn 4+ et 5+ Mn. Manganèse forme également des liens solides avec des molécules contenant de l'oxygène tels que l'eau.
Chaque fois que le P680 absorbe un photon, il émet un électron, gagnant une charge positive. Cette charge est neutralisée par l'extraction d'un électron à partir du centre de manganèse, qui se trouve directement en dessous. Le procédé d'oxydation de deux molécules d'eau nécessite quatre électrons. Les molécules d'eau qui sont oxydés dans le centre de manganèse sont la source des électrons qui réduisent les deux molécules de Q à 2 QH. À ce jour, ce centre catalytique décomposition de l'eau ne peut pas être reproduite par un catalyseur de l'homme.
Photosystème I
Après l'électron a laissé photosystème II, il est transféré dans un Complexe cytochrome b6f, puis à plastocyanine, un bleu cuivre protéines et électrons transporteur. Le complexe de plastocyanine porte l'électron qui neutraliser la paire dans le centre de réaction suivante, photosystème I.
Comme photosystème II et le centre de réaction bactérienne, une paire de molécules de chlorophylle a initie séparation de charge photo-induit. Cette paire est appelée P700. 700 est une référence à la longueur d'onde à laquelle les molécules de chlorophylle absorbent la lumière au maximum. Le P700 se trouve au centre de la protéine. Une fois que la séparation de charge photoinduite a été lancé, l'électron se déplace le long d'une voie à travers une molécule de chlorophylle α situé directement au-dessus du P700, par l'intermédiaire d'une molécule de quinone situé directement au-dessus qui, par trois groupes 4Fe-4S et, enfin, à un complexe d'ferrédoxine interchangeables. Ferrédoxine est une protéine soluble contenant un groupe 2Fe-2S coordonné par quatre résidus cysteine. La charge positive gauche sur la P700 est neutralisé par le transfert d'un électron de plastocyanine. Ainsi, la réaction globale catalysée par le photosystème I est:
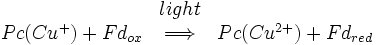
La coopération entre les photosystèmes I et II crée un flux d'électrons à partir de H 2 O en NADP +. Cette voie est appelée «Z-régime» parce que le schéma redox de P680 à P700 ressemble à la lettre z.

