Líquido
Sabías ...
SOS Children, una organización benéfica educación , organizó esta selección. Madres SOS cada aspecto después de un una familia de niños apadrinados .

| Mecánica de medios continuos |
|---|
 |
Leyes
|
Mecánica de sólidos
|
|
Reología
|
Liquid es una de los cuatro estados fundamentales de la materia (los otros son sólidos , gas y plasma ), y es el único estado con un volumen definido pero sin forma fija. Un líquido está compuesto de pequeñas partículas que vibran de la materia, como los átomos y las moléculas, se mantienen unidos por enlaces intramoleculares. El agua es, por lejos, el líquido más común en la Tierra. Como un gas, un líquido es capaz de fluir y tomar la forma de un recipiente. Algunos líquidos resistir la compresión, mientras que otros pueden ser comprimidos. A diferencia de un gas, un líquido no se dispersa para llenar cada espacio de un contenedor, y mantiene una densidad bastante constante. Una propiedad distintiva del estado líquido es la tensión superficial , lo que lleva a fenómenos humectante.
La densidad de un líquido es por lo general cercana a la de un sólido, y mucho mayor que en un gas. Por lo tanto, líquidos y sólidos se denominan tanto de la materia condensada . Por otro lado, como líquidos y gases comparten la capacidad de fluir, ambos están llamados fluidos. Aunque el agua líquida es abundante en la Tierra, este estado de la materia es en realidad el menos común en el universo conocido, porque los líquidos requieren un rango de temperatura / presión relativamente estrecho para existir. Asunto más conocido en el universo está en forma gaseosa (con restos de materia sólida detectable) como nubes interestelares o en forma de plasma dentro de las estrellas.
Introducción

El líquido es uno de los tres primaria estados de la materia, con los otros son sólidos y gas . Un líquido es un fluido. A diferencia de un sólido, las moléculas en un líquido tienen una mayor libertad para moverse. Las fuerzas que se unen las moléculas juntos en un sólido son sólo temporales en un líquido, lo que permite un líquido a fluir mientras que sigue siendo un sólido rígido.
Un líquido, como un gas, muestra las propiedades de un fluido. Un líquido puede fluir, asumir la forma de un recipiente, y, si se colocan en un recipiente sellado, distribuirá uniformemente la presión aplicada a cada superficie en el recipiente. A diferencia de un gas, un líquido no siempre puede mezclar fácilmente con otro líquido, no siempre llenar cada espacio en el recipiente, formando su propia superficie, y no comprimir significativamente, excepto bajo presiones extremadamente altas. Estas propiedades hacen que un líquido adecuado para aplicaciones tales como la hidráulica.
Las partículas líquidas están unidos firmemente, pero no rígida. Ellos son capaces de moverse libremente alrededor de la otra, lo que resulta en un grado limitado de la movilidad de las partículas. Como los temperatura aumenta, el aumento de las vibraciones de las moléculas hace que las distancias entre las moléculas que aumentan. Cuando un líquido alcanza su punto de ebullición , las fuerzas de cohesión que se unen las moléculas estrechamente rompen, y los cambios líquidos a su estado gaseoso (a menos sobrecalentamiento se produce). Si se disminuye la temperatura, las distancias entre las moléculas se hacen más pequeños. Cuando el líquido alcanza su punto de congelación de las moléculas suelen bloquear en un orden muy específico, llamado cristalización, y los vínculos entre ellos ser más rígida, cambiando el líquido en su estado sólido (a menos sobreenfriamiento se produce).
Ejemplos
Sólo dos elementos son líquidos a condiciones normales de temperatura y presión: el mercurio y bromo . Cuatro elementos más tienen puntos de fusión ligeramente por encima temperatura ambiente: francio , cesio , galio y el rubidio . Las aleaciones metálicas que son líquidos a temperatura ambiente incluyen NaK, una aleación de metal de sodio-potasio, galinstan, un líquido aleación fusible, y algunos amalgamas (aleaciones involucran mercurio).
Las sustancias puras que son líquidos en condiciones normales incluyen agua , etanol y muchos otros disolventes orgánicos. El agua líquida es de vital importancia en la química y la biología; que se cree que es una necesidad para la existencia de la vida .
Líquidos cotidianas importantes incluyen acuosas soluciones como hogar lejía, otra mezclas de diferentes sustancias tales como aceite mineral y gasolina, emulsiones como vinagreta o mayonesa, suspensiones, como la sangre , y coloides como pintar y leche .
Muchos de los gases pueden ser líquidos licuados por enfriamiento, tales como la producción de oxígeno líquido, nitrógeno líquido, hidrógeno líquido y helio líquido. No todos los gases pueden ser licuados a presión atmosférica, por ejemplo dióxido de carbono sólo puede ser licuado a presiones superiores a 5,1 atm.
Algunos materiales no se pueden clasificar dentro de los tres clásicos estados de la materia; que poseen propiedades de sólidos como líquidos y similares. Los ejemplos incluyen cristales líquidos , utilizados en las pantallas LCD, y membranas biológicas.
Aplicaciones
Los líquidos tienen una variedad de usos, como lubricantes, disolventes y refrigerantes. En los sistemas hidráulicos, el líquido se utiliza para transmitir energía.
En tribología, los líquidos son estudiados por sus propiedades como lubricantes. Lubricantes tales como aceite son elegidos por características de viscosidad y flujo que son adecuados durante todo el gama de temperaturas de funcionamiento del componente. Los aceites se usan a menudo en motores, cajas de cambio, metalurgia y sistemas hidráulicos para sus buenas propiedades de lubricación.
Muchos de los líquidos se utilizan como disolventes , para disolver otros líquidos o sólidos. Soluciones se encuentran en una amplia variedad de aplicaciones, incluyendo pinturas, selladores, y adhesivos. Naptha y acetona se utilizan con frecuencia en la industria para limpiar aceite, grasa, y el alquitrán a partir de piezas y maquinaria. Los fluidos corporales son soluciones a base de agua.
Los tensioactivos se encuentran comúnmente en jabones y detergentes. Disolventes como alcohol se utilizan a menudo como antimicrobianos. Se encuentran en cosméticos, tintas y líquido láseres de colorante. Se utilizan en la industria alimentaria, en procesos tales como la extracción de aceite vegetal.
Los líquidos tienden a tener mejor conductividad térmica de los gases, y la capacidad de fluir hace que un líquido adecuado para eliminar el exceso de calor de los componentes mecánicos. El calor se puede eliminar mediante la canalización del líquido a través de una intercambiador de calor, tal como una radiador, o el calor pueden ser removidos con el líquido durante el evaporación. El agua o la refrigerantes de glicol se utilizan para mantener motores de sobrecalentamiento. Los refrigerantes utilizados en reactores nucleares incluyen agua o líquidos metales, tales como sodio o de bismuto . Películas propelentes líquidos se usan para enfriar las Cámaras de empuje de cohetes. En mecanizado, agua y aceites se utilizan para eliminar el exceso de calor generado, que puede arruinar rápidamente tanto la pieza de trabajo y la herramienta. Durante la transpiración, el sudor elimina el calor del cuerpo humano por evaporación. En el calefacción, ventilación, y la industria de aire acondicionado (HVAC), líquidos, como el agua se utilizan para transferir calor de un área a otra.
Liquid es el componente principal de sistemas hidráulicos, que se aprovechan de Ley de Pascal para proporcionar Energía en fluidos. Los dispositivos tales como bombas y ruedas hidráulicas se han utilizado para cambiar el movimiento de líquido en trabajo mecánico desde la antigüedad. Aceites son forzados a través bombas hidráulicas, que transmiten esta fuerza para cilindros hidráulicos. Hydraulics se puede encontrar en muchas aplicaciones, tales como frenos de automoción y transmisiones, equipo pesado, y sistemas de control de avión. Vario prensas hidráulicas se utilizan ampliamente en la reparación y la fabricación, para la elevación, presión, amarre y formando.
Los líquidos se utilizan a veces en los dispositivos de medición. La termómetro utiliza a menudo el expansión térmica de líquidos, tales como mercurio , combinado con su capacidad de fluir para indicar la temperatura. La manómetro utiliza el peso del líquido para indicar presión del aire.
Propiedades mecánicas
Volumen
Las cantidades de líquidos se miden comúnmente en unidades de volumen . Estos incluyen la Unidad SI metro cúbico (m 3) y sus divisiones, en particular, el decímetro cúbico, más comúnmente llamado la litros (1 dm 3 = 1 L = 0,001 m 3), y el centímetro cúbico, también llamado mililitro (1 cm 3 = 1 ml = 0.001 L = 10 -6 m 3).
El volumen de una cantidad de líquido se fija por su temperatura y presión. Los líquidos generalmente se expanden cuando se calientan y se contraen cuando se enfrían. Agua entre 0 ° C y 4 ° C es una excepción notable. Los líquidos tienen poco compresibilidad: agua, por ejemplo, requiere una presión del orden de 200 bar para aumentar su densidad por 1/1000. En el estudio de la dinámica de fluidos, líquidos a menudo son tratados como incompresible, especialmente cuando se estudia flujo incompresible.
Presión y flotabilidad
En un campo gravitatorio, líquidos ejercen presión sobre los lados de un contenedor, así como en cualquier cosa dentro del propio líquido. Esta presión se transmite en todas las direcciones y aumenta con la profundidad. Si un líquido está en reposo en un campo gravitatorio uniforme, la presión, p, a cualquier profundidad, z, viene dada por
donde:
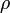 es la densidad del líquido (que se supone constante)
es la densidad del líquido (que se supone constante)  es la aceleración de la gravedad .
es la aceleración de la gravedad .
Tenga en cuenta que esta fórmula supone que la presión en la superficie libre es cero, y que la tensión superficial efectos pueden despreciarse.
Objetos sumergidos en líquidos están sujetas al fenómeno de la flotabilidad. (Flotabilidad se observa también en otros fluidos, pero es especialmente fuerte en líquidos debido a su alta densidad).
Superficies

A menos que el volumen de un líquido coincide exactamente con el volumen de su recipiente, se observan una o más superficies. La superficie de un líquido se comporta como una membrana elástica en la que la tensión superficial aparece, permitiendo la formación de gotas y burbujas. Las ondas de superficie, acción capilar, humectante, y ondulaciones son otras consecuencias de la tensión superficial .
Flujo
Medidas de viscosidad de la resistencia de un líquido que está siendo deformado por cualquiera de tensión de cizallamiento o estrés extensional.
Cuando un líquido es superenfriada hacia el de transición vítrea, la viscosidad aumenta dramáticamente! El líquido se convierte en una medio viscoelástico que muestra tanto las la elasticidad de un sólido y la fluidez de un líquido, dependiendo de la escala de tiempo de observación o de la frecuencia de perturbación.
Propagación del sonido
En un fluido el único no-cero rigidez es a la deformación volumétrica (un líquido no mantiene la fuerzas de cizallamiento). Por lo tanto la velocidad del sonido en un fluido está dada por 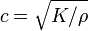 donde K es el módulo de compresibilidad del fluido, y la densidad ρ. Para dar un valor típico, en agua dulce c = 1497 m / s a 25 ° C.
donde K es el módulo de compresibilidad del fluido, y la densidad ρ. Para dar un valor típico, en agua dulce c = 1497 m / s a 25 ° C.
Termodinámica
Transiciones de fase
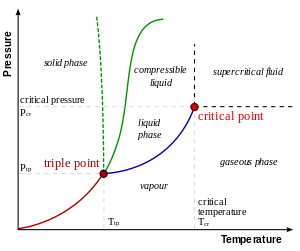
A una temperatura por debajo del punto de ebullición , cualquier materia en forma de líquido se evaporará hasta que la condensación de gas por encima de llegar a un equilibrio. En este punto el gas se condensa en la misma tasa que el líquido se evapora. Por lo tanto, un líquido no puede existir permanentemente si el líquido evaporado se elimina continuamente. Un líquido en su punto de ebullición se evapora más rápidamente que el gas se puede condensar a la presión actual. Un líquido en o por encima de su punto de ebullición normal hervirá, aunque sobrecalentamiento puede evitar que esto en determinadas circunstancias.
A una temperatura por debajo del punto de congelación, un líquido tenderá a cristalizar, cambiando a su forma sólida. A diferencia de la transición a gas, no existe un equilibrio en este transición bajo presión constante, por lo menos sobreenfriamiento ocurre, el líquido finalmente se cristalizará completamente. Tenga en cuenta que esto sólo es cierto bajo presión constante, por lo que por ejemplo, el agua y el hielo en un gran recipiente cerrado podría llegar a un equilibrio en el que las dos fases coexisten. Para la transición opuesta de sólido a líquido, ver de fusión.
Soluciones
Los líquidos pueden mostrar inmiscibilidad. La mezcla más familiar de dos líquidos inmiscibles en la vida cotidiana es el aceite vegetal y agua en Ensalada aderezo italiano. Un conjunto familiar de líquidos miscibles en agua y alcohol. Los componentes líquidos en una mezcla a menudo pueden ser separados uno de otro a través de destilación fraccionada.
Propiedades microscópicas
Factor de estructura estática

En un líquido, átomos no forman una red cristalina, ni muestran cualquier otra forma de orden de largo alcance. Esto se evidencia por la ausencia de Picos de Braga en De rayos X y difracción de neutrones. En condiciones normales, el patrón de difracción tiene simetría circular, que expresa la isotropía del líquido. En dirección radial, la intensidad de difracción oscila suavemente. Esto generalmente se describe por el factor de estructura estática S (q), con número de onda q = (4π / λ) sinθ propuesta por el λ la longitud de onda de la sonda (de fotones o neutrones) y la Θ ángulo de Bragg. Las oscilaciones de S (q) expresan el orden cerca del líquido, es decir, las correlaciones entre un átomo y unos caparazones de más cercano, segundo, ... vecinos más cercanos.
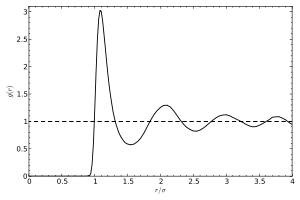
Una descripción más intuitiva de estas correlaciones está dada por la función de distribución radial g (r), que es básicamente el Transformada de Fourier de S (q). Representa un promedio espacial de una instantánea temporal de par correlaciones en el líquido.
Dispersión de sonido y la relajación estructural
La expresión anterior para la velocidad del sonido 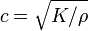 contiene el K módulo de volumen. Si K es independiente de la frecuencia, entonces el líquido se comporta como una medio lineal, por lo que el sonido se propaga sin disipación y sin acoplamiento de modos. En realidad, cualquier líquido muestra algunos dispersión: con frecuencia cada vez mayor, K cruza desde el, límite líquido como de baja frecuencia
contiene el K módulo de volumen. Si K es independiente de la frecuencia, entonces el líquido se comporta como una medio lineal, por lo que el sonido se propaga sin disipación y sin acoplamiento de modos. En realidad, cualquier líquido muestra algunos dispersión: con frecuencia cada vez mayor, K cruza desde el, límite líquido como de baja frecuencia 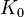 a la alta frecuencia, límite de sólido-like
a la alta frecuencia, límite de sólido-like 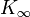 . En los líquidos normales, la mayor parte de esta cruz la entrega se produce a frecuencias entre GHz y THz, a veces llamado Hypersound.
. En los líquidos normales, la mayor parte de esta cruz la entrega se produce a frecuencias entre GHz y THz, a veces llamado Hypersound.
A frecuencias sub-GHz, un líquido normal no puede sostener ondas de corte: el límite de frecuencia cero de la módulo de corte es 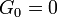 . Esto es a veces visto como la propiedad definitoria de un líquido. Sin embargo, al igual que el módulo de compresibilidad K, el módulo de cizalla G es dependiente de la frecuencia, y en las frecuencias Hypersound muestra una cruz similar a lo largo del límite de tipo líquido
. Esto es a veces visto como la propiedad definitoria de un líquido. Sin embargo, al igual que el módulo de compresibilidad K, el módulo de cizalla G es dependiente de la frecuencia, y en las frecuencias Hypersound muestra una cruz similar a lo largo del límite de tipo líquido 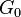 con un límite de tipo sólido, distinto de cero
con un límite de tipo sólido, distinto de cero 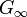 .
.
De acuerdo con la Relación Kramers-Kronig, la dispersión en la velocidad del sonido (dada por la parte real de K o G) va junto con un máximo en la atenuación del sonido (disipación, dada por la parte imaginaria de K o G). De acuerdo a la teoría de respuesta lineal, la transformada de Fourier de K o G se describe cómo el sistema vuelve al equilibrio después de una perturbación externa; Por esta razón, la etapa de dispersión en la región GHz..THz también se llama relajación estructural. Según el teorema de fluctuación-disipación, la relajación hacia el equilibrio está íntimamente ligada a las fluctuaciones en el equilibrio. Las fluctuaciones de densidad asociados con las ondas de sonido se pueden observar experimentalmente Dispersión de Brillouin.
En sobreenfriamiento un líquido hacia la transición vítrea, el crossover de líquido similar al de respuesta mueve sólida como desde GHz a MHz, kHz, Hz, ...; equivalentemente, el tiempo característico de los aumentos de relajación estructural de ns a microsiemens, ms, s, ... Esta es la explicación microscópica del comportamiento viscoelástico mencionado anteriormente de líquidos formadores de vidrio.
Efectos de la asociación
Los mecanismos de atómico / molecular de difusión (o el desplazamiento de las partículas) en los sólidos están estrechamente relacionados con los mecanismos de flujo viscoso y solidificación en materiales líquidos. Descripciones de en términos de la viscosidad molecular "espacio libre" dentro del líquido fueron modificados según sea necesario para tener en cuenta para líquidos cuyas moléculas son conocidos por estar "asociado" en el estado líquido a temperaturas ordinarias. Cuando varias moléculas se combinan entre sí para formar una molécula asociada, que encierran dentro de un sistema semi-rígido de una cierta cantidad de espacio que antes estaba disponible como espacio libre para las moléculas móviles. Por lo tanto, el aumento de la viscosidad al enfriarse debido a la tendencia de la mayoría de las sustancias para asociarse al enfriarse.
Argumentos similares se podrían utilizar para describir los efectos de presión sobre la viscosidad, donde se puede suponer que la viscosidad es principalmente una función del volumen para líquidos con una finita compresibilidad. Por lo tanto, se espera un aumento de la viscosidad con la subida de la presión. Además, si el volumen se expande por calor, pero reduce de nuevo por la presión, la viscosidad sigue siendo el mismo.
La tendencia local para la orientación de las moléculas en grupos pequeños se presta el líquido (según lo anteriormente) un cierto grado de asociación. Esta asociación se traduce en un considerable "presión interna" dentro de un líquido, que se debe casi por completo a las moléculas que, a causa de sus bajas velocidades temporales (siguiendo la distribución de Maxwell) se han unido con otras moléculas. La presión interna entre varias de estas moléculas podría corresponder a la que existe entre un grupo de moléculas en forma sólida.