Esclerosis múltiple
Antecedentes de las escuelas de Wikipedia
SOS Children han producido una selección de artículos de la Wikipedia para escuelas desde 2005. Visite el sitio web de Aldeas Infantiles SOS en http://www.soschildren.org/
| Esclerosis múltiple | |
|---|---|
| Clasificación y recursos externos | |
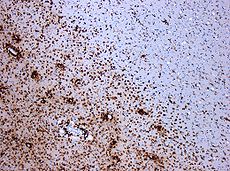 La desmielinización por MS. La De seda de color CD68 muestra varios macrófagos en la zona de la lesión. Escala original 1: 100 | |
| CIE- 10 | G 35 |
| CIE- 9 | 340 |
| OMIM | 126200 |
| DiseasesDB | 8412 |
| MedlinePlus | 000737 |
| Medcenter | neuro / 228 oph / 179 emerg / 321 pmr / 82 radio / 461 |
| MeSH | D009103 |
| GeneReviews |
|
La esclerosis múltiple (MS), también conocido como "esclerosis diseminada" o "encefalomielitis diseminada", es una inflamatoria de la enfermedad en la que el graso vainas de mielina alrededor de la axones de la cerebro y la médula espinal están dañados, lo que lleva a desmielinización y cicatrices, así como un amplio espectro de y signos síntomas. Inicio de la enfermedad por lo general se presenta en adultos jóvenes, y es más común en las mujeres. Tiene un prevalencia que oscila entre 2 y 150 por 100.000. MS fue descrita por primera vez en 1868 por Jean-Martin Charcot.
MS afecta a la capacidad de las células nerviosas en el cerebro y la médula espinal para comunicarse entre sí de manera eficaz. Las células nerviosas se comunican enviando señales eléctricas llamadas potenciales de acción las fibras largas llamadas axones, que están contenidos dentro de una sustancia aislante llamada mielina. En la EM, del propio cuerpo del sistema inmunológico ataca y daña la mielina. Cuando se pierde la mielina, los axones ya no pueden llevar a cabo con eficacia las señales. El nombre de la esclerosis múltiple se refiere a las cicatrices (esclerótica - mejor conocido como placas o lesiones) en particular en el la materia blanca del cerebro y la médula espinal, que se compone principalmente de la mielina. Aunque se sabe mucho sobre los mecanismos implicados en el proceso de la enfermedad, la causa sigue siendo desconocida. Las teorías incluyen la genética o las infecciones . Diferente ambiental También se han encontrado factores de riesgo.
Casi cualquier neurológica síntoma puede aparecer con la enfermedad, y la enfermedad a menudo progresa hasta física y discapacidad cognitiva. MS toma varias formas, con nuevos síntomas que ocurren en los ataques discretos (formas recidivantes) o acumulando con el tiempo (formas progresivas). Entre los ataques, los síntomas pueden desaparecer por completo, pero los déficits neurológicos permanentes ocurren a menudo, sobre todo a medida que avanza la enfermedad.
No se conoce ninguna cura para la esclerosis múltiple. Los tratamientos intentan devolver la función después de un ataque, prevenir nuevos ataques, y prevenir la discapacidad. MS medicamentos pueden tener efectos adversos o ser mal tolerado, y muchas personas seguir tratamientos alternativos, a pesar de la falta de apoyo a estudios científicos. La pronóstico es difícil de predecir; que depende del subtipo de la enfermedad, características de la enfermedad de la persona, los síntomas iniciales y el grado de incapacidad que experimenta la persona como el tiempo avanza. La esperanza de vida de las personas con EM es de 5 a 10 años menor que la de la población no afectada.
Signos y síntomas
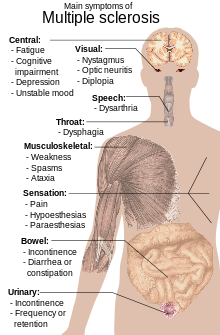
Una persona con EM puede sufrir casi cualquier síntoma o signo neurológico, incluyendo cambios en la sensibilidad, como la pérdida de la sensibilidad u hormigueo, pinchazos o entumecimiento ( hipoestesia y parestesia), debilidad muscular, clonus, espasmos musculares o dificultad en el movimiento; dificultades con la coordinación y el equilibrio ( ataxia); problemas en el habla ( disartria) o tragar ( disfagia), problemas visuales ( nistagmo, neuritis óptica que incluye fosfenos, o diplopía), fatiga, aguda o dolor crónico, y de la vejiga y dificultades intestinales. El deterioro cognitivo de diversos grados y síntomas emocionales de depresión o estado de ánimo inestable también son comunes. Fenómeno de Uhthoff, una exacerbación de los síntomas existentes debido a una exposición a temperaturas ambientales superiores a lo habitual, y Signo de Lhermitte, una sensación eléctrica que baja por la parte posterior al doblar el cuello, son particularmente características de la EM, aunque no específico. La principal medida clínica de la progresión de la discapacidad y la severidad de los síntomas es la Expanded Disability Status Scale o EDSS.
Los síntomas de la EM suelen aparecer en períodos agudos episódicos de empeoramiento (llamados recaídas, las exacerbaciones, combates, ataques, o "flare-ups"), en un deterioro gradual progresiva de la función neurológica, o en una combinación de ambos. Recidivas de esclerosis múltiple son a menudo imprevisibles, que ocurren sin previo aviso y sin factores de incitación obvia con una tasa rara vez por encima de uno y medio por año. Algunos ataques, sin embargo, son precedidos por desencadenantes comunes. Las recaídas son más frecuentes en primavera y verano. Las infecciones virales como el resfriado común , la gripe o gastroenteritis aumentan el riesgo de recaída. El estrés también puede desencadenar un ataque. El embarazo afecta a la susceptibilidad a la recaída, con una menor tasa de recaídas en cada trimestre de la gestación. Durante los primeros meses después del parto, sin embargo, se incrementa el riesgo de recaída. En general, el embarazo no parece influir sobre la incapacidad a largo plazo. Muchos factores desencadenantes potenciales han sido examinados y considerados no influir en las tasas de recaída de la EM. No hay evidencia de que la vacunación y la lactancia, trauma físico, o fenómeno de Uhthoff son disparadores de recaída.
Causas
Lo más probable MS se produce como resultado de una combinación de factores genéticos, ambientales e infecciosas, y posiblemente otros factores como problemas vasculares. Los estudios epidemiológicos de MS han proporcionado pistas sobre las posibles causas de la enfermedad. Las teorías tratan de combinar los datos conocidos en explicaciones plausibles, pero ninguno ha demostrado ser definitivo.
Genética

MS no se considera un enfermedad hereditaria. Sin embargo, un número de variaciones genéticas han demostrado aumentar el riesgo de desarrollar la enfermedad.
El riesgo de adquirir MS es mayor en los familiares de una persona con la enfermedad que en la población general, especialmente en el caso de hermanos, padres y niños. La enfermedad tiene una tasa de recurrencia familiar global de 20%. En el caso de gemelos monocigóticos gemelos, concordancia sólo se produce en aproximadamente el 35% de los casos, mientras que se reduce a alrededor de 5% en el caso de los hermanos y aún menor en medio hermanos. Esto indica la susceptibilidad es en parte poligénicamente impulsado. Parece ser más común en algunos grupos étnicos que en otros.
Aparte de estudios familiares, específica genes se han relacionado con la EM. Las diferencias en el antígeno leucocitario humano (HLA) sistema de un grupo de genes en cromosoma 6 que sirve como el complejo mayor de histocompatibilidad (MHC) en los seres humanos aumentan la probabilidad de padecer EM. El hallazgo más consistente es la asociación entre la esclerosis múltiple y alelos del MHC definido como DR15 y DQ6. Otros loci han demostrado un efecto protector, tal como HLA-C554 y HLA-DRB1 * 11.
Factores ambientales
Diferentes factores ambientales, tanto de origen infeccioso y no infeccioso, se han propuesto como factores de riesgo para la EM. Aunque algunos son parcialmente modificables, los ensayos serán sólo más investigación, especialmente clínica revelan si su eliminación puede ayudar a prevenir la esclerosis múltiple.
La esclerosis múltiple es más común en las personas que viven más lejos del ecuador, aunque existen muchas excepciones. Disminución de la exposición solar se ha relacionado con un mayor riesgo de MS. Disminución de la vitamina D la producción y el consumo ha sido el principal mecanismo biológico utilizado para explicar el mayor riesgo entre las menos expuestas al sol.
Grave el estrés puede ser un factor de riesgo aunque la evidencia es débil. Fumar también se ha demostrado que es un factor de riesgo independiente para el desarrollo de la EM. Asociación con las exposiciones ocupacionales y toxinas -principalmente disolventes -ha sido evaluados, pero no se ha llegado a conclusiones claras. Las vacunas fueron investigados como factores causales de la enfermedad; Sin embargo, la mayoría de los estudios no muestran asociación entre la EM y vacunas. Varios otros posibles factores de riesgo, tales como la dieta y la hormona de admisión, han sido investigados; Sin embargo, la evidencia de su relación con la enfermedad es "escasa y poco convincente".
La gota se produce menos de lo que estadísticamente se espera en las personas con EM, y bajos niveles de ácido úrico se han encontrado en las personas con EM en comparación con individuos normales. Esto condujo a la teoría de que el ácido úrico protege contra la MS, aunque su importancia exacta sigue siendo desconocida.
Infecciones
Muchos microbios se han propuesto como posibles desencadenantes infecciosos de la EM, pero ninguna ha sido probada. Mover a una edad temprana de un lugar en el mundo a otro se altera el riesgo subsiguiente de MS de una persona. Una explicación para esto podría ser que algún tipo de infección, producida por un microbio generalizada en lugar de un patógeno rara, es el origen de la enfermedad. Hay una serie de mecanismos propuestos, incluyendo la hipótesis de la higiene y la hipótesis prevalencia. La hipótesis de la higiene propone que la exposición a varios agentes infecciosos temprano en la vida es protectora contra la MS, la enfermedad de ser una respuesta a un encuentro posterior con tales agentes. La hipótesis propone que la prevalencia de la enfermedad se debe a una patógeno más común en regiones de alta prevalencia de la EM, donde en la mayoría de las personas le produce infección persistente asintomática. Sólo en unos pocos casos, y después de muchos años Qué causa la desmielinización. La hipótesis de la higiene ha recibido más apoyo que la hipótesis de la prevalencia.
La evidencia de los virus como una causa incluye la presencia de bandas oligoclonales en el cerebro y el líquido cefalorraquídeo de la mayoría de las personas con EM, la asociación de varios virus con desmielinización humana encefalomielitis, y la inducción de desmielinización en los animales a través de la infección viral. Herpes virus humanos son un grupo de virus candidatos vinculados a la EM. Las personas que nunca han sido infectadas por el El virus de Epstein-Barr tienen un menor riesgo de padecer la enfermedad, y los infectados como adultos jóvenes tienen un riesgo mayor que los que tenían a una edad más joven. Aunque algunos consideran que esto va en contra de la hipótesis de la higiene, ya que el no infectado probablemente han experimentado una educación más higiénico, otros creen que no hay contradicción, ya que es un primer encuentro en un momento posterior con el virus causante de que es el desencadenante de la enfermedad . Otras enfermedades que también han sido relacionados con la EM son el sarampión , las paperas y la rubéola .
Fisiopatología

Autoimmunology
MS se cree que es una trastorno inmune mediada por una compleja interacción de la genética del individuo y como insultos ambientales aún no identificados. Se cree que el daño causado por el propio sistema inmune de la persona ataca el sistema nervioso. Posibles objetivos de la respuesta inmune incluyen la proteína básica de la mielina (MBP) y proteína proteolipídica (PLP). El fármaco para la EM comúnmente prescrito Copaxone fue diseñado para imitar MBP y por lo tanto actuar como un señuelo para las células inmunes autorreactivas. Aun así, el papel de la PMI en la EM es polémico; que está enterrado dentro de la vaina de mielina (en lugar de en la superficie), donde las células inmunes no serían capaces de reconocerlo.
Los datos recientes sugieren un papel de los lípidos de la mielina en la EM. Históricamente, los investigadores han asumido el objetivo era una proteína de la mielina, a pesar de la vaina de mielina es casi el 80% de lípidos. Además, los lípidos son conocidos por ser el blanco de otro prominente enfermedad autoinmune del sistema nervioso, Síndrome de Guillain-Barré.
Ya sea que el autoantígeno es una proteína o un lípido, la autoinmunidad puede surgir cuando las células inmunes que reconocen un antígeno extraño reacción cruzada con los antígenos propios. Este proceso se conoce como mimetismo molecular.
Las lesiones
El nombre de la esclerosis múltiple se refiere a las cicatrices (esclerótica - mejor conocido como placas o lesiones) que se forman en el sistema nervioso. Lesiones de EM más comúnmente implican áreas de sustancia blanca cerca de la ventrículos del cerebelo , tronco cerebral, ganglios basales y medula espinal; y la nervio óptico. La función de las células de la sustancia blanca es para transportar señales entre áreas de materia gris, donde se realiza el tratamiento, y el resto del cuerpo. La sistema nervioso periférico es rara vez participan.
Más específicamente, MS destruye oligodendrocitos, las células responsables de crear y mantener una capa de grasa conocida como vaina de mielina, que ayuda a las neuronas llevan señales eléctricas (potenciales de acción). MS se traduce en un adelgazamiento o completa pérdida de la mielina y, a medida que avanza la enfermedad, la corte (transección) de la neurona de axones. Cuando se pierde la mielina, una neurona puede llevar a cabo ya no efectivamente señales eléctricas. Un proceso de reparación, llamado remielinización, se lleva a cabo en las primeras fases de la enfermedad, pero los oligodendrocitos no puede reconstruir completamente la vaina de mielina de las células. Los ataques repetidos llevan a remyelinations sucesivamente menos efectiva, hasta que una placa similar a una cicatriz se construye alrededor de los axones dañados. Diferentes patrones de lesión se han descrito.
Inflamación
Aparte de desmielinización, la otra característica patológica de la enfermedad es inflamación. Según un estrictamente explicación inmunológica de MS, el proceso inflamatorio es causado por Las células T, un tipo de linfocitaria. Los linfocitos son células que juegan un papel importante en las defensas del cuerpo. En la EM, las células T entrará en el cerebro a través de las interrupciones en el barrera hematoencefálica. La evidencia de los modelos animales también apuntan a un papel de Las células B, además de las células T en el desarrollo de la enfermedad.
Las células T reconocen la mielina como extraño y atacan como si se tratara de un virus invasor. Esto desencadena procesos inflamatorios, estimular otras células inmunes y factores solubles como citoquinas y anticuerpos . Otras filtraciones se forman en la barrera sangre-cerebro, que a su vez causa una serie de otros efectos perjudiciales tales como hinchazón , la activación de macrófagos, y una mayor activación de citoquinas y otras proteínas destructivas.
Rotura de la barrera hematoencefálica
La barrera sangre-cerebro es una parte de la sistema capilar que impide la entrada de las células T en el sistema nervioso central. Sin embargo, puede ser permeable a estos tipos de células debido a una infección o un virus. Cuando la barrera sangre-cerebro recupera su integridad, típicamente después de la infección o virus ha aclarado, las células T están atrapados en el interior del cerebro.
Diagnóstico
La esclerosis múltiple puede ser difícil de diagnosticar ya que sus signos y síntomas pueden ser similares a otros problemas médicos. Organizaciones médicas han desarrollado criterios de diagnóstico para facilitar y estandarizar el proceso de diagnóstico sobre todo en las primeras etapas de la enfermedad. Históricamente, la Schumacher y Criterios de Poser fueron populares.
Actualmente, el Criterios de McDonald se centran en una manifestación con clínica, datos de laboratorio y radiológicos de la difusión de las lesiones de la EM en el tiempo y el espacio para el diagnóstico no invasivo de MS, aunque algunos han afirmado que el único diagnóstico probado de MS es la autopsia, o de vez en cuando la biopsia, donde las lesiones típico de MS se puede detectar mediante técnicas histopatológicas.
Solo datos clínicos pueden ser suficientes para un diagnóstico de esclerosis múltiple si un individuo ha sufrido episodios separados de síntomas neurológicos característicos de la EM. Dado que algunas personas buscan atención médica después de un solo ataque, otras pruebas puede acelerar y facilitar el diagnóstico. Las herramientas de diagnóstico más utilizados son neuroimagen, análisis de líquido cefalorraquídeo y potenciales evocados. La resonancia magnética del cerebro y la columna vertebral muestra las áreas de desmielinización (lesiones o placas). El gadolinio se puede administrar por vía intravenosa como un contraste para resaltar placas activas y, por eliminación, demostrar la existencia de lesiones históricos no asociados con síntomas en el momento de la evaluación. Ensayo de líquido cefalorraquídeo obtenido de una punción lumbar puede proporcionar evidencia de la crónica inflamación del sistema nervioso central. El líquido cefalorraquídeo es la prueba de bandas oligoclonales de IgG en la electroforesis, que son marcadores de inflamación que se encuentran en el 75-85% de las personas con EM. El sistema nervioso de una persona con EM responde menos activamente a la estimulación de la nervio óptico y nervios sensoriales debido a la desmielinización de tales vías. Estas respuestas cerebrales pueden ser examinadas usando visual y sensorial potenciales evocados.
Cursos clínicos

Varios subtipos, o patrones de progresión, se han descrito. Subtipos utilizan el pasado curso de la enfermedad en un intento de predecir el curso futuro. Ellos son importantes no sólo para el pronóstico, sino también para las decisiones terapéuticas. En 1996 los Estados Unidos National Multiple Sclerosis Society estandarizada cuatro cursos clínicos:
- remitente recidivante,
- secundaria progresiva,
- primaria progresiva, y
- progresiva con recaídas.
El subtipo de recaída-remisión se caracteriza por recaídas imprevisibles seguidos por períodos de meses o años de relativa calma ( remisión) sin nuevos signos de actividad de la enfermedad. Los déficits sufridos durante los ataques o bien puede resolver o dejar secuelas, siendo este último más común como una función del tiempo. Esto describe el curso inicial de 80% de las personas con EM. Cuando los déficit siempre se resuelven entre los ataques, esto se conoce como a veces EM benigna, aunque la gente todavía derivarse algún grado de discapacidad a largo plazo. El subtipo de recaída-remisión por lo general comienza con una síndrome clínicamente aislado (CIS). En la CEI, una persona tiene un ataque sugestivo de desmielinización, pero no cumple con los criterios para la esclerosis múltiple. Sin embargo, sólo 30 a 70% de las personas que experimentan CIS más tarde desarrollar MS.

EM progresiva secundaria describe alrededor del 65% de las personas con una EM remitente-recurrente, que entonces comienza a tener deterioro neurológico progresivo entre los ataques agudos sin periodos definidos de remisión inicial. Pueden aparecer recaídas y remisiones ocasionales leves. La mediana de tiempo entre el inicio de la enfermedad y la conversión de recaída-remisión de EM progresiva secundaria es de 19 años. El subtipo progresiva primaria describe el aproximadamente el 10-15% de las personas que nunca han tenido la remisión después de que sus síntomas iniciales MS. Se caracteriza por la progresión de la discapacidad desde el inicio, que no tenga o sólo ocasional y leve, remisiones y mejoras. La edad de inicio para el subtipo progresiva primaria es posterior a la recaída-remisión, pero similar a la media de edad de progresión entre el remitente-recurrente y la secundaria progresiva. En ambos casos se trata de alrededor de 40 años de edad.
EM progresiva recurrente describe a aquellas personas que, desde el inicio, tienen una disminución neurológico estable, pero también sufren ataques superpuestas claras. Este es el menos común de todos los subtipos.
Variantes atípicas de MS con un comportamiento no estándar se han descrito; éstos incluyen Enfermedad de Devic, Enfermedad de Baló, Esclerosis difusa de Schilder y Esclerosis múltiple Marburg. Existe un debate sobre si son variantes de EM o diferentes enfermedades. La esclerosis múltiple también se comporta de manera diferente en los niños, teniendo más tiempo para llegar a la etapa progresiva. Sin embargo todavía llegar a una edad media inferior a los adultos.
Administración
Aunque no existe una cura conocida para la esclerosis múltiple, varias terapias han demostrado su utilidad. Los objetivos principales de la terapia están regresando funcionar después de un ataque, la prevención de nuevos ataques, y la prevención de la discapacidad. Como con cualquier tratamiento médico, los medicamentos utilizados en el tratamiento de la EM tienen varios efectos adversos. Los tratamientos alternativos son perseguidos por algunas personas, a pesar de la escasez de apoyo, estudio comparable, replica el científico.
Los ataques agudos
Durante los ataques sintomáticos, la administración de altas dosis de intravenoso corticosteroides, como la metilprednisolona, es la terapia de rutina para las recaídas agudas, mientras que los corticosteroides orales parecen tener un perfil de eficacia y seguridad similares. Aunque generalmente eficaz en el corto plazo para aliviar los síntomas, los tratamientos con corticosteroides no parecen tener un impacto significativo en la recuperación a largo plazo. Consecuencias de los ataques graves que no responden a los corticosteroides pueden ser tratados por plasmaféresis.
Tratamientos modificadores de la enfermedad

A partir de enero de 2013, siete tratamientos modificadores de la enfermedad han sido aprobados por los organismos reguladores de los distintos países, incluido el US Food and Drug Administration (FDA), la Agencia Europea de Medicamentos (EMA) y los japoneses PMDA. Los medicamentos aprobados son interferón beta-1a, interferón beta-1b, acetato de glatiramer, mitoxantrona (una inmunosupresor también se utiliza en la quimioterapia del cáncer), natalizumab (a humanizado inmunomodulador anticuerpo monoclonal), fingolimod y teriflunomida.
Los interferones y acetato de glatiramer son entregados por inyecciones frecuentes, que varía de una vez al día para el acetato de glatiramer a una vez por semana (pero intra-muscular) para el interferón beta-1a. Natalizumab y mitoxantrona se dan por vía intravenosa (IV) de infusión a intervalos mensuales en el caso de natalizumab y cada tres meses en el caso de mitoxantrona. En 2010 fingolimod convirtió en el primer fármaco oral aprobado por la FDA, siendo seguido en 2012 por teriflunomida. Fingolimod y teriflunomida se toman a través de una sola dosis diaria.
La mayoría de los medicamentos son aprobados sólo para el curso recurrente-remitente (EMRR). Los medicamentos son modestamente efectiva de reducir el número de ataques en la EMRR.
Los interferones y el acetato de glatiramer son aproximadamente equivalentes, la reducción de recaídas en aproximadamente un 30%. Las comparaciones con natalizumab muestran que los más eficaces es la última, tanto en términos de reducción de la tasa de recaídas y la progresión de la discapacidad detención. La mitoxantrona puede ser el más eficaz de todos ellos; sin embargo, generalmente no se considera como una terapia a largo plazo, ya que su uso está limitado por efectos secundarios graves. Aunque se necesitan más estudios sobre los efectos a largo plazo de los medicamentos, especialmente para los más nuevos tratamientos, los datos existentes sobre los efectos de los interferones y el acetato de glatiramer indican que la terapia temprana iniciada a largo plazo es seguro y que se relaciona con mejores resultados.
La presentación clínica más temprana de la EMRR es el síndrome clínicamente aislado (CIS). El tratamiento con interferones durante un ataque inicial disminuye la probabilidad de que una persona desarrolle MS clínicos. El tratamiento de la EM progresiva es más difícil que remitente-recidivante MS. La mitoxantrona ha demostrado efectos positivos en aquellos con cursos progresiva con recaídas y secundaria progresiva. Es moderadamente eficaz en la reducción de la progresión de la enfermedad y la frecuencia de las recaídas en el corto plazo de seguimiento. Ningún tratamiento ha sido probado para modificar el curso de la EM progresiva primaria. La eficacia de los tratamientos más comunes, interferones y el acetato de glatiramer, en la aparición temprana de la EM (antes de los dieciocho años de edad) se ha estimado en más o menos equivalente a los adultos.
Al igual que con muchos tratamientos médicos, estos tratamientos tienen varios efectos adversos. Uno de los más comunes es la irritación en el sitio de la inyección para el acetato de glatiramer y los tratamientos con interferón. Con el tiempo, un hueco visible en el sitio de inyección, debido a la destrucción local de tejido graso, conocido como lipoatrofia, se puede desarrollar. Los interferones producen síntomas similares a la gripe; algunas personas que toman glatiramer experiencia una reacción post-inyección manifiestan por rubor, opresión en el pecho, palpitaciones, falta de aire, y la ansiedad, que suele durar menos de treinta minutos. Más peligroso, pero mucho menos comunes son daño hepático por interferones, grave cardiotoxicidad, infertilidad, y leucemia mieloide aguda de mitoxantrona, y el vínculo entre el supuesto natalizumab y algunos casos de leucoencefalopatía multifocal progresiva. Efectos secundarios fingolimod en los ensayos clínicos han incluido condiciones cardiovasculares, edema macular, infecciones, toxicidad hepática y tumores malignos.
La gestión de los efectos de la EM
Tratamientos modificadores de la enfermedad reducen la tasa de progresión de la enfermedad, pero no detenerlo. Como esclerosis múltiple progresa, la sintomatología tiende a aumentar. La enfermedad se asocia con una variedad de síntomas y déficits funcionales que resultan en una gama de deterioros progresivos y discapacidad. Por lo tanto, de gestión de estos déficit es muy importante. Tanto la terapia de drogas y neurorehabilitación han mostrado para aliviar la carga de algunos síntomas, aunque ninguno de progresión de la enfermedad influencias. Algunos de los síntomas tienen una buena respuesta a la medicación, como la vejiga inestable y la espasticidad, mientras que la gestión de muchos otros es mucho más complicado. Como para cualquier persona con deficiencias neurológicas, una enfoque multidisciplinario es fundamental para mejorar la calidad de vida; Sin embargo, existen dificultades particulares en la especificación de un "equipo básico" porque las personas con EM pueden necesitar ayuda de casi cualquier profesión sanitaria o servicio en algún momento. Programas de rehabilitación multidisciplinarios aumentar la actividad y la participación de las personas con EM, pero no influyen en el nivel de deterioro. Debido a la escasez de estudios controlados aleatorios, existe evidencia limitada de la eficacia general de las disciplinas de terapia individual, aunque hay buena evidencia de que los enfoques específicos, como el ejercicio, terapias de psicología, en particular enfoques cognitivo-conductuales y la instrucción de conservación de energía son eficaces.
Los tratamientos alternativos
Muchas personas con EM utilizan la medicina complementaria y alternativa. En función de los tratamientos, la evidencia es débil o ausente. Ejemplos son un régimen dietético, la medicina herbal (incluyendo el uso de cannabis medicinal), oxigenación hiperbárica y la auto-infección con anquilostoma (conocida generalmente como terapia de helmintos). Terapia con helmintos de infección Trichuris suis óvulos está bajo investigación a partir de 2013, con los resultados esperados de un ensayo clínico en 2014. Los datos preliminares indican que puede ser seguro y clínicamente útil.
Pronóstico

sin datos <13 13-16 16-19 19-22 22-25 25-28 | 28-31 31-34 34-37 37-40 40-43 > 43 |
La pronóstico (el curso futuro esperado de la enfermedad) para una persona con esclerosis múltiple depende del subtipo de la enfermedad; sexo, la edad, y los síntomas iniciales de la persona; y el grado de incapacidad que experimenta la persona. Los evoluciona la enfermedad y los avances durante décadas, siendo 30 los años promedio a muerte desde el inicio.
El sexo femenino, el subtipo de recaída-remisión, neuritis óptica o síntomas sensoriales en inicio, unos ataques en los primeros años y la edad especialmente temprano en el inicio, se asocian con un mejor curso.
La la esperanza de vida de las personas con EM es de 5 a 10 años menor que la de las personas no afectadas. Casi el 40% de las personas con EM llegar a la séptima década de la vida. Sin embargo, dos tercios de las muertes en las personas con EM están directamente relacionados con las consecuencias de la enfermedad. El suicidio también tiene una prevalencia más alta que en la población sana, mientras que las infecciones y las complicaciones son especialmente peligrosos para los más discapacitados.
Aunque la mayoría de las personas pierden la capacidad de caminar antes de la muerte, el 90% son todavía capaces de caminar de forma independiente a los 10 años desde el inicio, y el 75% a los 15 años.
Epidemiología
Dos medidas principales se utilizan en estudios epidemiológicos: incidencia y prevalencia. La incidencia es el número de nuevos casos por unidad de tiempo-persona en situación de riesgo (por lo general el número de nuevos casos por mil personas-año); mientras prevalencia es el número total de casos de la enfermedad en la población en un momento dado. La prevalencia se sabe que no sólo dependerá de la incidencia, sino también en la tasa de supervivencia y las migraciones de las personas afectadas. MS tiene una prevalencia que oscila entre 2 y 150 por 100.000, dependiendo del país o población específica. Los estudios sobre los patrones poblacionales y geográficas de medidas epidemiológicas han sido muy común en la EM, y han dado lugar a la propuesta de diferente (causales) teorías etiológicas.
EM suele aparecer en adultos en sus treinta años, pero también puede aparecer en niños. El subtipo progresiva primaria es más común en las personas en sus cincuenta años. Al igual que con muchos trastornos autoinmunes, la enfermedad es más común en las mujeres, y la tendencia puede estar aumentando. La Datos de los CDC sugieren que la EM es tres veces más común en mujeres que en hombres en los Estados Unidos. En los niños, la diferencia la proporción de sexos es mayor, mientras que en las personas mayores de cincuenta años, la EM afecta a hombres y mujeres casi por igual.
Hay un gradiente norte-sur en el hemisferio norte y un gradiente de sur a norte en el hemisferio sur, con MS es mucho menos común en las personas que viven cerca del ecuador . El clima , la luz del sol y la ingesta de vitamina D han sido investigados como posibles causas de la enfermedad que podría explicar este gradiente de latitud. Sin embargo, hay excepciones importantes al patrón norte-sur y los cambios en las tasas de prevalencia en el tiempo; en general, esta tendencia puede ser desapareciendo. Esto indica que otros factores tales como el medio ambiente o la genética tienen que ser tomadas en cuenta para explicar el origen de la EM. MS también es más común en las regiones con poblaciones del norte de Europa. Pero incluso en regiones donde es común la EM, algunos grupos étnicos están en bajo riesgo de desarrollar la enfermedad, incluyendo la Samis, Turcomanos, Amerindios, Canadá Hutteritas, africanos y Nueva Zelanda Maoríes.
Los factores ambientales durante la infancia pueden desempeñar un papel importante en el desarrollo de MS más tarde en la vida. Varios estudios de los migrantes muestran que si se produce la migración antes de cumplir los 15, el migrante adquiere la susceptibilidad de la nueva región a la EM. Si la migración se lleva a cabo después de los 15 años, el migrante conserva la susceptibilidad de su país de origen. Sin embargo, el riesgo-edad geográfica para el desarrollo de la esclerosis múltiple puede abarcar un período de tiempo mayor. Una relación entre la temporada de nacimiento y MS también se ha encontrado que se presta apoyo a una asociación con la luz del sol y la vitamina D. Por ejemplo un menor número de personas con EM nacen en noviembre en comparación con mayo.
Historia
Descubrimiento médico
Los franceses neurólogo Jean-Martin Charcot (1825-1893) fue la primera persona en reconocer la esclerosis múltiple como una enfermedad distinta en 1868. Resumiendo los informes anteriores y añadiendo sus propias observaciones clínicas y patológicas, Charcot denomina esclerosan enfermedad en placas. Los tres signos de MS conocidos ahora como Charcot de triada 1 son nistagmo, temblor intencional, y habla telegráfica (discurso de exploración), aunque estos no son exclusivos de la EM. Charcot también observó cambios cognitivos, describiendo sus pacientes como teniendo un "marcado debilitamiento de la memoria" y "concepciones que se formaron poco a poco".
Antes de Charcot, Robert Carswell (1793-1857), un profesor británico de la patología , y Jean Cruveilhier (1791-1873), un profesor francés de la anatomía patológica, había descrito e ilustrado muchos de los detalles clínicos de la enfermedad, pero no lo identifican como una enfermedad aparte. Específicamente, Carswell describió las lesiones que encontró como "una notable lesión de la médula espinal acompañada con atrofia". Bajo el microscopio, patólogo suizo Georg Eduard Rindfleisch (1836-1908) señaló en 1863 que las lesiones asociados con la inflamación se distribuyeron alrededor de los vasos sanguíneos.
Después de la descripción de Charcot, Eugène Devic (1858-1930), Jozsef Balo (1895-1979), Paul Schilder (1886-1940), y Otto de Marburgo (1874-1948) describe casos especiales de la enfermedad. Durante todo el siglo 20 hubo un importante desarrollo en las teorías sobre la causa y la patogénesis de la esclerosis múltiple mientras que los tratamientos eficaces comenzaron a aparecer en 1990.
Los casos históricos
Hay varios relatos históricos de las personas que vivieron antes o poco después de la enfermedad fue descrita por Charcot y probablemente tenía EM.
Una joven llamada Halldora que vivía en Islandia hacia el año 1200 perdió de repente su visión y movilidad, pero, después de rezar a los santos, los recuperó siete días después. Santa Liduvina de Schiedam (1380-1433), un holandés monja , puede ser uno de los primeros pacientes con EM claramente identificables. Desde la edad de 16 años hasta su muerte a los 53 años, sufrió un dolor intermitente, debilidad de las piernas, y pérdida de la visión: los síntomas típicos de la EM. Ambos casos han dado lugar a la propuesta de una hipótesis "gen Vikingo 'para la difusión de la enfermedad.
Augustus Frederick d'Este (1794-1848), hijo de Augusto de Sussex y Lady Augusta Murray y el nieto de Jorge III del Reino Unido , es casi seguro que sufrían de esclerosis múltiple. D'Este dejó un diario detallado describiendo sus 22 años que viven con la enfermedad. Su diario se inició en 1822 y terminó en 1846, aunque se mantuvo desconocido hasta 1948. Sus síntomas comenzaron a los 28 años con una repentina pérdida transitoria visual ( amaurosis fugaz) después del funeral de un amigo. Durante el curso de su enfermedad, desarrolló debilidad de las piernas, torpeza de las manos, entumecimiento, mareos, trastornos de la vejiga, y la disfunción eréctil. En 1844, comenzó a usar una silla de ruedas. A pesar de su enfermedad, mantuvo una visión optimista de la vida.
Otra consideración a principios de la EM se mantuvo por el cronista británico WNP Barbellion, nom-de-plume de Bruce Frederick Cummings (1889-1919), que mantiene un registro detallado de su diagnóstico y lucha con EM. Su diario fue publicado en 1919 como El Diario de un hombre decepcionado .
Investigación
Terapias
Direcciones de investigación sobre tratamientos de la EM incluyen investigaciones de MS patogénesis y la heterogeneidad; la investigación de nuevos tratamientos más eficaces, convenientes o tolerables para la EMRR; creación de terapias para los subtipos progresivos; estrategias de neuroprotección; y la búsqueda de tratamientos sintomáticos eficaces. Un número de tratamientos que pueden reducir los ataques o mejorar la función están bajo investigación. Agentes emergentes para EMRR que habían mostrado prometedores en la fase 2 de ensayos antes de 2009 incluía alemtuzumab, daclizumab, rituximab, dirucotide, BHT-3009, la cladribina, fumarato de dimetilo, estriol, laquinimod, pegilado interferón-β-1a, minociclina, estatinas, temsirolimus y teriflunomida.
Desde MS se ha relacionado con la deficiencia de vitamina D se ha propuesto que la vitamina D podría ser utilizado para tratar la enfermedad. Los ensayos clínicos han sido escasos, de baja calidad y no han mostrado clara indicación de beneficio.
Si bien hay evidencia anecdótica de beneficio parabaja dosis naltrexona, sólo los resultados de un estudio piloto en la EM progresiva primaria se han publicado.
Biomarcadores de la enfermedad
La presentación clínica variable de la EM y la falta de pruebas de diagnóstico de laboratorio conducen a retrasos en el diagnóstico y la imposibilidad de predecir el diagnóstico. Nuevos métodos de diagnóstico están siendo investigados. Estos incluyen el trabajo con anti-mielina anticuerpos , análisis de microarrays de expresión génica y estudios con suero y líquido cefalorraquídeo, pero ninguno de ellos ha dado resultados positivos fiables.
De momento no se han establecido clínicamente investigaciones de laboratorio disponibles que pueden predecir el pronóstico. Sin embargo, se han propuesto varios enfoques prometedores. Las investigaciones sobre la predicción de la evolución se han centrado en el seguimiento de la actividad de la enfermedad. Biomarcadores de activación de la enfermedad incluyen la interleucina-6, el óxido nítrico y óxido nítrico sintasa, la osteopontina y fetuina-A. Por otra parte desde progresión de la enfermedad es el resultado de la neurodegeneración las funciones de las proteínas indicativas de neuronal, axonal, y pérdida glial como neurofilamentos, tau y N-acetil aspartato están bajo investigación.
Un campo de investigación final es el trabajo con los biomarcadores que distinguen entre los respondedores y no respondedores medicación.
Insuficiencia venosa cerebroespinal crónica
En 2008, cirujano vascular italiano Paolo Zamboni informó investigaciones que sugieren que la EM implica un proceso de la enfermedad vascular se refirió como la insuficiencia venosa cerebroespinal crónica (CCSVI, CCVI), en la que las venas del cerebro se contraen. Encontró CCSVI en la mayoría de las personas con EM, realizó un procedimiento quirúrgico para corregir y afirmó que el 73% de la gente mejoró. Se ha expresado preocupación con la investigación de Zamboni, ya que no era ni estudios cegados ni controladas y otras han tenido resultados variables. Esto ha planteado serias objeciones a la hipótesis de CCSVI origina la esclerosis múltiple. La comunidad de la neurología recomienda actualmente no utilizar el tratamiento propuesto a menos que su eficacia es confirmada por estudios controlados, cuya necesidad ha sido reconocida por los organismos científicos dedicados a la investigación de MS.