
Doença falciforme
Você sabia ...
Crianças SOS, que corre cerca de 200 sos escolas no mundo em desenvolvimento, organizado esta selecção. Para comparar instituições de caridade de patrocínio esta é a melhor ligação de patrocínio .
| Doença falciforme | |
|---|---|
| Classificação e recursos externos | |
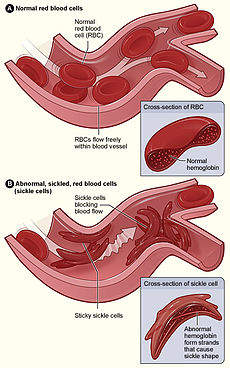 Figura (A) mostra células normais do sangue vermelho que flui livremente através das veias. A inserção mostra uma secção transversal de uma célula de sangue vermelho normal com hemoglobina normal. Figura B mostra, glóbulos vermelhos falciformes anormais log empastelamento, furando e acumulando no ponto de ramificação em uma veia. A imagem ampliada mostra uma secção transversal de uma célula falciforme com longas cadeias polimerizados HbS e alongamento distorcer a forma da célula. | |
| CID- 10 | D 57 |
| CID- 9 | 282,6 |
| OMIM | 603903 |
| DiseasesDB | 12069 |
| MedlinePlus | 000527 |
| Medcenter | med / 2126 oph / 490 ped / 2096 emerg / 26 emerg / 406 |
| MeSH | C15.378.071.141.150.150 |
| GeneReviews |
|
A drepanocitose (SCD), ou anemia falciforme (AF) ou drepanocitose, é uma autossômica recessivo genético doença do sangue com sobredominância, caracterizado por Os glóbulos vermelhos que assumem um anormal, rígida, forma de foice. Afoiçamento diminui a flexibilidade e os resultados das células em risco de várias complicações. O afoiçamento ocorre devido a uma mutação no hemoglobina gene. A expectativa de vida é encurtado. Em 1994, os EUA, a expectativa média de vida de pessoas com essa condição foi estimada em 42 anos no sexo masculino e 48 anos em mulheres, mas hoje, graças a uma melhor gestão da doença, os pacientes podem viver até os 50 anos ou mais.
Doença falciforme ocorre mais comumente em pessoas (ou seus descendentes) a partir de partes do tropical e sub-tropical regiões Subsaariana, onde a malária é ou foi comum. Em áreas onde a malária é comum, há uma benefício de fitness em portadores de apenas um gene falciforme única ( traço falciforme). Aqueles com apenas um dos dois alelos da doença falciforme, embora não totalmente resistentes, são mais tolerantes à infecção e, portanto, mostram sintomas menos graves quando infectados.
A anemia falciforme é o nome de uma forma específica de drepanocitose em que há homozigotia para o mutação que causa a HbS. A anemia falciforme é também referido como "HbSS", "doença SS", "hemoglobina S" ou permutações das mesmas. Em pessoas heterozigotas, que têm apenas um gene da anemia falciforme e um gene normal para adultos hemoglobina, que é referido como "HbAS" ou "traço falciforme". Outras formas mais raras, de anemia falciforme incluem foice doença de hemoglobina C (HbSC), foice beta-plus- talassemia (HbS / β +) e foice beta-talassemia zero (HbS / β 0). Estas outras formas de doença falciforme são estados heterozigotos compostos em que a pessoa tem apenas uma cópia da mutação que causa a HbS e uma cópia de outro anormal hemoglobina alelo.
O termo doença é aplicada, porque a anormalidade herdada provoca uma condição patológica que pode conduzir a complicações graves e morte. Nem todas as variantes herdadas de hemoglobina são prejudiciais, um conceito conhecido como polimorfismo genético.
Os sinais e sintomas

Doença falciforme pode levar a várias complicações agudas e crônicas, vários dos quais têm uma alta taxa de mortalidade.
Crise de células falciformes
O termo "crise de células falciformes" é usado para descrever várias condições agudas independentes que ocorrem em pacientes com doença falciforme. A doença falciforme resulta em anemia e crises que poderão ser de vários tipos, incluindo a crise vaso-oclusiva, crise aplástica, Crise de seqüestro, crise hemolítica e outros. A maioria dos episódios de crises de células falciformes duram entre cinco e sete dias. "Embora a infecção, a desidratação, acidose e (todos os quais favorecem falcização) pode agir como gatilhos, na maioria dos casos não causa predisposição seja identificado."
Crise vaso-oclusiva
O crise vaso-oclusiva é causada por células vermelhas do sangue em forma de foice que obstruem capilares e restringir o fluxo de sangue a um órgão, resultando em isquemia, dor, necrose e muitas vezes danos nos órgãos. A frequência, gravidade e duração destas crises variam consideravelmente. Crises dolorosas são tratados com hidratação, analgésicos e transfusão de sangue; manejo da dor requer administração de opióides em intervalos regulares até que a crise se instalou. Para crises mais leves, um subgrupo de pacientes em gerenciar AINEs (tal como diclofenac ou naproxeno). Para as crises mais graves, a maioria dos pacientes requerem uma gestão hospitalar para opióides por via venosa; dispositivos de analgesia (PCA) controlada pelo paciente são comumente usados neste cenário. Crise vaso-oclusiva envolvendo órgãos como o pênis ou pulmões são considerados uma emergência e tratada com transfusões de glóbulos vermelhos do sangue. Difenidramina é, por vezes, eficazes para o prurido associado com o uso de opióides. Espirometria incentivo, uma técnica para encorajar a respiração profunda para minimizar o desenvolvimento de atelectasia, é recomendado.
Crise de seqüestro esplênico
Por causa de suas embarcações estreitas e função de limpeza dos glóbulos vermelhos defeituosos, os baço é freqüentemente afetada. É geralmente enfartada antes do final da infância em indivíduos que sofrem de anemia falciforme. Este autoesplenectomia aumenta o risco de infecção a partir de organismos encapsulados; antibióticos e vacinas preventivas são recomendadas para aqueles com tal asplenia.
- Crises sequestro esplênico: são ampliações agudas, dolorosas do baço, causada pelo aprisionamento interna do baço de células vermelhas e resultando em uma queda abrupta dos níveis de hemoglobina com o potencial de choque hipovolêmico. Crises de seqüestro são considerados uma emergência. Se não for tratada, os pacientes podem morrer dentro de 1-2 horas devido à insuficiência circulatória. Gestão é de suporte, às vezes com transfusão de sangue. Essas crises são transitórios, eles continuam por 3-4 horas e pode durar por um dia.
Crise aplástica
Crise aplástica são agravamentos agudos de anemia basais do doente, produzindo palidez, taquicardia, e fadiga. Esta crise é normalmente desencadeada por parvovírus B19, o que afeta diretamente eritropoiese (produção de células vermelhas do sangue) ao invadir os precursores das células vermelhas e multiplicando neles e destruindo-as. A infecção pelo parvovírus quase impede completamente a produção de células vermelhas do sangue de dois a três dias. Em indivíduos normais, este é de pouca importância, mas a vida dos glóbulos vermelhos reduzido de pacientes falciformes resulta em, uma situação de risco de vida abrupta. Contagens de reticulócitos cair drasticamente durante a doença (causando reticulocitopénia), e a rápida renovação das células vermelhas leva à queda na hemoglobina. Esta crise leva 4 dias a uma semana a desaparecer. A maioria dos doentes podem ser controlados supportively; alguns precisam de transfusão de sangue.
Crise hemolítica
Crises hemolíticas são gotas acelerados agudas no nível de hemoglobina. As células vermelhas do sangue quebrar a uma taxa mais rápida. Isto é particularmente comum em pacientes com co-existente Deficiência de G6PD. Gestão é de suporte, às vezes com transfusões de sangue.
Outro
Uma das primeiras manifestações clínicas é dactylitis, apresentando assim que seis meses de idade, e podem ocorrer em crianças com traço falciforme. A crise pode durar até um mês. Outro tipo reconhecido de crise falciforme é a síndrome torácica aguda, uma condição caracterizada por febre, dor no peito, dificuldade em respirar, e infiltrado pulmonar em um peito X-ray. Dado que a pneumonia e falcização no pulmão podem produzir estes sintomas, o paciente é tratado para ambas as condições. Ela pode ser desencadeada por uma crise dolorosa, infecção respiratória, embolização de medula óssea, ou, eventualmente, por atelectasia, a administração de opiáceos, ou cirurgia.
Complicações
A anemia falciforme pode levar a várias complicações, incluindo:
- Pós esmagadora (automático) infecção esplenectomia (IFPE), que é devido a asplenia funcional, causada por organismos encapsulados, tais como Streptococcus pneumoniae e Haemophilus influenzae. Diariamente penicilina profilaxia é o tratamento mais comumente utilizado durante a infância, com algumas haematologists continuar o tratamento indefinidamente. Os pacientes se beneficiam hoje de vacinação de rotina para H. influenzae, S. pneumoniae, e Neisseria meningitidis.
- Acidente vascular cerebral , o que pode resultar de um progressivo estreitamento de vasos sanguíneos, evitando que o oxigénio alcance o cérebro. Enfarte cerebral ocorre em crianças e em adultos hemorragia cerebral.
- AVC silencioso é um acidente vascular cerebral que não causa sintomas imediatos, mas está associado com danos ao cérebro. Acidente vascular cerebral em silêncio é, provavelmente, cinco vezes mais comuns como acidente vascular cerebral sintomática. Aproximadamente 10-15% das crianças com doença falciforme sofrer acidentes vasculares cerebrais, com cursos silenciosos predominando nos pacientes mais jovens.
- Colelitíase (cálculos biliares) e colecistite, que pode resultar de excessiva produção de bilirrubina e precipitação devido à prolongada hemólise.
- A necrose avascular ( asséptica necrose óssea) do quadril e outras articulações grandes, o que pode ocorrer como resultado de isquemia.
- Diminuição reações imunes devido a hipoesplenismo (mau funcionamento do baço).
- Priapismo e infarto do pênis.
- Osteomielite (infecção bacteriana óssea); a causa mais comum de osteomielite na doença falciforme é Salmonella (especialmente o sorotipos não típico Salmonella typhimurium, Salmonella enteritidis, Salmonella choleraesuis e Salmonella paratyphi B), seguido por Staphylococcus aureus e bacilos entéricos Gram-negativos talvez porque afoiçamento intravascular do intestino leva a infarto isquêmico desigual.
- Tolerância a opiáceos, que pode ocorrer como uma resposta normal, fisiológico para o uso terapêutico de opiáceos. Dependência de opiáceos ocorre mais comumente entre os indivíduos com doença falciforme do que entre os outros indivíduos tratados com opiáceos por outras razões.
- Necrose papilar aguda nos rins.
- Úlceras de perna.
- Nos olhos, retinopatia de fundo, retinopatia proliferativa, hemorragias vítreas e descolamento de retina, resultando em cegueira. Verificações de olho anuais regulares são recomendados.
- Durante a gravidez, retardo do crescimento intrauterino, espontâneo aborto, e pré-eclâmpsia.
- A dor crônica: Mesmo na ausência de dor vaso-oclusiva aguda, muitos pacientes têm dor crônica que não é relatado.
- A hipertensão pulmonar (aumento da pressão sobre o artéria pulmonar), levando a tensão sobre o ventrículo direito e um risco de insuficiência cardíaca; Os sintomas típicos são falta de ar, diminuição da tolerância ao exercício e episódios de síncope.
- Crônico insuficiência renal devido à Falciforme nefropatia manifesta-se com hipertensão (pressão arterial alta), proteinúria (perda de proteína na urina), hematúria (perda de células vermelhas do sangue na urina) e piora a anemia. Se ele progride para a fase final da insuficiência renal, ele carrega um prognóstico pobre.
Heterozigotos
O formulário de heterozigotos ( traço falciforme) é quase sempre assintomática, ea única manifestação significativa usual é o defeito de concentração renal apresenta com isostenúria.
Fisiopatologia
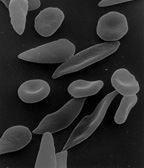
A anemia falciforme é causada por um mutação de ponto na cadeia de globina β- hemoglobina, fazendo com que o aminoácido hidrofílico ácido glutâmico, para ser substituído pelo aminoácido hidrofóbico valina na sexta posição. O gene da globina β é encontrado em cromossoma 11. A associação de dois subunidades de tipo selvagem α-globina com duas subunidades-globina β mutantes forma hemoglobina S (HbS). Sob condições de baixa oxigenação (sendo a alta altitude, por exemplo), a ausência de um aminoácido polar na posição seis da cadeia β-globina promove a polimerização não covalente (agregação) de hemoglobina, o que distorce as células vermelhas do sangue numa forma de foice e diminui a sua elasticidade.
A perda de elasticidade células vermelhas do sangue é fundamental para a fisiopatologia da doença falciforme. Os glóbulos vermelhos normais são bastante elástico, que permite que as células se deforme para passar através dos capilares. Na doença falciforme, a tensão baixa concentração de oxigênio promove afoiçamento de glóbulos vermelhos e episódios repetidos de afoiçamento danificar a membrana celular e diminuir a elasticidade da célula. Estas células não conseguem retornar à forma normal quando a tensão de oxigênio normal é restaurado. Como consequência, estas células sanguíneas rígidas são incapazes de deformar-se à medida que passam através dos capilares estreitos, levando a oclusão do vaso e isquemia.
A anemia real da doença é causada pela A hemólise, a destruição das células vermelhas, por causa da sua misshape. Apesar de medula óssea tenta compensar através da criação de novas células vermelhas, ele não coincidir com a taxa de destruição. Glóbulos vermelhos saudáveis vivem tipicamente 90-120 dias, mas as células falciformes só sobrevivem 10-20 dias.
Normalmente, os seres humanos têm hemoglobina A, que consiste em duas cadeias alfa e duas beta, hemoglobina A2, a qual consiste de duas cadeias alfa e duas delta e Hemoglobina F, que consiste de duas alfa e duas cadeias gama nos seus corpos. Destes, Hemoglobina A faz-se em torno de 96-97% da hemoglobina normal em humanos.
Genética
Mutação do gene falciforme provavelmente surgiu espontaneamente em diferentes áreas geográficas, como sugerido por análise de restrição de endonuclease. Essas variantes são conhecidos como Camarões, Senegal, Benin, Bantu e Arábia-asiático. Suas nascentes de importância clínica do fato de que alguns deles estão associados a níveis mais elevados de HbF, por exemplo, Senegal e variantes Arábia-asiáticas, e tendem a ter doença mais branda.
Em pessoas heterozigotos para HgbS ( portadores de afoiçamento hemoglobina), os problemas de polimerização são menores, porque o normal, alelo é capaz de produzir mais de 50% da hemoglobina. Em pessoas homozigóticos para HgbS, a presença de polímeros de cadeia longa de HbS distorcer a forma da célula vermelha de sangue a partir de uma suave forma de rosca-como a irregular e cheio de espinhos, tornando-se frágil e suscetível a quebra dentro capilares. Operadoras têm sintomas apenas se eles são privadas de oxigênio (por exemplo, ao escalar uma montanha) ou enquanto severamente desidratado. A anemia falciforme ocorre quando o sétimo aminoácido (se a metionina inicial é contado), ácido glutâmico, é substituído por valina para alterar a sua estrutura e função. Valina é hidrofóbico, fazendo com que a hemoglobina a colapsar sobre si mesmo, de vez em quando. A estrutura não é alterado de outro modo. Quando a hemoglobina suficiente colapsa em si mesma os glóbulos vermelhos tornam-se em forma de foice.

O defeito genético é um conhecido mutação de uma única nucleotídeo (veja único polimorfismo de nucleótidos - SNP) (A para T) do gene da globina β, o que resulta em ácido glutâmico substituído por valina na posição 6. A hemoglobina S com esta mutação é referida como a HbS, ao contrário do adulto normal HbA. A doença genética é devido ao mutação de um único nucleótido, a partir de um CTC CAC codão na estrutura helicoidal da matriz, o que é transcrita em um codão GUG. Isto é normalmente uma mutação benigna, sem causar efeitos aparentes sobre a secundário, terciário, ou estrutura quaternária da hemoglobina em condições normais de oxigênio concentração. O que ele permite, em condições de baixo oxigênio concentração, é o polimerização da HbS em si. A forma desoxi da hemoglobina expõe um adesivo hidrofóbico na proteína entre as hélices E e F. Os resíduos hidrofóbicos da valina na posição 6 da cadeia beta da hemoglobina é capaz de associar-se com o adesivo hidrofóbico, fazendo com que as moléculas de hemoglobina S para agregar e formar precipitados fibrosos.
O alelo responsável pela anemia falciforme é autossômica recessivo e pode ser encontrado no braço curto do cromossomo 11. A pessoa que recebe o gene defeituoso de ambos, pai e mãe desenvolve a doença; uma pessoa que recebe um defeituoso e de um alelo saudável permanece saudável, mas pode transmitir a doença e é conhecido como um transportadora. Se os dois pais que são portadores ter um filho, há uma chance de 1 em 4 de seu filho desenvolver a doença e uma chance de 1 em 2 de seu filho ser apenas um portador. Uma vez que o gene recessivo é incompleta, as operadoras podem produzir alguns glóbulos vermelhos falciformes, não o suficiente para causar sintomas, mas o suficiente para dar resistência à malária. Esta não confere imunidade total à malária; heterozigotos ainda são capazes de contrair malária, mas seus sintomas são geralmente menos grave. Devido a isso, os heterozigotos têm uma maior aptidão do que qualquer um dos homozigotos. Isto é conhecido como vantagem heterozigoto.
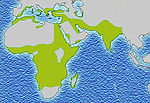
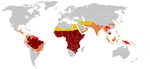
Devido à vantagem adaptativa do heterozigoto, a doença ainda é prevalente, especialmente entre as pessoas com ascendência recente em áreas atingidas pela malária, como a África , o Mediterrâneo , a Índia eo Oriente Médio . A malária era endêmica, historicamente, para o sul da Europa, mas foi declarada erradicada em meados do século 20, com a exceção de raros casos esporádicos.
O parasita da malária tem um ciclo de vida complexo e passa parte do que nas células vermelhas do sangue. Em um transportador, a presença do parasita da malária faz com que as células vermelhas do sangue de hemoglobina com defeito à ruptura prematuramente, fazendo com que o plasmodium incapazes de se reproduzir. Além disso, a polimerização da Hb afecta a capacidade do parasita para digerir Hb em primeiro lugar. Portanto, em áreas onde a malária é um problema, as chances de sobrevivência das pessoas realmente aumentar se eles carregam traço falciforme (seleção da heterozigoto).
No EUA , onde não há malária endémica, a prevalência de anemia falciforme entre negros é menor (cerca de 0,25%) do que na África Ocidental (cerca de 4,0%) e está caindo. Sem malária endêmica, a mutação falciforme é puramente desvantajoso e tenderá a ser selecionado para fora da população afetada via seleção natural . No entanto, a comunidade americana Africano do EUA é conhecido por ser o resultado da mistura significativa entre vários grupos étnicos africanos e não-africanos, e também representa os descendentes dos sobreviventes da escravidão eo tráfico de escravos. Assim, um menor grau de endogamia e, em particular, a pressão anormalmente alta de saúde seletivo através da escravidão podem ser as explicações mais plausíveis para a menor prevalência de anemia falciforme (e, possivelmente, outras doenças genéticas) entre os afro-americanos em comparação com Sub -Saharan africanos. Outro fator limitante a disseminação de genes de células falciformes na América do Norte é a ausência de tendências culturais a poligamia, o que permite que homens afetados a continuar a procurar as crianças não afetadas com múltiplos parceiros.

Herança
Condições falciformes são herdadas dos pais da mesma maneira como tipo sanguíneo, cor e textura do cabelo, cor dos olhos, e outros traços físicos. Os tipos de hemoglobina que uma pessoa faz nas células vermelhas do sangue depende do que genes de hemoglobina são herdadas de seus pais. Se um dos pais tem anemia falciforme (SS) eo outro tem traço falciforme, então há uma chance de 50% de ter a doença falciforme de uma criança e 50% de chance de ter traço falciforme de uma criança. Quando ambos os pais têm o traço falciforme uma criança tem uma chance de 25% de doença falciforme, como mostrado no diagrama.
Diagnóstico
Em HBSS, a hemograma completo revela os níveis de hemoglobina no intervalo de 6-8 g / dL com um elevado contagem de reticulócitos (como a medula óssea compensa a destruição de células falciformes, produzindo mais glóbulos vermelhos). Em outras formas de doença de células falciformes, níveis de hemoglobina tendem a ser mais elevado. A película de sangue pode mostrar características de hipoesplenismo ( células alvo e Howell-Jolly corpos).
Falcização das células vermelhas do sangue, por uma película de sangue, pode ser induzida pela adição de metabissulfito de sódio. A presença de hemoglobina falciforme também pode ser demonstrada com o "teste de solubilidade foice". Uma mistura da hemoglobina S (HbS), em uma solução de redutor (tal como ditionito de sódio) dá uma aparência turva, enquanto que a Hb normal, dá uma solução clara.
Anormal formas de hemoglobina pode ser detectada em eletroforese de hemoglobina, uma forma de electroforese em gel em que os vários tipos de hemoglobina mover-se a velocidades variáveis. Hemoglobina falciforme (HgbS) e hemoglobina C com afoiçamento (HgbSC) -as duas mais comuns formas-pode ser identificado a partir daí. O diagnóstico pode ser confirmado com cromatografia líquida de alto desempenho (HPLC). Os testes genéticos raramente é realizada, como outras investigações são altamente específicos para HbS e HbC.
Uma crise falciforme aguda é frequentemente precipitada por infecção. Por conseguinte, um exame de urina para detectar uma infecção do trato urinário oculto, e radiografia de tórax para procurar pneumonia oculta deve ser realizada rotineiramente.
As pessoas que são conhecidos portadores da doença são freqüentemente submetidos a aconselhamento genético antes de ter um filho. Um teste para ver se uma criança por nascer tem a doença leva qualquer um sangue amostra do feto ou uma amostra de líquido amniótico. Uma vez tomando uma amostra de sangue a partir de um feto tem maiores riscos, o último teste é geralmente utilizado.
Após a mutação responsável por esta doença foi descoberto em 1979, o Força Aérea dos EUA necessário candidatos negros para testar a mutação. Ele descartou 143 candidatos porque eles eram portadores, embora nenhum deles tinha a doença. Ele acabou por retirar a exigência, mas só depois de um estagiário entrou com uma ação.
Gestão
O ácido fólico e penicilina
As crianças que nascem com doença falciforme serão submetidos a observação atenta pelo pediatra e exigirá a gestão por um hematologista para garantir que eles permaneçam saudáveis. Esses pacientes vão tomar uma dose de 1 mg de ácido fólico por dia para toda a vida. Do nascimento aos cinco anos de idade, eles também terá que tomar penicilina diariamente devido ao sistema imunológico imaturo que os torna mais propensos a doenças da primeira infância.
Quimioprofilaxia da malária
O efeito protetor do traço falciforme não se aplica a pessoas com doença falciforme; na verdade, eles são excepcionalmente vulneráveis à malária, uma vez que a causa mais comum de crises dolorosas em países malária é a infecção com malária. Por conseguinte, foi recomendado que as pessoas com doença falciforme que vivem em países de malária devem receber quimioprofilaxia anti-malária para a vida.
Crise vaso-oclusiva
A maioria das pessoas com doença falciforme têm episódios intensamente dolorosas chamado crises vaso-oclusivas. A frequência, gravidade e duração destas crises, no entanto, variam enormemente. Crises dolorosas são tratados sintomaticamente com analgésicos ; manejo da dor requer administração de opióides em intervalos regulares até que a crise se instalou. Para crises mais leves, um subgrupo de pacientes em gerenciar AINEs (tal como diclofenac ou naproxeno). Para as crises mais graves, a maioria dos pacientes requerem uma gestão hospitalar para opióides por via venosa; dispositivos de analgesia (PCA) controlada pelo paciente são comumente usados neste cenário. Difenidramina é também um agente eficaz que é frequentemente prescrita pelos médicos, a fim de ajudar a controlar qualquer prurido associado com o uso de opióides.
Crise torácica aguda
A administração é semelhante a crise vaso-oclusiva, com a adição de antibióticos (geralmente uma quinolona ou macrólido, uma vez ["atípicos"] bactérias são pensados para contribuir para a síndrome da parede celular deficiente), suplemento de oxigénio para hipóxia, e observação rigorosa. Caso o infiltrado pulmonar piorar ou a requisitos de aumento de oxigênio, simples transfusão de sangue ou transfusão de troca é indicado. Este último envolve a troca de uma porção significativa de pacientes com a massa de glóbulos vermelhos para glóbulos vermelhos normais, o que diminui a percentagem de hemoglobina S no sangue do paciente.
Hidroxiureia
A primeira droga aprovada para o tratamento causal da anemia falciforme, hidroxiureia, foi mostrado para reduzir o número e gravidade dos ataques de um estudo em 1995 (Charache et ai.) e mostrou-se, eventualmente, aumentar o tempo de sobrevivência de um estudo em 2003 (Steinberg et al.). Isto é conseguido, em parte, pela reactivação a produção de hemoglobina fetal em lugar da hemoglobina S que provoca anemia das células falciformes. A hidroxiureia foi previamente utilizado como um agente de quimioterapia, e existe alguma preocupação de que o uso a longo prazo pode ser prejudicial, mas este risco tenha sido mostrado para ser nula ou muito pequena, e é provável que os benefícios são superiores aos riscos.
Terapia transfusional
Transfusões de sangue são frequentemente utilizados no tratamento da doença das células falciformes, em casos agudos e para prevenir complicações através da diminuição do número de glóbulos vermelhos (RBC) que podem foice por adição de glóbulos vermelhos normais. Em crianças de glóbulos vermelhos profilático crônica (RBC) terapia de transfusão tem sido mostrado para ser eficaz em certa medida, na redução do risco de acidente vascular cerebral ou acidente vascular cerebral primeira silenciosa quando Doppler transcraniano (DTC) ultra-sonografia mostra um aumento da velocidade do fluxo sanguíneo cerebral anormal. Em aqueles que tenham sofrido um AVC antes também reduz o risco de AVC recorrente e acidentes vasculares cerebrais silenciosas adicionais.
Transplantes de medula óssea
Transplantes de medula óssea têm provado ser eficaz em crianças. Transplantes de medula óssea é a única cura conhecida para SCD.
Prognóstico
Cerca de 90% dos pacientes sobrevivem até 20 anos de idade, e perto de 50% sobrevivem além do quinto decade.In 2001, de acordo com um estudo, a sobrevivência média estimada para pacientes com anemia falciforme era 53 anos para os homens e 58 anos para as mulheres com SCD homozigótica.
Epidemiologia
A maior freqüência de doença falciforme é encontrado em regiões tropicais, particularmente a África subsaariana, Índia e Médio Oriente. Migração das populações substanciais dessas áreas de alta prevalência para países com baixa prevalência na Europa aumentou drasticamente nas últimas décadas e, em alguns países europeus doença falciforme já ultrapassou condições genéticas mais conhecidas, como hemofilia e fibrose cística .
África
Três quartos dos casos falciformes ocorrem em África. Uma recente da OMS relatório estimou que cerca de 2% dos recém-nascidos na Nigéria foram afetados pela anemia falciforme, dando um total de 150.000 crianças afetadas que nascem a cada ano na Nigéria sozinho. A frequência portadora varia entre 10% e 40% em toda a África equatorial, diminuindo para 1-2%, na costa norte Africano e <1% na África do Sul.
Estados Unidos
O prevalência da doença no Estados Unidos é de aproximadamente 1 em 5000, afetando principalmente os americanos de ascendência Africano Sub-Sahariana, de acordo com o National Institutes of Health. Nos Estados Unidos, cerca de 1 em 500 crianças Africano-americanos e 1: 36.000 crianças hispano-americanos nascidos terá anemia falciforme. Estima-se que a doença Falciforme (SCD) afeta 90.000 americanos. A maioria das crianças com anemia falciforme nascidas nos Estados Unidos são agora identificados por triagem neonatal de rotina. Quarenta e quatro estados, juntamente com o Distrito de Columbia, Porto Rico e as Ilhas Virgens fornecem actualmente a triagem neonatal universal para SCD. Traço falciforme ocorre entre cerca de 01:12 afro-americanos e 1: 100 hispano-americanos. Estima-se que 2,5 milhões de americanos são portadores heterozigotos para o traço falciforme.
França
Na Europa , uma elevada prevalência da doença foi observado em França . Como resultado do crescimento da população em regiões Africano-caribenhos de ultramarino da França, e agora imigração essencialmente do Norte e África sub-saariana para França continental, doença falciforme tem se tornado um problema de saúde na França. SCD se tornou a doença genética mais comum neste país, com uma prevalência de natalidade global de 1 / 2.415 na França continental, à frente de fenilcetonúria (1 / 10.862), congênita hipotireoidismo (1 / 3.132), congênita hiperplasia adrenal (1 / 19.008) e fibrose cística (1 / 5.014) para o mesmo período de referência. Em 2010, 31,5% de todos os recém-nascidos na França continental (253.466 de 805.958) tiveram os pais originou a partir de uma região definida "em risco" (principalmente a África e os departamentos e territórios ultramarinos da França) e foram selecionados para SCD. 341 recém-nascidos com anemia falciforme e 8744 portadores heterozigotos foram encontrados representando 1,1% de todos os recém-nascidos na França continental. O distrito de Paris metropolitana ( Île-de-France) é a região que representa a maior número de pessoas em presumivelmente maior risco de SCD. De fato, 60% de todos os recém-nascidos nesta área em 2010 tinham pais originado de uma região definida como "em risco" e foram selecionados para SCD. O segundo maior número de situação de risco está em Provence-Alpes-Côte d'Azur em cerca de 43,2% eo número mais baixo é em Brittany em 5,5%. Esta percentagem foi de 19% em 2000 e aumentou em 65%.
Reino Unido
No Reino Unido, um bebê em cada 2.000 nasce com essa condição.
Oriente Médio
Na Arábia Saudita cerca de 4,2% da população é portadora do traço falciforme e 0,26% têm a doença falciforme. A maior prevalência na província Oriental, onde aproximadamente 17% da população são portadores do gene e 1,2% têm a doença falciforme. Em 2005, na Arábia Saudita, foi lançado um teste pré-marital obrigatória incluindo HB eletroforese e teve como objetivo diminuir a incidência de SCD e talassemia.
Índia
A doença falciforme é prevalente em muitas partes da Índia, onde a prevalência variou 9,4-22,2% em áreas endêmicas.
História
Esta coleção de achados clínicos era desconhecida até a explicação das células falciformes em 1910 pelo cardiologista Chicago e professor de medicina James B. Herrick (1861-1954), cujo estagiário Ernest Edward Irons (1877-1959) encontraram células "peculiares alongados e em forma de foice" no sangue de Walter Clement Noel, a 20-year-old primeiro ano estudante de odontologia de Granada, depois de Noel foi internado no Hospital Presbiteriano em Chicago dezembro 1904 sofrendo de anemia .
Noel foi readmitido várias vezes ao longo dos próximos três anos para "reumatismo muscular" e "ataques" bilioso. Noel completou seus estudos e voltou para a capital de Grenada (de St. George) para a prática odontologia. Ele morreu de pneumonia em 1916 e está enterrado no cemitério católico de Sauteurs no norte de Granada. Relato publicado de Herrick incluído ilustrações, mas o mais adiantado de slides disponíveis mostrando células falciformes é a de uma autópsia 1918 a partir de um soldado com traço falciforme, inicialmente avaliação apenas 92 anos mais tarde.
A doença foi chamada "anemia falciforme" pela Verne Mason em 1922, em seguida, um médico residente em Johns Hopkins Hospital. No entanto, alguns elementos da doença tinha sido reconhecido anteriormente: Um papel no Jornal de Medicina Farmacologia Southern em 1846 descreveu a ausência de um baço no autópsia de um escravo fugitivo. A literatura médica Africano relataram essa condição na década de 1870, quando era conhecido localmente como ogbanjes ("crianças que vêm e vão") por causa da elevada taxa de mortalidade infantil causada por esta condição. A história da condição rastreados relatórios de volta a 1670 em uma família de Gana.
Pauling e colegas foram os primeiros, em 1949, para demonstrar que a drepanocitose ocorre como um resultado de uma alteração na molécula de hemoglobina. Esta foi a primeira vez que uma doença genética foi ligado a uma mutação de uma proteína específica, um marco na história de biologia molecular, que foi publicado no seu artigo " Anemia Falciforme, uma doença molecular ".

