
Ácido fórmico
Acerca de este escuelas selección Wikipedia
SOS ofrecen una descarga completa de esta selección para las escuelas para su uso en escuelas intranets. patrocinio SOS Niño es cool!
| Ácido fórmico | |
|---|---|
 |  |
Ácido metanoico | |
Otros nombres Ácido carboxílico Hidrógeno | |
| Identificadores | |
| CAS | 64-18-6 |
| Número RTECS | LQ4900000 |
| Imágenes-Jmol 3D | Image 1 |
SONRISAS
| |
| Propiedades | |
| Fórmula molecular | CH 2 O 2 HCOOH |
| Masa molar | 46,0254 g / mol |
| Apariencia | Incoloro, líquido fumante |
| Densidad | 1,22 g / ml, líquido |
| Punto de fusion | 8,4 ° C (47,1 ° F) |
| Punto de ebullicion | 100.8 ° C (213,3 ° F) |
| Solubilidad en agua | Miscible |
| Acidez (p K a) | 3,744 |
| Viscosidad | 1.57 c P a 26 ° C |
| Estructura | |
| Forma molecular | Planar |
| Momento bipolar | 1.41 D (gas) |
| Peligros | |
| MSDS | MSDS externa |
| Frases R | R10, R35 |
| Frases S | (S1 / 2), S23, S26, S45 |
| Principal peligros | Corrosivo; irritante; sensibilizador. |
| NFPA 704 |  2 3 0 |
| Punto de inflamabilidad | 69 ° C (156 ° F) |
| Compuestos relacionados | |
| Relacionados ácidos carboxílicos | Ácido acético El ácido propiónico |
| Compuestos relacionados | Formaldehído El metanol |
| Página de datos complementaria | |
| Estructura y propiedades | n, ε r, etc. |
| Termodinámica datos | Comportamiento de fase Sólido, líquido, gas |
| Los datos espectrales | UV, IR, RMN , MS |
| Excepto cuando se indique lo contrario, los datos se den materiales en su condiciones normales (25 ° C, 100 kPa) | |
| Exenciones y referencias | |
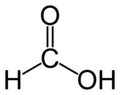
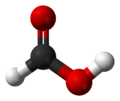
El ácido fórmico (llamado sistemáticamente ácido metanoico) es el más simple de ácido carboxílico . Su fórmula es H C O OH o CH 2 O 2. Es un importante en el Intermedio síntesis química y se produce naturalmente, lo más notablemente en el veneno de abeja y la hormiga picaduras.
En la naturaleza , se encuentra en el picaduras y picaduras de muchos insectos del orden Hymenoptera , principalmente hormigas . Es también un significativo producto de la combustión resultante de combustible alternativo vehículos incendiados metanol (y etanol , si se contaminan con agua ) cuando se mezcla con gasolina. Su nombre proviene del latín palabra hormiga, formica, en referencia a su temprana aislamiento por la destilación de los cuerpos de hormigas. Un compuesto químico tal como una sal de la neutralización del ácido fórmico con una base, o una éster derivado de ácido fórmico, se conoce como formiato (o metanoato). El formiato de iones tiene la fórmula HCOO -.
Propiedades
El ácido fórmico es miscible con el agua y la mayoría polares orgánicos disolventes , y algo soluble en hidrocarburos. En hidrocarburos y, en la fase de vapor, que en realidad consiste en dímeros con enlaces de hidrógeno en lugar de moléculas individuales. En la fase de gas, resultados de este enlace de hidrógeno en las desviaciones graves de la ley de los gases ideales. Ácido fórmico líquidos y sólidos consiste en una red de manera efectiva sin fin de moléculas de ácido fórmico con enlaces de hidrógeno.
Acciones ácido fórmico de la mayoría de las propiedades químicas de otros ácidos carboxílicos , aunque en condiciones normales, no se formará o bien una cloruro de acilo o un anhídrido de ácido. Hasta hace muy poco, todos los intentos para formar cualquiera de estos derivados han resultado en monóxido de carbono en su lugar. Ahora se ha demostrado que el anhídrido puede ser producido por reacción de fluoruro de formilo con formiato de sodio a -78 ° C, y el cloruro haciendo pasar HCl en una solución de 1-formimidazole en monoclorometano a -60 ° C. El calor también puede causar que el ácido fórmico se descomponga al monóxido de carbono y agua. Acciones ácido fórmico algunas de la la reducción de propiedades de aldehídos.
El ácido fórmico es único entre los ácidos carboxílicos en su capacidad para participar en reacciones de adición con alquenos . Ácidos fórmico y alquenos reaccionan fácilmente para formar formiato ésteres. En presencia de ciertos ácidos, incluyendo sulfúrico y ácidos fluorhídrico, sin embargo, una variante de la Reacción de Koch se lleva a cabo en su lugar, y el ácido fórmico se añade a la alqueno para producir un ácido carboxílico más grande.
La mayoría de las sales de formiato simples son agua soluble . También es un compuesto bi-funcional.
Producción
Una cantidad significativa de ácido fórmico se produce como un subproducto en la fabricación de otros productos químicos, especialmente ácido acético . Esta producción es insuficiente para satisfacer la demanda actual de ácido fórmico, y un poco de ácido fórmico debe ser producido por su propio bien.
Cuando metanol y monóxido de carbono se combinan en la presencia de un fuerte base, el derivado de ácido fórmico resultados formiato de metilo, de acuerdo con la ecuación química
En la industria, esta reacción se lleva a cabo en la fase líquida a presión elevada. Condiciones de reacción típicas son 80 ° C y 40 atm. La base más ampliamente usado es metóxido de sodio. La hidrólisis del formiato de metilo produce el ácido fórmico:
La hidrólisis directa de formiato de metilo requiere un gran exceso de agua para proceder de manera eficiente, y algunos productores realizar por una ruta indirecta por primera reaccionar el formiato de metilo con amoniaco para producir formamida y, a continuación, la hidrolización de la formamida con ácido sulfúrico para producir ácido fórmico:
Esta técnica tiene sus propios problemas, en particular la eliminación de la de amonio subproducto sulfato, energía para algunos fabricantes han desarrollado recientemente medios eficientes de separación del ácido fórmico de la gran cantidad en exceso de agua utilizada en la hidrólisis directa. En uno de estos procesos (utilizado por BASF) el ácido fórmico se retira del agua a través de extracción de líquido con una base orgánica.
En el laboratorio de ácido fórmico puede obtenerse por calentamiento ácido oxálico en anhidro glicerol y la extracción por destilación al vapor. Otra preparación (que debe realizarse bajo una campana de extracción) es el ácido hidrólisis de acetato de isonitrilo usando HCl solución.
- C 2 H 5 NC + 2 H 2 O → C 2 H 5 NH 2 + HCOOH
El isonitrilo se obtiene por reacción de etil amina con cloroformo (tenga en cuenta que se requiere la campana de humos debido al olor objetable apabullante del isonitrilo).
Usos
El uso principal de ácido fórmico es como una conservante y antibacteriano agente en la alimentación del ganado. Cuando se rocía en fresco heno u otra ensilado, se detiene a ciertos procesos de desintegración y hace que la alimentación para conservar su valor nutritivo más tiempo, y lo que es ampliamente utilizado para preservar la alimentación de invierno para el ganado . En las aves de corral de la industria, a veces se añade al pienso para matar bacteria de la salmonela. Otros usos:
- Se utiliza para procesar látex orgánico (SAP) en bruto de caucho .
- Los apicultores utilizan ácido fórmico como acaricida contra la traqueal ( Acarapisosis) y el ácaro Ácaro Varroa.
- Es de menor importancia en el textil la industria y para la curtido de cuero.
- Algunos formiato ésteres son aromas artificiales o perfumes.
- Es el ingrediente activo en algunas marcas de la casa eliminador de depósitos calcáreos.
- Se utiliza en laboratorios como un modificador de solvente para Las separaciones por HPLC de proteínas y péptidos, sobre todo cuando se está preparando la muestra por espectrometría de masas análisis.
- Es utilizado por los laboratorios de patología clínica para desinfectar prión actividad en muestras de cerebro
En la química orgánica sintética, el ácido fórmico se utiliza a menudo como una fuente de ion hidruro. La Reacción de Eschweiler-Clarke y la Reacción de Leuckart-Wallach, son ejemplos de esta aplicación. También se utiliza como una fuente de hidrógeno en hidrogenación por transferencia.
En el laboratorio de ácido fórmico también se utiliza como fuente de monóxido de carbono , que se libera mediante la adición de ácido sulfúrico . El ácido fórmico es también una fuente para una grupo formilo por ejemplo en el formilación de metilanilina a N-metilformanilida en tolueno .
Las pilas de combustible que utilizan modificados ácido fórmico son prometedores.
Historia
Ya en el siglo 15, algunos alquimistas y naturalistas eran conscientes de que los hormigueros despedían un vapor ácido. La primera persona en describir el aislamiento de esta sustancia (por la destilación de un gran número de hormigas) fue el Inglés naturalista John Ray, en 1671. Las hormigas secretan el ácido fórmico con fines de ataque y defensa. El ácido fórmico fue sintetizado por primera vez a partir de ácido cianhídrico por el francés químico Joseph Gay-Lussac. En 1855, otro químico francés, Marcellin Berthelot, desarrolló una síntesis a partir de monóxido de carbono que es similar a la utilizada hoy en día.
En la industria química, ácido fórmico fue considerado durante mucho tiempo un compuesto químico de interés industrial sólo de menor importancia. A finales de la década de 1960, sin embargo, cantidades importantes de esta se hizo disponible como un subproducto de ácido acético de producción. Se encuentra ahora creciente uso como conservante y antibacteriana in alimentación del ganado.
Seguridad
El peligro principal de ácido fórmico es de la piel o los ojos con ácido fórmico líquido o con los vapores concentrados. Cualquiera de estas vías de exposición puede causar quemaduras químicas graves, y exposición de los ojos puede provocar daños permanentes en los ojos. Vapores inhalados pueden igualmente causar irritación o quemaduras en las vías respiratorias. Dado que el monóxido de carbono también puede estar presente en los vapores de ácido fórmico, se debe tener cuidado donde grandes cantidades de vapores de ácido fórmico están presentes. Los EE.UU. OSHA Nivel de exposición permisible ( PEL) del vapor de ácido fórmico en el ambiente de trabajo es de 5 partes por millón de partes de aire ( ppm).
El ácido fórmico es metabolizado y eliminado por el cuerpo fácilmente. Sin embargo, algunos efectos crónicos se han documentado. Algunos experimentos con animales han demostrado que es un mutágeno, y la exposición crónica puede causar daño al hígado o riñón. Otra posibilidad con la exposición crónica es el desarrollo de una piel de alergia que se manifiesta sobre re-exposición al químico.
Los peligros de las soluciones de ácido fórmico dependen de la concentración. La siguiente tabla muestra el Clasificación de las soluciones de ácido fórmico de la UE:
| Concentración ( por ciento en peso) | Clasificación | Frases-R |
|---|---|---|
| 2% -10% | Irritante (Xi) | R36 / 38 |
| 10% -90% | Corrosivo (C) | R34 |
| > 90% | Corrosivo (C) | R35 |
Una ensayo para ácido fórmico en los fluidos corporales, diseñado para la determinación de formiato después de la intoxicación por metanol, se basa en la reacción de formiato con formiato deshidrogenasa bacteriana.

