
De fer (III) chlorure
Renseignements généraux
SOS croit que l'éducation donne une meilleure chance dans la vie des enfants dans le monde en développement aussi. Le parrainage d'enfants aide les enfants un par un http://www.sponsor-a-child.org.uk/ .
| De fer (III) chlorure | |
|---|---|
 | |
 |  |
De fer (III) chlorure | |
Autres noms chlorure ferrique | |
| Identificateurs | |
| Numéro CAS | 7705-08-0, hexahydraté: [ |
| Numéro RTECS | LJ9100000 |
| Propriétés | |
| Formule moléculaire | FeCl 3 |
| Masse molaire | 162,2 g · mol -1 hexahydraté: 270,3 g · mol -1 |
| Apparence | vert-noir par la lumière réfléchie; rouge-violet par lumière transmise hexahydraté: solide jaune aq. solutions: marron |
| Densité | 2,80 g · cm -3 Solution à 40%: 1,4 g · ml -1 |
| Point de fusion | 306 ° C, 579 K, 583 ° F |
| Point d'ébullition | 315 ° C, 588 K, 599 ° F (décomposition partielle de FeCl 2 + Cl 2) |
| Solubilité dans l'eau | 92 g / 100 ml (20 ° C) |
| Solubilité dans l'acétone Méthanol Éthanol De l'éther diéthylique | 63 g / 100 ml (18 ° C) très soluble 83 g / 100 ml très soluble |
| Viscosité | Solution à 40%: 12 c P |
| Structure | |
| Crystal structure | hexagonal |
| Coordination géométrie | octaédrique |
| Risques | |
| Phrases-R | R22, R34 |
| Phrases S | S26, S28 |
| Principal dangers | Très corrosif |
| NFPA 704 |  0 3 1 |
| Des composés apparentés | |
| D'autres anions | Fer (III) fluorure De fer (III) de bromure |
| D'autres cations | Fer (II) chlorure Manganèse (II) chlorure Cobalt (II) chlorure Le ruthénium (III), le chlorure de |
| Connexe coagulants | Le sulfate de fer (II) Chlorure Polyaluminium |
| Sauf indication contraire, les données sont données pour le matériel dans leur état standard (à 25 ° C, 100 kPa) | |
| Références d'Infobox | |
De fer (III) chlorure, génériquement appelé chlorure ferrique, est un produit à l'échelle industrielle un composé chimique , la formule FeCl 3. La couleur de fer (III) cristaux de chlorure dépend de l'angle de vue: par la lumière réfléchie les cristaux apparaissent vert foncé, mais par la lumière transmise ils apparaissent rouge pourpre. Fer (III) anhydre est le chlorure de déliquescente, formant hydraté brumes de chlorure d'hydrogène dans l'air humide.
Lorsque dissous dans l'eau, le fer (III) subit chlorure hydrolyse et dégage de la chaleur dans un réaction exothermique. Le brun, acide, et résultant corrosive solution est utilisée comme un coagulant dans traitement des eaux usées et production d'eau potable, et en tant que agent d'attaque chimique pour métaux à base de cuivre en les cartes de circuits imprimés. Fer (III) anhydre chlorure est une assez forte Acide de Lewis, et on l'utilise comme catalyseur dans synthèse organique.
Propriétés chimiques et physiques
Fer (III) chlorure a un point de fusion relativement faible et se résume à environ 315 ° C. La vapeur se compose du dimère Fe 2 Cl 6 (comparer chlorure d'aluminium ) qui se dissocie de plus en plus dans le monomère FeCl 3 (D 3h groupe de points symétrie moléculaire) à température plus élevée, en concurrence avec sa décomposition réversible pour donner de fer (II) chlorure et le chlore gazeux.
Réactions
Fer (III) chlorure est un indicateur modérément fort Acide de Lewis, formant produits d'addition avec Les bases de Lewis telles que oxyde de triphénylphosphine, par exemple FeCl 3 (OPPh 3) 2 où Ph = un groupe phényle.
Fer (III) réagit avec du chlorure autre sels de chlorure pour donner le jaune tétraédrique FeCl 4 - ion. Sels de FeCl 4 - dans l'acide chlorhydrique peuvent être extraits dans éther diéthylique.
Lorsqu'il est chauffé avec de fer (III) de l'oxyde à 350 ° C, de fer (III) donne le chlorure de l'oxychlorure de fer, une couche solide et intercalation hôte.
- FeCl 3 + Fe 2 O 3 → 3 FeOCl
En présence d'une base, un métal alcalin des alcoolates réagissent pour donner la complexes dimères:
- 2 FeCl 3 + 6 C 2 H 5 OH + NH 3 → 6 (Fe (OC 2 H 5 3)) 2 + 6 NH 4 Cl
Oxalates réagissent rapidement avec une solution aqueuse de fer (III) pour donner le chlorure de [Fe (C 2 O 4) 3] 3. Autre sels de carboxylate forment des complexes, par exemple, citrate et tartrate.
De fer (III) est un chlorure doux agent oxydant, par exemple capable d'oxyder le cuivre (I) de chlorure de cuivre (II) . Les agents réducteurs tels que hydrazine convertir le fer (III) chlorure de complexes de fer (II).
Structure
De fer (III) chlorure adopte la Structure BiI 3, qui comprend octaédrique Fe (III) reliées entre elles par deux centres de coordonnées ligands chlorure.
Préparation et la production
Fer (III) anhydre chlorure peut être préparé par l'union des éléments:
Solutions de fer (III) chlorure sont produits industriellement à la fois de fer et de minerai, dans un procédé en boucle fermée.
- La dissolution pur fer dans une solution de fer (III) chlorure
Fe (s) + 2 FeCl3 (aq) → 3 FeCl 2 (aq) - Dissolution le minerai de fer dans l'acide chlorhydrique
Fe 3 O 4 (s) + 8 HCl (aq) → FeCl 2 (aq) + 2 FeCl3 (aq) + 4 H 2 O - Mise à jour du de fer (II) avec du chlorure de chlore
FeCl 2 2 (aq) + Cl 2 (g) → 2 FeCl3 (aq)
En variante, le fer (II) chlorure peut être oxydé avec le dioxyde de soufre:
- 32 FeCl 2 + 8 SO 2 + 32 HCl → 32 FeCl 3 + S 8 + 16 H 2 O
Comme beaucoup d'autres chlorures métalliques hydratés, le fer (III) hydraté chlorure peut être converti en le sel anhydre par chauffage au reflux avec le chlorure de thionyle. L'hydrate ne peut pas être converti en fer (III) anhydre chlorure seulement par la chaleur, comme la place du HCl se dégage et formes d'oxychlorure de fer.
Utilisations
Industriel
Dans une application industrielle, le fer (III) est utilisé en chlorure traitement des eaux usées et production d'eau potable. Dans cette application, FeCl 3 dans de l'eau légèrement basique réagit avec l' hydroxyde ions pour former un floc de fer (III) de l'hydroxyde, ou plus précisément formulé comme FeO (OH) -, qui peuvent éliminer les matières en suspension.
- Fe 3+ + 4 OH - → Fe (OH) 4 - → FeO (OH) 2 - · H 2 O
Une autre application importante de fer (III) est le chlorure de gravure de cuivre en deux étapes réaction d'oxydoréduction de cuivre (I) de chlorure et de cuivre (II) dans la production de les cartes de circuits imprimés.
- FeCl 3 + Cu + → FeCl 2 CuCl
- FeCl 3 + CuCl → FeCl 2 + CuCl2
De fer (III) chlorure est utilisé comme catalyseur pour la réaction de l'éthylène avec le chlore en formant du dichlorure d'éthylène ( Le 1,2-dichloroéthane), un important produit chimique de base, qui est principalement utilisé pour la production industrielle de le chlorure de vinyle, le monomère pour la fabrication de PVC.
- H 2 C = CH 2 Cl 2 → + ClCH 2 CH 2 Cl
Utilisation en laboratoire
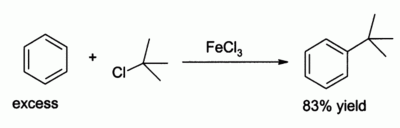
Dans le laboratoire de fer (III) chlorure est couramment employé en tant que Acide de Lewis pour catalyser des réactions telles que chloration du les composés aromatiques et Réaction de Friedel-Crafts de composés aromatiques. Il est moins puissant que le chlorure d'aluminium , mais dans certains cas, cette douceur conduit à des rendements plus élevés, par exemple dans l'alkylation du benzène:
Le «test de chlorure ferrique" est un test colorimétrique traditionnel pour phénols, qui utilise un 1% de fer (III) une solution de chlorure qui a été neutralisé avec de l'hydroxyde de sodium jusqu'à ce qu'un léger précipité de FeO (OH) est formé. Le mélange est filtré avant utilisation. La substance organique est dissoute dans l'eau, le methanol ou l'éthanol , puis neutralisé le fer (III) une solution de chlorure est ajoutée une coloration temporaire ou permanent (, vert ou bleu généralement pourpre) indique la présence d'un phénol ou d'énol.
D'autres utilisations
Anhydre fer (III) chlorure est parfois utilisé en tant que réactif de séchage dans certaines réactions.
Fer (III) chlorure est parfois utilisé par les collectionneurs américains pour identifier les dates de Nickels Buffalo qui sont si mal porté que la date ne est plus visible.
Fer (III) chlorure est couramment utilisé par les artisans de couteau et des forgerons épée à lames de taches, pour donner un effet de contraste au métal, et de voir la stratification ou les imperfections métal.
De fer (III) chlorure est nécessaire pour la gravure de plaques de photogravure pour l'impression d'images photographiques et d'art fines dans et la gravure en taille-douce pour cylindres de rotogravure utilisés dans l'industrie de l'impression.
Fer (III) chlorure est également utilisé en médecine vétérinaire pour traiter overcropping des griffes d'un animal, en particulier lorsque les résultats de overcropping des saignements.
Précautions
De fer (III) chlorure est toxique, très corrosif et acide. Le matériau anhydre est un agent de déshydratation puissant. Dans les écoles secondaires / élevés partout dans le monde, où le design et la technologie est une matière enseignée, chlorure ferrique utilisé pour PCB gravure est généralement diluée avec de l'eau. Malgré cela, les mains et les autres surfaces qui ont contacté il devrait encore être lavés immédiatement après une finitions avec elle.

