
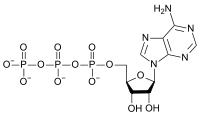
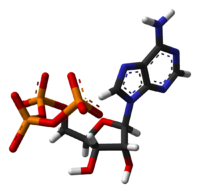
Trifosfato de adenosina
Sobre este escolas selecção Wikipedia
Esta seleção Wikipedia está offline disponível a partir de Crianças SOS, para distribuição no mundo em desenvolvimento. Com SOS Children você pode escolher para patrocinar crianças em mais de cem países
| Trifosfato de adenosina | |
|---|---|
 | |
 | |
5- (6-aminopurina-9-il) | |
| Identificadores | |
| Número CAS | 56-65-5 |
| Propriedades | |
| Fórmula molecular | C 10 H 16 N 5 O 13 P 3 |
| Massa molar | 507,181 g / mol |
| Acidez (p Ka) | 6.5 |
| Excepto quando indicado, os dados são dados para materiais no seu estado normal (a 25 ° C, 100 kPa) | |
| Referências de Infobox | |
A adenosina 5'-trifosfato (ATP) é um multifuncional nucleótidos que é mais importante como um " molecular moeda "de intracelular energia transferência. Neste papel, o ATP transporta energia química dentro de células para metabolismo. É produzido como uma fonte de energia durante os processos de fotossíntese e respiração celular e consumida por muitos enzimas e uma multiplicidade de processos celulares, incluindo reações biossintéticas, e motilidade divisão celular. Em vias de transdução de sinal, o ATP é utilizado como um substrato pela quinases que fosforilar proteínas e lípidos , bem como pelos adenilato-ciclase, que utiliza ATP para produzir o segunda molécula mensageira AMP cíclico.
A estrutura desta molécula é constituída por um base de purina ( adenina) ligado ao um 'átomo de carbono de um açúcar pentose ( ribose). Três grupos fosfato estão ligados na extremidade 5 'átomo de carbono do açúcar pentose. ATP é também incorporada ácidos nucleicos por polimerases nos processos de A replicação do ADN e transcrição. Quando o ATP é utilizado na síntese do ADN, o açúcar ribose é primeiro convertido deoxyribose por ribonucleótido-redutase. ATP foi descoberto em 1929 por Karl Lohmann, e foi proposta como sendo a principal molécula de transferência de energia na célula por Fritz Albert Lipmann em 1941.
Propriedades físicas e químicas
ATP consiste adenosina --se um composto de anel de adenina e um ribose açúcar - e três grupos fosfatos (trifosfato). Os grupos fosforilo, começando com o grupo mais próximo da ribose, são referidos como o alfa (α), beta (β) e gama (γ) fosfatos. O ATP é altamente solúvel em água e é bastante estável em soluções de pH entre 6,8-7,4, mas é rapidamente hidrolisado pelo pH extremo. Por conseguinte, o ATP é melhor armazenado como um sal anidro.
O ATP é uma molécula instável e tende a ser hidrolisados em água. Se ATP e ADP estão em equilíbrio químico , quase todo o ATP será convertido em ADP. Qualquer sistema que está longe do equilíbrio contém energia potencial, e é capaz de fazer o trabalho . Células biológicas manter a proporção do ADP em ATP para um ponto de dez ordens de grandeza em relação ao equilíbrio, com concentrações mais elevadas de ATP mil vezes do que a concentração de ADP. Este deslocamento do equilíbrio significa que a hidrólise de ATP na célula liberta uma grande quantidade de energia. ATP é vulgarmente referida como uma "molécula de alta energia"; porém isso é incorreto, como uma mistura de ATP e ADP em equilíbrio na água pode fazer nenhum trabalho útil a todos. O ATP não contêm "ligações de alta energia", e qualquer outra molécula instável serviria igualmente bem como uma forma de armazenar energia, se a célula manteve sua concentração longe do equilíbrio.
A quantidade de energia libertada pode ser calculada a partir das mudanças na energia em condições não-naturais. A variação líquida em energia térmica ( entalpia ) a a temperatura e pressão da decomposição do ATP padrão em hidratada ADP e fosfato inorgânico hidratado é -20,5 kJ / mol, com uma mudança de energia livre de 3,4 kJ / mol. A energia liberada por clivagem ou um fosfato (Pi) ou pirofosfato (IPP) unidade de ATP, com todos os reagentes e produtos na sua estados padrão de concentração de 1 M, são os seguintes:
- ATP + H2O → ADP (hidratado) + Pi (hidratado) + H + (hidratado) ΔG˚ = -30,54 kJ / mol (-7,3 kcal / mol)
- ATP + H2O → AMP (hidratado) + PPi (hidratado) + H + (hidratado) ΔG˚ = -45,6 kJ / mol (-10,9 kcal / mol)
Estes valores podem ser usados para calcular a variação da energia sob condições fisiológicas e o rácio celular de ATP / ADP. Os valores indicados para a energia livre de Gibbs para esta reacção são dependentes de uma série de factores, incluindo a força iónica total e a presença de metais alcalino-terrosos , tais como os iões Mg2 + e Ca2 +. Sob condições típicas celulares, ΔG é aproximadamente -57 kJ / mol (-14 Kcal / mol).
A ionização em sistemas biológicos
ATP tem vários grupos ionizáveis com diferente As constantes de dissociação de ácido. Em solução neutra, o ATP é ionizado e existe principalmente como ATP 4-, com uma pequena proporção de ATP 3-. Como ATP tem vários grupos carregados negativamente em solução neutra, que pode metais de quelato com afinidade muito elevada. O constante de ligação para vários iões metálicos são (como determinado por mole) como Mg 2+ (9 554), Na + (13), Ca 2+ (3 722), K + (8), Sr2 + (1 381) e Li + (25). Devido à força destas interacções, ATP existe principalmente na célula num complexo com Mg2 +.
Biossíntese
O ATP concentração no interior da célula é tipicamente 1 - 10 mM. O ATP pode ser produzido pela reações redox usando simples e complexos açúcares ( carboidratos ) ou lipídios como fonte de energia. Para ATP para ser sintetizado a partir de combustíveis complexos, eles primeiro precisam ser dividido em seus componentes básicos. Os carboidratos são hidrolisado em açúcares simples, tais como glucose e frutose. Gorduras ( triglicéridos) são metabolizados para dar ácidos gordos e glicerol.
O processo global de oxidação de glicose para o dióxido de carbono é conhecido como respiração celular e pode produzir até 36 moléculas de ATP a partir de uma única molécula de glicose. O ATP pode ser produzido por uma série de processos celulares distintas; as três vias principais usado para gerar energia em eucariotas organismos são glicólise eo ciclo de ácido cítrico / fosforilação oxidativa, ambos os componentes de respiração celular; e beta-oxidação. A maior parte desta produção de ATP por uma não- fotossintética eucariota aeróbico tem lugar na mitocôndria , o que pode tornar-se quase 25% do volume total de uma célula típica.
Glicólise
Na glicólise, glucose e glicerol são metabolizados para piruvato através da via glicolítica. Na maioria dos organismos este processo ocorre no citosol, mas em alguns protozoários, tais como a cinetoplastídeos, esta é levada a cabo num especializada organelo denominado glicossomo. Glicólise gera um dois líquidos moléculas de ATP através substrato de fosforilação catalisada por duas enzimas: PGK e piruvato-quinase. Duas moléculas de O NADH também é produzido, o qual pode ser oxidado através do elétron cadeia de transporte e resultado na geração de ATP adicional ATP sintase. O piruvato gerado como um produto final da glicólise é um substrato para a Ciclo de Krebs.
Ciclo de ácido cítrico
Na mitocôndria , piruvato é oxidado pela complexo piruvato desidrogenase de acetil-CoA, que está totalmente oxidado a dióxido de carbono através do ciclo do ácido cítrico (também conhecido como o ciclo de Krebs). Cada "virada" do ciclo do ácido cítrico produz duas moléculas de dióxido de carbono , uma molécula de ATP o equivalente trifosfato de guanosina (GTP) através de nível de substrato de fosforilação catalizada pela succinil CoA sintetase, três moléculas da reduzida coenzima NADH, e uma molécula da coenzima reduzido FADH 2. Ambas estas últimas moléculas são reciclados para os seus estados oxidada (NAD + e FAD, respectivamente) através do cadeia de transporte de elétrons, o que gera ATP adicional fosforilação oxidativa. A oxidação de uma molécula de NADH resulta na síntese de cerca de 3 moléculas de ATP, e a oxidação de um FADH 2 produz cerca de 2 moléculas de ATP. A maioria do ATP celular é gerado por este processo. Embora o ciclo de ácido cítrico não envolve molecular de oxigénio , é uma obligately processo aeróbio porque O2 é necessária para reciclar o NADH e FADH2 reduzida aos seus estados oxidados. Na ausência de oxigênio o ciclo de ácido cítrico deixará de funcionar devido à falta de disponibilidade de NAD + e FAD.
A geração de ATP pela mitocôndria de NADH citosólico baseia-se na shuttle malato-aspartato (e, em menor extensão, o transporte para o glicerol-fosfato) porque a membrana mitocondrial interna é impermeável ao NADH e NAD +. Em vez de transferir o NADH gerada, uma malato convertidos enzima desidrogenase oxaloacetato para malato, que é translocado para a matriz mitocondrial. Outra reacção catalisada por malato desidrogenase ocorre na direcção oposta, produzindo oxaloacetato e NADH a partir do malato recém transportados e armazenar o interior da mitocôndria de NAD +. A transaminase converte o oxaloacetato de aspartato para o transporte de volta através da membrana e para dentro do espaço intermembranar.
Em fosforilação oxidativa, a passagem de electrões do NADH e FADH2 através dos poderes cadeia de transporte de electrões do bombeamento de protões para fora da matriz mitocondrial e no espaço intermembranar. Isto cria um próton força motriz que é o efeito líquido de um e um gradiente de pH gradiente de potencial eléctrico através da membrana mitocondrial interna. Fluxo de prótons para baixo este gradiente de potencial - ou seja, a partir do espaço intermembranar para a matriz - fornece a força motriz para a síntese de ATP por ATP sintase. Este enzima contém uma subunidade de rotor que roda fisicamente em relação às porções estáticas da proteína durante a síntese de ATP.
A maior parte do ATP sintetizado nas mitocôndrias será utilizada para os processos celulares no citosol; Desse modo, deve ser exportado do seu local de síntese na matriz mitocondrial. A membrana interna contém um antiportador, a translocase ADP / ATP, que é um proteína de membrana integral utilizado para a troca de recém-sintetizado de ATP em ADP para a matriz no espaço intermembranar. Este translocase é conduzido pelo potencial de membrana, tal como resulta no movimento de cerca de 4 cargas negativas para fora da membrana mitocondrial em troca de três cargas negativas movido para dentro. No entanto, é também necessário para o transporte de fosfato na mitocôndria; o transportador move-se um fosfato de protões em cada com fosfato, dissipando-se parcialmente o gradiente de protões.
Beta-oxidação
Os ácidos gordos também podem ser discriminados acetil-CoA beta-oxidação. Cada ronda deste ciclo reduz o comprimento da cadeia de acilo por dois átomos de carbono e produz um NADH e FADH2 uma molécula, que são utilizados para gerar ATP pela fosforilação oxidativa. Porque NADH e FADH2 são moléculas ricas em energia, dezenas de moléculas de ATP pode ser gerado pela beta-oxidação de uma única cadeia acilo longa. A alta produção de energia deste processo eo armazenamento compacto de gordura explicar por que é a fonte mais densa de dietética calorias.
Respiração anaeróbica
Respiração anaeróbica ou fermentação implica a geração de energia por meio do processo de oxidação na ausência de O2 como um aceitador de electrões. Na maior parte dos eucariotas, a glucose é usada como um armazenamento de energia e um doador de electrões. A equação para a oxidação de glicose para ácido láctico é:
- C 6 H 12 O 6
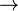 2CH 3 CH (OH) COOH + 2 ATP
2CH 3 CH (OH) COOH + 2 ATP
Em procariotas, vários aceitadores de electrões pode ser usado na respiração anaeróbia. Estes incluem nitrato , sulfato ou dióxido de carbono. Estes processos levam aos processos ecologicamente importantes da desnitrificação, e redução do sulfato acetogénese, respectivamente.
ATP reabastecimento por quinases nucleosídeo difosfato
ATP também pode ser sintetizado por várias chamadas reacções "reabastecimento" catalisada pela enzima de famílias quinases nucleosídeos difosfato (NDKs), que usam outros trifosfatos de nucleósidos como um doador de fosfato de alta energia, eo ATP: família guanido-fosfotransferase, que usa creatina.
- ADP + GTP
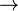 ATP + PIB
ATP + PIB
Produção de ATP durante a fotossíntese
Em plantas, o ATP é sintetizado membrana tilacoide do durante o cloroplasto reações luz-dependentes da fotossíntese em um processo chamado fotofosforilação. Aqui, a energia de luz é utilizada para bombear protões através da membrana do cloroplasto. Isso produz uma força motriz protónica e isso impulsiona o ATP sintase, exatamente como na fosforilação oxidativa. Algum do ATP produzido nos cloroplastos é consumido na Ciclo de Calvin, que produz açúcares triose.
Reciclagem de ATP
A quantidade total de ATP no corpo humano é de cerca de 0,1 toupeira. A maioria do ATP não é normalmente sintetizada de novo, mas é gerado a partir de ADP pelos processos acima mencionados. Assim, a qualquer momento, o montante total de ATP + ADP permanece relativamente constante.
A energia utilizada pelas células humanas requer a hidrólise de 100 a 150 moles de ATP ao dia, que é de cerca de 50 a 75 kg. Tipicamente, um ser humano vai usar-se o seu peso corporal de ATP ao longo do dia. Isto significa que cada molécula de ATP é reciclado 1000-1500 vezes durante um único dia (100 / 0,1 = 1,000). ATP não pode ser armazenada, daí o seu consumo segue de perto a sua síntese.
Regulamento da biossíntese
Produção de ATP em uma célula eucariótica aeróbico é fortemente regulado por mecanismos alostéricos, por efeitos de feedback, e pela dependência da concentração de substrato de enzimas individuais dentro das glicólise e oxidativos vias de fosforilação. Os pontos-chave de controlo ocorrer em reacções enzimáticas que são tão energeticamente favorável que sejam eficazmente irreversível sob condições fisiológicas.
Na glicólise, hexoquinase é directamente inibida pelo seu produto, a glucose-6-fosfato, e piruvato-quinase é inibida por ATP em si. O principal ponto de controle para a via glicolítica é fosfofrutoquinase (PFK), que é alostericamente inibida por altas concentrações de ATP e activado por altas concentrações de AMP. A inibição da PFK por ATP é invulgar, uma vez que o ATP é também um substrato na reacção catalisada por PFK; a forma biologicamente activa da enzima é um tetrâmero que existe em duas conformações possíveis, apenas um dos quais se liga o segundo substrato de frutose-6-fosfato (F6P). A proteína tem dois sites para ATP vinculativo - o local activo é acessível em qualquer conformação da proteína, mas a ligação ao local de inibidor de ATP estabiliza a conformação que se liga F6P mal. Um número de outras moléculas pequenas podem compensar a mudança induzida por ATP em equilíbrio de conformação e reactivar PFK, incluindo AMP cíclico, os iões de amónio, fosfato inorgânico, e frutose 1,6 e 2,6 bifosfato.
O ciclo do ácido cítrico é regulado principalmente pela disponibilidade de substratos principais, particularmente a proporção de NAD + para NADH e as concentrações de cálcio , fosfato inorgânico, ATP, ADP, AMP e. Citrato - a molécula que dá nome ao ciclo - é um inibidor de feedback citrato sintase e também inibe PFK, proporcionando uma ligação directa entre a regulação do ciclo do ácido cítrico e glicólise.
Em fosforilação oxidativa, o ponto de controlo chave é a reacção catalisada pela citocromo c oxidase, que é regulada pela disponibilidade do seu substrato, a forma reduzida de citocromo c. O montante da redução do citocromo c disponível está diretamente relacionada com as quantidades de outros substratos:
o que implica diretamente esta equação:
Assim, um elevado rácio de [NADH] a [NAD +] ou um rácio baixo de [ADP] [P i] a [ATP] implica uma elevada quantidade de citocromo c reduzido e um elevado nível de actividade do citocromo c oxidase. Um nível adicional de regulação é introduzido pelos preços de transporte de ATP e NADH entre a matriz mitocondrial eo citoplasma.
Funções em células
ATP é gerado na célula por processos que consomem energia e é decomposto por processos de libertação de energia. Desta forma ATP transfere energia entre espacialmente separado reacções metabólicas. ATP é a principal fonte de energia para a maioria das funções celulares. Isto inclui a síntese de macromoléculas, incluindo ADN, ARN, e proteínas. ATP também desempenha um papel fundamental no transporte de macromoléculas através da membrana celular, por exemplo, exocitose e endocitose.
Na síntese do ácido nucleico ARN, o ATP é uma das quatro nucleótidos incorporados directamente para moléculas de ARN por As polimerases de ARN. A energia motriz esta polimerização vem de clivagem de um pirofosfato (dois grupos fosfato). O processo é semelhante na biossíntese de ADN, excepto que o ATP é reduzido para o desoxirribonucleótido dATP, antes da incorporação no ADN.
O ATP é criticamente envolvido na manutenção da estrutura da célula, facilitando a montagem e desmontagem dos elementos do citoesqueleto. Em um processo relacionado, o ATP é necessário para o encurtamento de filamentos de actina e miosina pontes cruzadas necessárias para contracção do músculo. Este último processo é uma das principais necessidades energéticas dos animais e é essencial para locomoção e respiração.
Sinalização celular
Sinalização extracelular
O ATP é também um molécula sinalizadora. ATP, ADP, adenosina ou são reconhecidos por receptores purinérgicos.
Nos seres humanos, este papel de sinalização é importante, tanto no sistema nervoso central e periférico. Liberação dependente de atividade de ATP a partir de sinapses, axônios e glia ativa os receptores de membrana conhecidos como purinérgicos P2. Os receptores metabotrópicos são P2Y, ou seja Acoplado à proteína G e modulam principalmente cálcio intracelular e, por vezes, os níveis de AMP cíclicos. Quinze membros da família P2Y foram relatados (P2Y1-P2Y15), embora alguns só estão relacionados através de homologia fraca e vários (P2Y5, P2Y7, P2Y9, P2Y10) não funcionam como receptores que aumentam cálcio citosólico. O subgrupo receptor P2X ionotropic composto por sete membros (P2X1-P2X7), que são canais de Ca2 + íon -permeable fechado por ligando que se abrem quando ligado a um nucleótido purina extracelular. Em contraste com receptores P2 (fim agonista ATP> ADP> AMP> ADO), purinérgico nucleótidos como ATP não são fortes agonistas de receptores P1, que são fortemente activadas por adenosina e outros nucleosídeos (ADO> AMP> ADP> ATP). Receptores P1 tem A1, A2a, A2b, e A3 subtipos ("a" como um remanescente da antiga nomenclatura de receptor de adenosina), todos os quais são receptores acoplados à proteína, A1 e A3 ser acoplados a Gi, e A2a e A2b sendo acoplado a Gs.
Sinalização intracelular
O ATP é crítica em processos de transdução de sinal. É usado por quinases como a fonte de grupos de fosfato nas suas reacções de transferência de fosfato. Actividade de cinase em substratos, tais como proteínas ou lípidos da membrana são uma forma comum de transdução de sinal. A fosforilação de uma proteína por uma quinase pode activar esta cascata tal como a activada por mitogénio cascata de proteina-quinase.
ATP também é utilizado por adenilato-ciclase e é transformado no segundo mensageiro AMP cíclico molécula, a qual está envolvida no desencadeamento de sinais de cálcio pela libertação de cálcio das reservas intracelulares. Esta forma de transdução de sinal é particularmente importante na função cerebral, embora esteja envolvida na regulação de uma grande variedade de outros processos celulares.
Síntese desoxirribonucle�ido
Em todos os organismos conhecidos, os desoxirribonucleótidos que compõem ADN são sintetizados pela acção de ribonucleótido-redutase (RNR) enzimas de ribonucleótidos nos seus correspondentes. Esta enzima reduz a 2 ' grupo hidroxilo no de açúcar da ribose de desoxirribose, formando um desoxirribonucleótido (denotado dATP). Todas as enzimas redutase de ribonucleótidos usar um comum sulfidrila mecanismo radical dependente reativa resíduos de cisteína que oxidam para formar ligações dissulfureto no decurso da reacção. RNR enzimas são reciclados por reacção com thioredoxin ou glutarredoxina.
A regulação da RNR e enzimas relacionadas mantém um equilíbrio de dNTP em relação ao outro e em relação ao NTPs na célula. Muito inibe de baixa concentração de dNTP A síntese de ADN e de reparação do ADN e é letal para a célula, enquanto que uma proporção anormal de dNTP está mutagénico, devido ao aumento da probabilidade de o Polimerase de ADN incorporando o dNTP errado durante a síntese de ADN. Regulamento de diferencial ou especificidade de RNR tem sido proposta como um mecanismo para alterações nos tamanhos relativos dos grupos de dNTP intracelulares sob stress celular, tal como hipóxia.
A ligação às proteínas
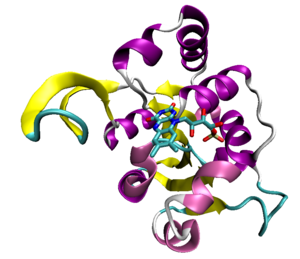
Algumas proteínas que se ligam ATP fazê-lo em uma característica dobragem da proteína conhecida como o Rossmann fold, que é um general de ligação de nucleotídeos domínio estrutural que também pode vincular o cofator NAD. As proteínas de ligação a ATP mais comuns, conhecidos como quinases, compartilhar um pequeno número de dobras comuns; o proteínas quinases, a maior superfamília quinase, todas as características estruturais comuns partes especializada para a ligação ATP e transferência de fosfato.
ATP em complexos com proteínas requer geralmente a presença de um divalente catião , quase sempre de magnésio , que se liga aos grupos fosfato do ATP. A presença de magnésio diminui grandemente o constante de dissociação de ATP a partir do seu parceiro de ligação da proteína, sem afectar a capacidade da enzima para catalisar a sua reacção uma vez que o ATP se ligou. A presença de iões de magnésio podem servir como um mecanismo para a regulação da cinase.
Análogos de ATP
Laboratórios de Bioquímica costumam usar estudos in vitro para explorar processos moleculares dependentes de ATP. Os inibidores de enzimas de enzimas dependentes de ATP, tais como quinases são necessários para analisar o sítios de ligação e estados de transição envolvidas em reacções dependentes de ATP. Análogos de ATP também são utilizados em A cristalografia de raios-X para determinar um estrutura de proteína em complexo com o ATP, frequentemente em conjunto com outros substratos. Análogos de ATP mais útil não pode ser hidrolisado como seria de ATP; em vez disso, armadilha da enzima em uma estrutura intimamente relacionada com o estado ATP-bound. Adenosina 5 '- (gama-thiotriphosphate) é um análogo de ATP extremamente comum em que um dos oxigénios do gama-fosfato é substituído por um enxofre átomo; esta molécula é hidrolisada a uma taxa significativamente mais lenta do que a própria e funções do ATP como um inibidor de processos dependentes de ATP. Em estudos de cristalografia, estados de transição hidrólise são modelados pelo limite ion vanadato. No entanto, recomenda-se precaução na interpretação dos resultados de experimentos usando análogos de ATP, uma vez que algumas enzimas podem hidrolisar-los a preços apreciáveis em alta concentração.
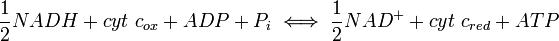
![\ Frac {cit ~ c_ {vermelho}} {{cit ~ c_ boi}} = \ left (\ frac {[NADH]} {[NAD] ^ {+}} \ right) ^ {\ frac {1} {2 }} \ left (\ frac {[ADP] [P_ {i}]} {[ATP]} \ right) K_ {eq}](../../images/131/13158.png)
