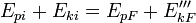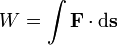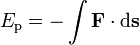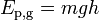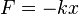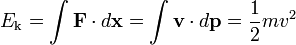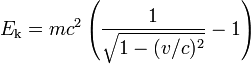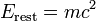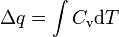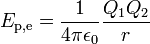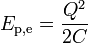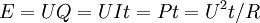Energia
Você sabia ...
Esta seleção é feita para as escolas de caridade infantil leia mais . Crianças SOS é a maior instituição de caridade do mundo dando órfãos e crianças abandonadas a chance da vida familiar.
Em física e outras ciências , energia (do grego ενεργός, energos ", ativo, trabalhando") é uma escalar quantidade física que é uma propriedade dos objectos e sistemas que é conservado por natureza. A energia é muitas vezes definida como a capacidade de fazer o trabalho .
Várias formas diferentes de energia, incluindo cinética , potencial, térmica, gravitacional, elástica, electromagnética , química, nuclear, e massa foram definidos para explicar todos os fenômenos naturais conhecidos.
A energia é convertida de uma forma para outra. Este princípio, o conservação de energia, foi postulada pela primeira vez no início do século 19, e se aplica a qualquer sistema isolado. Conforme Teorema de Noether, a conservação da energia é uma consequência do fato de que as leis da física não mudam ao longo do tempo.
Embora a energia total de um sistema não se altera com o tempo, o seu valor pode depender do quadro de referência. Por exemplo, um passageiro sentado em um avião em movimento tem zero de energia cinética em relação ao avião, mas a energia cinética diferente de zero em relação à terra.
História

O conceito de energia surgiu a partir da idéia de vis viva, que Leibniz definido como o produto da massa de um objeto e sua velocidade ao quadrado; ele acreditava que esse total vis viva foi conservada. Para explicar a abrandar devido ao atrito, Leibniz alegou que o calor consistiu no movimento aleatório das partes constituintes da matéria - uma opinião partilhada por Isaac Newton , apesar de que seria mais de um século até que este era geralmente aceite. Em 1807, Thomas Young foi o primeiro a usar o termo "energia", em vez de vis viva, em seu sentido moderno. Gustave-Gaspard Coriolis descrito " energia cinética ", em 1829, no seu sentido moderno, e em 1853, William Rankine cunhou o termo " energia potencial. "Foi alegado por alguns anos se a energia era uma substância (o calórica) ou apenas uma grandeza física, tal como impulso .
Ele amalgamado todas estas leis nas leis da termodinâmica , que ajudaram no desenvolvimento rápido de explicações de processos químicos que utilizam o conceito de energia por Rudolf Clausius, Josiah Willard Gibbs e Walther Nernst. É também conduziu a uma formulação matemática do conceito de entropia por Clausius, e para a introdução de leis de energia radiante por Jožef Stefan.
Durante uma palestra de 1961, para estudantes de graduação no California Institute of Technology, Richard Feynman , um professor de física célebre e Nobel Laureate, disse o seguinte sobre o conceito de energia:
| " | Há um fato, ou se quiser, uma lei, que rege os fenômenos naturais que são conhecidos até o momento. Não há nenhuma exceção conhecida a essa lei - é exata até agora nós sabemos. A lei é chamado conservação de energia; afirma que há uma certa quantidade, que chamamos de energia que não muda em múltiplas mudanças que a natureza sofre. Essa é uma idéia mais abstrata, porque é um princípio matemático; ele diz que há uma quantidade numérica, o que não muda quando algo acontece. Não é uma descrição de um mecanismo, ou nada de concreto; é apenas um fato estranho que nós podemos calcular um número, e quando terminar de assistir a natureza ir através de seus truques e calcular o número de novo, é o mesmo. | " |
- O Feynman Lectures on Physics | ||
Desde 1918 ele tem sido conhecido que a lei de conservação da energia é a conseqüência direta da matemática simetria de translação da quantidade conjugado de energia, ou seja o tempo . Ou seja, a energia é conservada porque as leis da física não fazem distinção entre os diferentes momentos do tempo (ver Teorema de Noether).
Energia em vários contextos, desde o início do universo
O conceito de energia e suas transformações é útil em explicar e predizer a maioria dos fenômenos naturais. A direção das transformações de energia (que tipo de energia é transformada para que outro tipo) é muitas vezes descrito por entropia (igual energia distribuída entre todos os disponíveis graus de liberdade) considerações, uma vez que, na prática, todas as transformações de energia são permitidas em pequena escala, mas certas transformações maiores não são permitidas porque é estatisticamente improvável que a energia ou matéria irá se mover aleatoriamente em formas mais concentradas ou espaços menores.
O conceito de energia é usada frequentemente em todos os campos da ciência.
- Em química , as diferenças de energia entre substâncias determinar se, e em que medida, eles podem ser convertidos em outras substâncias ou reagir com outras substâncias.
- Em biologia , as ligações químicas são quebradas e feito durante processos metabólicos, e as mudanças associadas na energia disponível são estudadas no ramo da bioenergética. A energia é muitas vezes armazenada por células sob a forma de substâncias, tais como hidratos de carbono (incluindo moléculas de açúcares) e lípidos , que libertam energia quando feito reagir com oxigénio .
- Em geologia e meteorologia, deriva continental, cordilheiras , vulcões e terremotos são fenômenos que podem ser explicados em termos de transformações de energia no interior da Terra. Enquanto fenômenos meteorológicos como vento , chuva , granizo, neve , relâmpagos, tornados e furacões , são todos um resultado de transformações de energia provocadas pela energia solar no planeta Terra.
- Em cosmologia e astronomia os fenômenos de estrelas , nova, supernova , quasares e explosões de raios gama são as mais elevadas-saída do universo transformações de energia da matéria. Tudo fenómenos estelares (incluindo a actividade solar) são accionados por vários tipos de transformações de energia. Energia em tais transformações é ou do colapso gravitacional da matéria (geralmente hidrogênio molecular) em várias classes de objetos astronômicos (estrelas, buracos negros, etc.), ou a partir da fusão nuclear (de elementos mais leves, principalmente hidrogênio).
Transformações de energia no universo ao longo do tempo são caracterizados por vários tipos de energia potencial que está disponível desde o Big Bang , mais tarde a ser "liberado" (transformada para tipos mais ativos de energia, como energia cinética ou radiante), quando um mecanismo de disparo é disponível.
Conhecer exemplos de tais processos incluem decaimento nuclear, em que a energia é liberada, que foi originalmente "armazenado" em isótopos pesados (como urânio e tório ), por nucleossíntese, um processo que, em última instância usa a energia potencial gravitacional liberada a partir do colapso gravitacional de supernovas, para armazenar energia na criação desses elementos pesados antes de serem incorporadas no sistema solar ea Terra. Esta energia é acionado e liberado em nuclear bombas de fissão. Em um processo mais lento, o calor de decaimento nuclear destes átomos no núcleo da Terra liberta calor, que por sua vez pode levantar montanhas, através orogenesis. Este levantamento lento representa um tipo de armazenamento de energia potencial gravitacional da energia térmica, que pode ser introduzida em energia cinética ativo em deslizamentos de terra, depois de um evento de disparo. Terremotos também liberam energia armazenada potencial elástica nas rochas, uma loja que tenha sido produzido em última análise, a partir das mesmas fontes de calor radioactivas. Assim, de acordo com o entendimento atual, eventos familiares, como deslizamentos de terra e terremotos liberar a energia que foi armazenada como energia potencial no campo gravitacional ou deformação elástica (energia potencial mecânica) da Terra em rochas; mas antes disso, representa a energia que foi armazenada em átomos pesados desde o colapso de estrelas de longa destruído criou esses átomos.
Em outra cadeia similar de transformações começando no início do universo, fusão nuclear do hidrogênio no Sol libera uma outra loja de energia potencial que foi criado no momento do Big Bang . Naquela época, segundo a teoria, espaço expandido eo universo esfriou muito rapidamente para o hidrogênio completamente fusível em elementos mais pesados. Isto significava que o hidrogênio representa um armazenamento de energia potencial que pode ser liberada por fusão. Um tal processo de fusão é accionado por calor e pressão gerado a partir de colapso gravitacional de nuvens de hidrogénio quando produzem estrelas, e uma parte da energia de fusão é, em seguida, transformada em luz solar. Essa luz solar do nosso Sun pode voltar a ser armazenada como energia potencial gravitacional depois que ele atinge a Terra, como (por exemplo) a água evapora dos oceanos e é depositado sobre montanhas (onde, após ser liberado em uma barragem hidroeléctrica, ele pode ser usado para conduzir turbinas / geradores para produzir electricidade). A luz solar também impulsiona toda a fenômeno meteorológico, incluindo eventos como aqueles acionados em um furacão, quando grandes áreas instáveis do mar quente, aquecida ao longo de meses, dar um pouco de sua energia térmica suddently para alimentar alguns dias de movimento de ar violenta. A luz solar é também é capturado pelas plantas como a energia química potencial, quando o dióxido de carbono e água são convertidos em uma combinação combustable de hidratos de carbono, lípidos, e oxigénio. Liberação dessa energia na forma de calor e luz podem ser desencadeados de repente por uma faísca, em um incêndio florestal; ou pode estar disponível mais lentamente para o metabolismo animal ou humano, em que estas moléculas são ingeridas, e catabolismo é desencadeada por ação da enzima. Através de todas essas cadeias Tranformation, a energia potencial armazenada no momento do Big Bang é liberado mais tarde por eventos intermediários, por vezes, ser armazenados em uma série de maneiras ao longo do tempo entre os lançamentos, como a energia mais ativo. Em todos estes eventos, um tipo de energia é convertida em outros tipos de energia, incluindo calor.
Em relação aplicações do conceito de energia
A energia é sujeita a uma estrita lei de conservação global; isto é, sempre que um (ou medidas) calcula a energia total de um sistema de partículas cujas interacções não depende explicitamente do tempo, verifica-se que a energia total do sistema permanece sempre constante.
- A energia total de uma sistema pode ser subdividido e classificados de várias formas. Por exemplo, é por vezes conveniente para distinguir energia potencial (que é uma função apenas de coordenadas) de energia cinética (que é uma função do tempo de coordenadas derivados apenas). Também pode ser conveniente para distinguir energia gravitacional, energia eléctrica, energia térmica, e outras formas. Estas classificações se sobrepõem; por exemplo, a energia térmica geralmente consiste em parte de cinética e, em parte, de energia potencial.
- A transferência de energia pode tomar várias formas; exemplos conhecidos incluem o trabalho, o fluxo de calor, e advection, como discutido abaixo .
- A palavra "energia" também é utilizado fora da física de muitas maneiras, o que pode levar a ambigüidade e incoerência. A terminologia vernacular não é consistente com a terminologia técnica. Por exemplo, o importante anúncio de serviço público, "Por favor, conservar energia" usa noções vernáculas de "conservação" e "energia" que fazem sentido no seu próprio contexto, mas são totalmente incompatíveis com as noções técnicas de "conservação" e "energia" ( tal como são utilizados na lei da conservação de energia).
Em energia física clássica é considerado uma quantidade escalar, o conjugado canônica de tempo . Em especial relatividade de energia também é um escalar (embora não seja uma Lorentz escalar, mas um componente de tempo do energia-momentum 4-vector). Em outras palavras, a energia é invariante no que diz respeito às rotações de espaço, mas não invariantes no que diz respeito às rotações de espaço-tempo (= impulsos).
A transferência de energia
Porque a energia é estritamente conservada e também é conservada localmente (onde quer que pode ser definido), é importante lembrar que, por definição, energia de a transferência de energia entre o "sistema" e as regiões adjacentes é de trabalho. Um exemplo conhecido é o trabalho mecânico . Em casos simples, isto é escrito como:
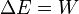 (1)
(1)
Se não houver outros processos de transferência de energia envolvidos. Aqui 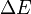 representa a quantidade de energia transferida, e
representa a quantidade de energia transferida, e  representa o trabalho feito no sistema.
representa o trabalho feito no sistema.
De modo mais geral, a transferência de energia pode ser dividida em duas categorias:
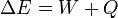 (2)
(2)
onde 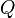 representa o fluxo de calor no sistema.
representa o fluxo de calor no sistema.
Há outras maneiras em que um sistema aberto pode ganhar ou perder energia. Se a massa é contada como energia (como em muitos problemas relativistas), em seguida,  deve conter um prazo para a massa perdeu ou ganhou. Em sistemas químicos, a energia pode ser adicionado a um sistema por meio da adição de substâncias com diferentes potenciais químicos potenciais, que são então extraídos (ambos destes processos são ilustrados, alimentando um automóvel, um sistema que ganha energia deste modo, sem adição de qualquer trabalho ou calor). Winding um relógio seria a adição de energia para um sistema mecânico. Estes termos podem ser adicionados com a equação acima, ou eles podem geralmente ser incluído numa quantidade denominada "termo de adição de energia
deve conter um prazo para a massa perdeu ou ganhou. Em sistemas químicos, a energia pode ser adicionado a um sistema por meio da adição de substâncias com diferentes potenciais químicos potenciais, que são então extraídos (ambos destes processos são ilustrados, alimentando um automóvel, um sistema que ganha energia deste modo, sem adição de qualquer trabalho ou calor). Winding um relógio seria a adição de energia para um sistema mecânico. Estes termos podem ser adicionados com a equação acima, ou eles podem geralmente ser incluído numa quantidade denominada "termo de adição de energia  ", Que se refere a qualquer tipo de energia transportada através da superfície de um sistema de controlo de volume ou de volume. Exemplos pode ser visto acima, e muitos outros podem ser imaginadas (por exemplo, a energia cinética de um fluxo de partículas de entrar um sistema, ou de energia a partir de um feixe de laser aumenta a energia do sistema, sem que nenhum ser tanto ou calor acrescentado, nos sentidos clássicos feito-obra).
", Que se refere a qualquer tipo de energia transportada através da superfície de um sistema de controlo de volume ou de volume. Exemplos pode ser visto acima, e muitos outros podem ser imaginadas (por exemplo, a energia cinética de um fluxo de partículas de entrar um sistema, ou de energia a partir de um feixe de laser aumenta a energia do sistema, sem que nenhum ser tanto ou calor acrescentado, nos sentidos clássicos feito-obra).
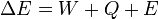 (3)
(3)
Onde E nesta equação geral representa outros termos energéticos advectado adicionais não abrangidas pelo trabalho feito em um sistema, ou calor adicionado a ele.
A energia também é transferido de energia potencial ( 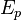 ) Em energia cinética (
) Em energia cinética ( 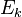 ) E, em seguida, volta para a energia potencial constantemente. Isto é referido como a conservação de energia. Neste sistema fechado, a energia não pode ser criado ou destruído, de modo que a energia inicial e o final de energia irá ser iguais uns aos outros. Isto pode ser demonstrado pelo seguinte:
) E, em seguida, volta para a energia potencial constantemente. Isto é referido como a conservação de energia. Neste sistema fechado, a energia não pode ser criado ou destruído, de modo que a energia inicial e o final de energia irá ser iguais uns aos outros. Isto pode ser demonstrado pelo seguinte:
A equação pode ser simplificada ainda mais, uma vez  (Massa vezes aceleração devida à gravidade vezes a altura) e
(Massa vezes aceleração devida à gravidade vezes a altura) e 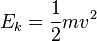 (Meia massa vezes velocidade ao quadrado). Em seguida, a quantidade total de energia pode ser encontrado adicionando
(Meia massa vezes velocidade ao quadrado). Em seguida, a quantidade total de energia pode ser encontrado adicionando 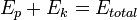 .
.
Energia e as leis do movimento
........................................ Jjj
O Hamiltonian
O total de energia de um sistema é às vezes chamado de Hamiltoniano, depois William Rowan Hamilton. As equações de movimento clássicas pode ser escrito em termos do Hamiltoniano, mesmo para sistemas altamente complexos ou abstratos. Essas equações clássicas têm análogos notavelmente diretos na mecânica quântica não-relativística.
O Lagrangian
Outro conceito relacionado com a energia é chamada de Lagrangian, depois de Joseph Louis Lagrange . Isto é ainda mais fundamental do que o hamiltoniano, e pode ser usado para derivar as equações de movimento. Na física não-relativística, o Lagrangian é a energia cinética de menos energia potencial.
Normalmente, o formalismo de Lagrange é matematicamente mais conveniente do que o Hamiltoniano para sistemas não conservativas (como sistemas com atrito).
Energia e termodinâmica
Energia interna
Energia interna - a soma de todas as formas microscópicas de energia de um sistema. Ela está relacionada com a estrutura molecular e o grau de actividade molecular e pode ser visto como a soma da energia cinética e potencial das moléculas; que compreende os seguintes tipos de energia:
| Tipo | Composição de Interno da Energia (U) |
|---|---|
| Energia Sensible | a porção do energia interna de um sistema associado com energias cinéticas (tradução molecular, rotação e vibração; tradução de elétrons e de spin e spin nuclear) das moléculas. |
| Energia latente | a energia interna associada com a fase de um sistema. |
| Energia química | a energia interna associada com os diferentes tipos de aggregration de átomos em questão . |
| Energia nuclear | a enorme quantidade de energia associada ao ligações fortes dentro do núcleo do próprio átomo. |
| Interações de energia | esses tipos de energias não armazenados no sistema (por exemplo, transferência de calor, transferência de massa, e trabalho ), mas que são reconhecidos no limite do sistema à medida que atravessá-la, o que representa ganhos ou perdas por um sistema durante um processo. |
| Energia térmica | a soma das formas sensível e latente de energia interna. |
As leis da termodinâmica
De acordo com a segunda lei da termodinâmica , o trabalho pode ser totalmente convertida em calor , mas não vice-versa.This é uma consequência matemática da mecânica estatística . A primeira lei da termodinâmica simplesmente afirma que a energia é conservada, e que o calor está incluído como uma forma de transferência de energia. Um corolário comumente usado da primeira lei é que, para um "sistema" sujeitos apenas às forças de pressão e de transferência de calor (por exemplo, um cilindro cheio de gás), a alteração no diferencial de energia do sistema (com um ganho de energia representado por uma quantidade positiva) é dada por:
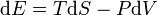 ,
,
onde o primeiro termo à direita é a transferência de calor para o sistema, definida em termos de temperatura T e a entropia S (em que a entropia aumenta e a mudança d S é positiva quando o sistema é aquecido); e o último termo do lado direito é identificado como "trabalho" feito no sistema, em que a pressão é P e volume V (os resultados negativos do sinal uma vez que a compressão do sistema é necessário para fazer o trabalho sobre ele, de modo que a variação do volume d V é negativo quando o trabalho é realizado no sistema). Embora esta equação é o exemplo livro-texto padrão de conservação de energia em termodinâmica clássica, é altamente específico, ignorando todos os químicos, energia elétrica, nuclear, e as forças gravitacionais, efeitos como advecção de qualquer forma de energia que não o calor, e porque contém um termo que depende da temperatura. A declaração mais geral da primeira lei - ou seja, a conservação de energia - é válido, mesmo em situações em que a temperatura é indefinível.
Energia é por vezes expressa como:
 ,
,
que é insatisfatório porque não podem existir quaisquer funções do Estado termodinâmicos W ou Q que são significativas no lado direito desta equação, exceto, talvez, em casos triviais.
Equipartição de energia
A energia de uma mecânica oscilador harmônico (a massa em uma mola) é alternativamente cinética e potencial. Em dois pontos na oscilação ciclo é inteiramente cinética, e alternativamente pelo outros dois pontos é inteiramente potencial. Ao longo de todo o ciclo, ou ao longo de muitos ciclos de energia líquida é, portanto, dividido igualmente entre cinética e potencial. Isto é chamado princípio de equipartição - total de energia de um sistema com muitos graus de liberdade é igualmente dividida entre todos esses graus de liberdade.
Este princípio é de vital importância para a compreensão do comportamento de uma quantidade intimamente relacionada com a energia, chamada entropia . A entropia é uma medida de uniformidade de um distribuição de energia entre as partes de um sistema. Este conceito também está relacionado com a segunda lei da termodinâmica , que basicamente afirma que quando um sistema isolado é dado mais graus de liberdade (= é dado novo disponível estados de energia que são o mesmo que os estados existentes), então a energia se espalha por todos os graus disponíveis igualmente, sem distinção entre "novos" e "antigos" graus.
Osciladores, fônons, e fótons
Em um conjunto (coleção conectado) de osciladores não sincronizadas, a energia média é distribuído igualmente entre os tipos de cinética e potencial.
Em um sólido, energia térmica (muitas vezes referida como frouxamente conteúdo de calor) pode ser descrito com precisão por um conjunto de fonões térmicas que actuam como osciladores mecânicos. Neste modelo, a energia térmica é igualmente cinética e potencial.
Em um gás ideal, o potencial de interacção entre as partículas é essencialmente a função delta que armazena nenhuma energia: assim, toda a energia térmica é cinética.
Porque um oscilador eléctrico (circuito LC) é análoga a um oscilador mecânico, a energia deve ser, em média, igual cinética e potencial. É completamente arbitrária se a energia magnética é considerada cinética e a energia potencial eléctrico considerado, ou vice-versa. Ou seja, ou o indutor é análoga à massa, enquanto o condensador é análoga à da mola, ou vice-versa.
- Por extensão da linha anterior do pensamento, no espaço livre do campo electromagnético pode ser considerado um conjunto de osciladores, o que significa que energia de radiação pode ser considerado igualmente potencial e cinética. Este modelo é útil, por exemplo, quando o Lagrangeanos electromagnética é de interesse primário e é interpretado em termos de energia potencial e cinética.
- Por outro lado, na equação fundamental
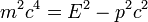 , A contribuição
, A contribuição  é chamado de energia de repouso, e todas as outras contribuições para a energia são chamados de energia cinética. Para uma partícula que tem a massa, isto implica que a energia cinética é
é chamado de energia de repouso, e todas as outras contribuições para a energia são chamados de energia cinética. Para uma partícula que tem a massa, isto implica que a energia cinética é  a velocidades muito menores do que c, como pode ser provada por escrito
a velocidades muito menores do que c, como pode ser provada por escrito 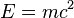 √
√ 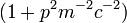 e expandir a raiz quadrada de ordem mais baixa. Por essa linha de raciocínio, a energia de um fóton é inteiramente cinética, porque o fóton é sem massa e não tem energia de repouso. Esta expressão é útil, por exemplo, quando a relação energia-contra-impulso é de interesse primordial.
e expandir a raiz quadrada de ordem mais baixa. Por essa linha de raciocínio, a energia de um fóton é inteiramente cinética, porque o fóton é sem massa e não tem energia de repouso. Esta expressão é útil, por exemplo, quando a relação energia-contra-impulso é de interesse primordial.
As duas análises são inteiramente consistentes. Os graus eléctricos e magnéticos de liberdade no item 1 são transversais à direcção de movimento, enquanto que a velocidade no ponto 2 é ao longo da direcção de movimento. Para as partículas não-relativistas estas duas noções de potencial em função da energia cinética são numericamente iguais, de modo que a ambigüidade é inofensivo, mas não para partículas relativistas.
Trabalho e trabalho virtual
O trabalho é mais ou menos força vezes distância. Mas, mais precisamente, é
Este diz que o trabalho (  ) É igual ao integral (ao longo de um determinado percurso) da força ; para mais detalhes veja o trabalho mecânico artigo.
) É igual ao integral (ao longo de um determinado percurso) da força ; para mais detalhes veja o trabalho mecânico artigo.
Trabalhar e, assim, a energia é enquadrar dependente. Por exemplo, considere uma bola ser atingido por um morcego. No quadro de referência centro de massa, o morcego não faz nenhum trabalho sobre a bola. Mas, no quadro de referência da pessoa balançando o bastão, é feito um trabalho considerável sobre a bola.
Mecânica quântica
No sector da energia mecânica quântica é definida em termos da operador de energia como um derivado do tempo função de onda. O Equação de Schrödinger equivale operador de energia para toda a energia de uma partícula ou um sistema. É, portanto, pode ser considerado como uma definição de medição de energia na mecânica quântica. A equação de Schrödinger descreve o espaço e tempo-dependência da função de onda de sistemas quânticos. A solução dessa equação para o sistema ligado é discreto (um conjunto de estados permitidos, cada uma caracterizada por uma nível de energia), que resulta no conceito de quanta. Na solução da equação de Schrödinger para qualquer oscilador (vibrador) e para ondas eletromagnéticas no vácuo, os estados de energia resultantes estão relacionadas com a frequência pelo Planck equação 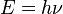 (Onde
(Onde 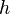 é o E constante de Planck
é o E constante de Planck 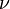 a frequência). No caso da onda eletromagnética esses estados de energia são chamados de quanta de luz ou fótons .
a frequência). No caso da onda eletromagnética esses estados de energia são chamados de quanta de luz ou fótons .
Relatividade
Ao calcular a energia cinética (= trabalhar para acelerar uma massa de zero velocidade para alguma velocidade finita) relativisticamente - usando Transformações de Lorentz, em vez de mecânica newtoniana , Einstein descobriu subproduto inesperado destes cálculos para ser um termo de energia que não desaparece à velocidade zero. Chamou- descanso da massa energia - energia que cada massa deve possuir, mesmo quando estando em repouso. A quantidade de energia é directamente proporcional à massa de corpo:
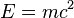 ,
,
onde
- m é a massa,
- c é a velocidade da luz no vácuo,
- E é a energia massa de repouso.
Por exemplo, considere elétron - aniquilação de positrões, em que a massa em repouso de partículas individuais é destruída, mas o equivalente a inércia do sistema das duas partículas (o seu massa invariante) permanece (desde toda a energia está associada a massa), e essa inércia e massa invariante é levado por fótons que são individualmente sem massa, mas como um sistema mantêm a sua massa. Este é um processo reversível - o processo inverso é chamado criação pair - em que a massa restante de partículas é criado a partir da energia de duas (ou mais) aniquilando fótons.
Na relatividade geral, o tensor de tensão-energia serve como o termo de origem para o campo gravitacional, em analogia grosseira com a forma de massa serve como o termo fonte na aproximação newtoniana não relativista.
Não é raro ouvir que a energia é "equivalente" à massa. Seria mais correto afirmar que cada energia tem inércia e gravidade equivalente, e porque a massa é uma forma de energia, em seguida, a massa também tem inércia e gravidade associada a ele.
Medição
Não há medida absoluta de energia, porque a energia é definida como o trabalho que faz um sistema (ou pode fazer) no outro. Assim, apenas a transição de um sistema a partir de um estado para outro pode ser definida e assim medido.
Métodos
Os métodos para a medição de energia muitas vezes implantar métodos para a avaliação de conceitos ainda mais fundamentais da ciência, ou seja, massa , distância , radiação, temperatura , tempo , carga eléctrica e corrente elétrica.

Convencionalmente a técnica mais empregada é calorimetria, a termodinâmica técnica que se baseia na medição da temperatura usando um termómetro ou da intensidade de radiação utilizando um bolómetro.
Unidades
Ao longo da história da ciência, a energia tem sido expressa em várias unidades diferentes, tais como ergs e calorias. Neste momento, a unidade de medição aceite para a energia é a Unidade SI de energia, a joule.
Formas de energia

A mecânica clássica distingue entre energia potencial, que é uma função da posição de um objecto, e a energia cinética , que é uma função do seu movimento . Tanto a posição e movimento são em relação a um quadro de referência, que devem ser especificados: esta é frequentemente (e inicialmente) um ponto fixo arbitrária na superfície da Terra, o quadro de referência terrestre. Alguns autores introdutórios tentar separar todas as formas de energia em qualquer cinética ou potencial: este não é incorreta, mas também não é claro que é uma verdadeira simplificação, como Feynman aponta:
Estas noções de energia potencial e cinética depender de uma noção de escala de comprimento. Por exemplo, pode-se falar do potencial macroscópica e energia cinética, que não incluem o potencial térmico e de energia cinética. Também o que é chamado de energia química potencial (abaixo) é uma noção macroscópica, e um exame mais atento mostra que é realmente a soma da energia potencial e cinética na escala atômica e subatômica. Observações semelhantes aplicam-se a energia nuclear "potencial" e mais outras formas de energia. Esta dependência de escala de comprimento não é problemático se as várias escalas de comprimento são dissociados, como é frequentemente o caso ... mas pode haver confusão quando diferentes escalas de comprimento estão acoplados, por exemplo, quando o atrito converte trabalho macroscópica em energia térmica microscópica.
| A energia mecânica é convertida | |
|---|---|
| em | por |
| Energia mecânica | Alavanca |
| Energia térmica | Freios |
| Energia elétrica | Dínamo |
| Radiação eletromagnética | Síncrotron |
| Energia química | Fósforos |
| Energia nuclear | Acelerador de partículas |
Energia potencial
A energia potencial, os símbolos E P, V ou Φ, é definida como o trabalho realizado contra uma determinada força (= trabalho de determinada força com sinal negativo) na mudança da posição de um objecto com respeito a um ponto de referência (muitas vezes tomado como sendo infinita separação). Se F é a força e s é a deslocamento,
com o ponto que representa o produto escalar dos dois vectores .
O nome energia "potencial" originalmente significava a ideia de que a energia poderia ser facilmente transferido como-no trabalho menos em um sistema idealizado (processo reversível, veja abaixo). Isto não é completamente verdadeiro para qualquer sistema real, mas é muitas vezes uma primeira aproximação razoável na mecânica clássica.
A equação geral acima pode ser simplificada numa série de casos comuns, nomeadamente quando se trata de gravidade ou com forças elásticas .
Energia potencial gravitacional
O força gravitacional perto da superfície da Terra varia muito pouco com a altura, H, e é igual à massa , m, multiplicado pela aceleração gravitacional, g = 9,81 m / s². Nestes casos, a energia potencial gravitacional é dada pela
A expressão mais geral para a energia potencial devido a Gravitação newtoniana entre dois corpos de massas m 1 e m 2, útil na astronomia , é
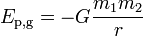 ,
,
em que r é a distância entre os dois corpos e G é a constante gravitacional, 6,6742 (10) 10 -11 × m³kg s -1 -2. Neste caso, o ponto de referência é a separação infinito de os dois corpos.
Energia potencial elástica

A energia potencial elástica é definido como uma obra necessária para comprimir (ou expandir) uma mola. A força, F, numa mola ou qualquer outro sistema que obedeça Lei de Hooke é proporcional à extensão ou compressão, x,
onde k é a a constante de força de mola especial (ou sistema). Neste caso, torna-se o trabalho calculado
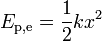 .
.
A lei de Hooke é uma boa aproximação para o comportamento de ligações químicas em condições normais, ou seja, quando eles não estão sendo quebrados ou formado.
Energia cinética
Energia cinética, símbolos E k, T ou K, é o trabalho necessário para acelerar um objeto para uma determinada velocidade. Na verdade, este trabalho calcular facilmente obtém o seguinte:
A velocidades próximas da velocidade da luz , c, este trabalho deve ser calculada utilizando Transformações de Lorentz, o que resulta no seguinte:
Esta equação se reduz ao que está acima dele, na pequena (em comparação com c) velocidade. Um matemático subproduto deste trabalho (que é imediatamente visto na última equação) é que, mesmo em repouso uma massa tem o valor de energia igual a:
Esta energia é assim chamado descansar energia em massa.
Energia térmica
| A energia térmica é convertida | |
|---|---|
| em | por |
| Energia mecânica | Turbina a vapor |
| Energia térmica | Trocador de calor |
| Energia elétrica | Par termoelétrico |
| Radiação eletromagnética | Objetos quentes |
| Energia química | Forno alto |
| Energia nuclear | Supernova |
A definição geral de energia térmica, ou símbolos q Q, também é problemático. A definição prática para pequenas transferências de calor é
em que C é o v capacidade de calor do sistema. Esta definição falhará se o sistema passa por uma fase se o gelo derrete a transição, por exemplo, água-em-que estes casos, o sistema pode absorver calor sem aumentar a sua temperatura. Em sistemas mais complexos, é preferível utilizar o conceito de interno da energia e não o de energia térmica (ver energia química abaixo ).
Apesar dos problemas teóricos, a definição acima é útil na medida experimental de alterações de energia. Em uma grande variedade de situações, é possível usar a energia libertada por um sistema para aumentar a temperatura de um outro objectivo, por exemplo, um banho de água. Também é possível medir a quantidade de a energia eléctrica necessária para elevar a temperatura do objecto pela mesma quantidade. O calorias foi originalmente definida como a quantidade de energia necessária para elevar a temperatura de um grama de água por 1 ° C (cerca de 4,1855 J, embora a definição mais tarde alterado), e aunidade térmica britânica foi definida como a energia necessária para aquecer umgalão (Reino Unido) de água por 1° F (mais tarde fixa como 1055,06 J).
Energia elétrica
| A energia elétrica é convertida | |
|---|---|
| em | por |
| Energia mecânica | Motor elétrico |
| Energia térmica | Resistência |
| Energia elétrica | Transformador |
| Radiação eletromagnética | Diodo emissor de luz |
| Energia química | Eletrólise |
| Energia nuclear | Síncrotron |
O energia potencial elétrico de determinada configuração de encargos é definida como o trabalho que deve ser feito contra a força de Coulomb para reorganizar encargos de separação infinita a esta configuração (ou o trabalho realizado pela força de Coulomb separando os encargos a partir desta configuração para o infinito). Para dois ponto-like encargos Q 1 e Q 2 a uma distância r esse trabalho, e, portanto, energia potencial elétrico é igual a:
onde ε 0 é a constante eléctrica de um vácuo, a 10 7 / 4π c 0 ² ou 8,854188 ... x 10 -12 M / m. Se a carga é acumulada em um capacitor (de capacitância C ), a configuração de referência é geralmente selecionada para não ser separação infinito de cargas, mas vice-versa - encargos em um extremamente estreita proximidade um do outro (assim lá é zero carga líquida em cada placa de um condensador). Neste caso, o trabalho e, consequentemente, a energia potencial eléctrico se torna
Se uma corrente eléctrica passa através de uma resistência, a energia eléctrica é convertida em calor; Se a corrente passa através de um aparelho eléctrico, uma parte da energia eléctrica vai ser convertida em outras formas de energia (embora alguns possam ser sempre perdida na forma de calor). A quantidade de energia eléctrica devido a uma corrente eléctrica pode ser expresso num número de maneiras diferentes:
onde L é a diferença de potencial eléctrico (em volts ), Q é a carga (em coulombs), I é a corrente (em Amperes), t é o tempo durante o qual a corrente flui (em segundos), P é a força (em watts) e R é a resistência eléctrica (em ohms ). A última destas expressões é importante na prática de medição de energia, como diferença de potencial, a resistência e o tempo podem ser medidos com precisão considerável.
A energia magnética
Não há diferença fundamental entre a energia magnética e energia elétrica: os dois fenômenos estão relacionados por equações de Maxwell . A energia potencial de um íman de momento magnético m em um campo magnético B é definida como o trabalho de força magnética (na verdade magnética de torque) em re-alinhamento do vector do momento dipolo magnético, e é igual:
enquanto que a energia armazenada em umindutor (deindutância L) quando a correnteIpassa através do que é
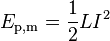 .
.
Esta segunda expressão constitui a base parasupercondutores de armazenamento de energia magnética.
Campos eletromagnéticos
| A radiação eletromagnética é convertido | |
|---|---|
| em | por |
| Energia mecânica | Vela solar |
| Energia térmica | Coletor solar |
| Energia elétrica | Célula solar |
| Radiação eletromagnética | Óptica não-linear |
| Energia química | Fotossíntese |
| Energia nuclear | Espectroscopia Mössbauer |
Calculandoo trabalhonecessário para criar um campo elétrico ou magnético em unidade de volume (por exemplo, em um capacitor ou um indutor) resultados nos campos elétricos e magnéticosdensidades de energia:
e
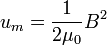 ,
,
em unidades SI.
A radiação eletromagnética, tais como microondas, luz visível ou raios gama, representa um fluxo de energia eletromagnética. Aplicando as expressões acima para componentes eléctricos e magnéticos de campo electromagnético, tanto a densidade volumétrica e o fluxo de energia em E / M campo podem ser calculados. O resultado Poynting vector, que é expressa como
em unidades SI, dá a densidade do fluxo de energia e a sua direcção.
A energia da radiação eletromagnética é quantizado (tem discretos níveis de energia). O espaçamento entre estes níveis é igual
em que h é a Planck constante, 6.6260693 (11) × 10 -34 Js, e ν é a frequência da radiação. Esta quantidade de energia eletromagnética é geralmente chamado de um fóton.Os fotões que compõem a luz visível tem energias de 270-520 YJ, equivalente a 160-310 kJ / mol, a força de mais fracasligações químicas.
Energia química
| A energia química é convertida | |
|---|---|
| em | por |
| Energia mecânica | Músculo |
| Energia térmica | Fogo |
| Energia elétrica | Célula de combustível |
| Radiação eletromagnética | Glowworms |
| Energia química | Reação química |
A energia química é a energia devido à associação de moléculas e átomos em vários outros tipos de agregados de matéria . Pode ser definido como um trabalho feito por forças elétricas durante a re-arranjo de cargas elétricas, elétrons e prótons, em processo de agregação. Se a energia química de um sistema diminui durante uma reacção química, que é transferido para o meio de alguma forma de energia (frequentemente calor ); Por outro lado, se a energia química de um sistema aumenta como um resultado de uma reacção química - é através da conversão de uma outra forma de energia a partir dos arredores. Por exemplo,
- quando doishidrogénioátomos de reagir para formar uma molécula de di-hidrogenofosfato, a energia químicadiminuipor 724 ZJ (aenergia de ligação da ligação H-H);
- quando o electrão é completamente removido a partir de um átomo de hidrogénio, a formação de um ião de hidrogénio (na fase gasosa), a energia químicaaumentapor 2,18 aJ (aenergia de ionização de hidrogénio).
É comum para citar as mudanças na energia química para umamole de a substância em questão: os valores típicos para a mudança na energia química molar durante um intervalo de reacção química a partir de dezenas a centenas de kJ / mol.
A energia química, tal como definido acima, também é referido por químicos como a energia interna, L : tecnicamente, este é medido por manter o volume do sistema de a constante. No entanto, a química mais prático é realizado a uma pressão constante e, se as alterações de volume durante a reacção (por exemplo, um gás é desprendido), uma correcção deve ser aplicada para ter em conta o trabalho feito por ou a atmosfera para se obter a entalpia , H :
- ΔH= ΔL+pΔV
Uma segunda correcção, para a mudança deentropia,S, devem também ser realizados para determinar se uma reacção química irá ocorrer ou não, com aenergia livre de Gibbs,G:
- ΔL= ΔH-TΔS
Estas correcções são, por vezes insignificante, mas muitas vezes não (especialmente em reações envolvendo gases).
Desde a revolução industrial , a queima de carvão , petróleo, gás natural ou produtos deles derivados tem sido uma transformação socialmente significativa de energia química em outras formas de energia. o "consumo" de energia (um realmente deve falar de "transformação de energia") de uma sociedade ou país é frequentemente citado em referência à energia média liberado pela queima desses combustíveis fósseis :
- 1 tonelada de carvão equivalente (TCE) = 29 GJ
- 1 tonelada equivalente de petróleo (tep) = 41,87 GJ
Na mesma base, um tanque cheio de gasolina (45 litros, 12 litros) é equivalente a cerca de 1,6 GJ de energia química. Outra unidade com base em química de medida de energia é a "tonelada de TNT ", tomado como 4.184 GJ. Assim, a queima de uma tonelada de liberações de petróleo, cerca de dez vezes mais energia do que a explosão de uma tonelada de TNT: felizmente, a energia é liberada normalmente de uma forma mais lenta, mais controlada.
Exemplos simples de energia química são baterias e alimentos. Ao comer o alimento é digerido e transformado em energia química que pode ser transformada em energia cinética.
Energia nuclear
| Energia de ligação nuclear é convertida | |
|---|---|
| em | por |
| Energia mecânica | A radiação alfa |
| Energia térmica | Sol |
| Energia elétrica | Radiação beta |
| Radiação eletromagnética | A radiação gama |
| Energia química | Decaimento radioativo |
| Energia nuclear | Isomeria nuclear |
Energia potencial nuclear , juntamente com a energia potencial elétrica, fornece a energia liberada a partir de fissão nuclear e processos de fusão nuclear. O resultado de ambos os processos são núcleos em que forças nucleares fortes ligam partículas nucleares mais fortemente e de perto. forças nucleares fracas (diferentes das forças fortes) fornecer a energia potencial de certos tipos de decaimento radioativo, como decaimento beta. A energia liberada em processos nucleares é tão grande que a mudança relativista em massa (após a energia ter sido removida) pode ser tanto quanto várias partes por mil.
Partículas nucleares ( nucleons) como prótons e nêutrons são não destruído (lei de conservação de número baryon) nos processos de fissão e fusão. Algumas partículas mais leves pode ser criada ou destruída (exemplo: menos beta e beta mais decadência, ou captura de elétrons decadência), mas estes processos menores não são importantes para a libertação de energia imediata em fissão e fusão. Em vez disso, a fissão ea fusão liberam energia quando coleções de bárions tornar-se mais ligado, e é a energia associada com uma fração da massa dos nucleons (mas não as partículas inteiras) que figura como o calor e radiação electromagnética gerada por reações nucleares . Este calor e radiação retém a massa "em falta", mas a massa está ausente só porque escapa sob a forma de calor e de luz, que retêm a massa e conduzi-la para fora do sistema em que não é medido. A energia do Sol , também chamado de energia solar , é um exemplo desta forma de conversão de energia. Na Sun , o processo de fusão do hidrogênio converte cerca de 4 milhões de toneladas de matéria solar por segundo para a luz, que é irradiado para o espaço, mas durante este processo, o número total de prótons e nêutrons no sol não muda. Neste sistema, a própria luz retém o equivalente de inércia da massa, e de facto da própria massa (tal como um sistema), que representa 4 milhões de toneladas por segundo de radiação electromagnética, que se deslocam no espaço. Cada um dos núcleos de hélio, que são formadas no processo são menos massa do que os quatro protões a partir de que foram formados, mas (para uma boa aproximação), não há partículas ou átomos são destruídos no processo de transformar energia potencial nuclear do sol para a luz.
Energia superficial
Se houver qualquer tipo de tensão numa superfície, tal como uma folha esticada de interfaces de borracha ou de material, é possível definir energia superficial . Em particular, qualquer reunião de materiais dissimilares que não se misturam irá resultar em algum tipo de tensão de superfície , se houver liberdade para mover as superfícies em seguida, como pode ser visto em superfícies capilares, por exemplo, irá ser procurada como de costume a energia mínima.
A de superfície mínima, por exemplo, representa a menor energia possível que uma superfície se pode ter a sua energia é proporcional à área da superfície. Por esta razão, (abertos) filmes de sabão de tamanho pequeno são superfícies mínimas (tamanho pequeno reduz os efeitos da gravidade, e da abertura de pressão impede que se acumule. Note-se que uma bolha é uma superfície de energia mínima, mas não é uma superfície mínima, por definição).
Transformações de energia
Uma forma de energia pode muitas vezes ser facilmente transformada em uma outra com a ajuda de um dispositivo- por exemplo, uma bateria, de energia química em energia eléctrica; uma barragem : a energia potencial gravitacional para energia cinética do movimento da água (e as pás de uma turbina) e, finalmente, a energia eléctrica através de um gerador eléctrico. Da mesma forma, no caso de uma explosão química, energia potencial químico é transformado em energia cinética e a energia térmica em um tempo muito curto. Ainda um outro exemplo é a de um pêndulo. Em seus pontos mais altos da energia cinética é zero ea energia potencial gravitacional é, no máximo. No seu ponto mais baixo da energia cinética está no máximo e é igual à redução de energia potencial. Se um (irrealisticamente) assume que não existe atrito, a conversão de energia entre estes processos é perfeita, e o pêndulo vai continuar balançando para sempre.
A energia pode ser convertida em matéria e vice-versa. O fórmula de equivalência massa-energia E = mc ², derivado de forma independente por Albert Einstein e Henri Poincaré, quantifica a relação entre massa e energia descansar. Desde 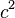 é extremamente grande em relação às escalas humanos comuns, a conversão de massa a outras formas de energia pode liberar enormes quantidades de energia, como pode ser visto em reatores nucleares e armas nucleares. Por outro lado, a massa equivalente de uma unidade de energia é minúscula, que é por isso uma perda de energia da maioria dos sistemas é difícil de medir, em peso, a menos que a perda de energia é muito grande. Exemplos de transformação de energia na matéria (partículas) são encontrados em alta energia física nuclear .
é extremamente grande em relação às escalas humanos comuns, a conversão de massa a outras formas de energia pode liberar enormes quantidades de energia, como pode ser visto em reatores nucleares e armas nucleares. Por outro lado, a massa equivalente de uma unidade de energia é minúscula, que é por isso uma perda de energia da maioria dos sistemas é difícil de medir, em peso, a menos que a perda de energia é muito grande. Exemplos de transformação de energia na matéria (partículas) são encontrados em alta energia física nuclear .
Na natureza, as transformações de energia pode ser fundamentalmente classificada em dois tipos: aqueles que são termodinamicamente reversível, e aqueles que são termodinamicamente . irreversível A processo reversível em termodinâmica é aquele em que nenhuma energia é dissipada em estados quânticos vazios disponíveis em um volume, a partir dos quais ele não pode ser recuperado em formas mais concentradas (menos estados quânticos), sem degradação de ainda mais energia. Um processo reversível é aquele em que este tipo de dissipação não acontece. Por exemplo, a conversão de energia a partir de um tipo de campo potencial para outro, é reversível, como no sistema de pêndulo descrito acima. Em processos nos quais o calor é gerado, no entanto, afirma quantum de energia mais baixa, apresentam como possíveis exitations em campos entre os átomos, actuam como um reservatório para a parte da energia, a partir da qual ele não pode ser recuperada, a fim de ser convertido com uma eficiência de 100% em outras formas de energia. Neste caso, a energia deve ficar parcialmente na forma de calor, e não pode ser totalmente recuperado como energia utilizável, excepto à custa de um aumento em algum outro tipo de aumento semelhante de calor em desordem em estados quânticos, no universo (tal como um expansão de matéria, ou uma randomização em um cristal).
Como o universo evolui com o tempo, mais e mais de sua energia fica preso em estados irreversíveis (ou seja, como calor ou outros tipos de aumentos de desordem). Isto tem sido referido como a termodinâmica inevitável morte térmica do universo. Neste aquecer morte a energia do universo não muda, mas a fração da energia que está disponível para fazer o trabalho, ou ser transformada em outras formas utilizáveis de energia, cresce menos e menos.
Lei da conservação da energia
Energia está sujeita à lei da conservação da energia . De acordo com esta lei, a energia não pode ser criada (produzido), nem se destruiu. Ela só pode ser transformado.
A maioria dos tipos de energia (com a energia gravitacional sendo uma notável exceção) também estão sujeitos a rigorosas leis de conservação locais, bem. Neste caso, a energia só podem ser trocadas entre as regiões adjacentes de espaço, e todos os observadores concordam quanto à densidade volumétrica de energia num determinado espaço. Há também uma lei global de conservação de energia, afirmando que a energia total do universo não pode mudar; este é um corolário da lei local, mas não vice-versa. Conservação de energia é a consequência matemática da simetria translacional de tempo (isto é, o indistinguibilidade de intervalos de tempo tomadas em tempo diferente) - veja Teorema de Noether.
Conforme lei da conservação de energia a entrada total de energia para um sistema de escoamento deve ser igual ao total de energia do sistema, além da mudança na energia contida no interior do sistema.
Esta lei é um princípio fundamental da física. Daqui resulta a partir da simetria translacional de tempo , uma propriedade da maioria dos fenômenos abaixo da escala cósmica que os torna independente de suas localizações no tempo de coordenadas. Dito de outro modo, ontem, hoje e amanhã são fisicamente indistinguíveis.
Assim porque a energia é a quantidade que é conjugado canônica tempo, é impossível definir a quantidade exata de energia durante qualquer intervalo de tempo definido - o que torna impossível aplicar a lei da conservação da energia. Isto não deve ser considerado uma "violação" da lei. Sabemos que a lei ainda se mantém, porque uma sucessão de curtos períodos de tempo não acumular qualquer violação da conservação da energia.
Na mecânica quântica energia é expressa usando o hamiltoniano operador. Em quaisquer escalas de tempo, a incerteza na energia é de
que é semelhante em forma ao Heisenbergprincípio da incerteza (mas não realmente matematicamente equivalente aos mesmos, uma vez queHetnão são dinamicamente variáveis conjugadas, nem no clássico nem na mecânica quântica).
Emfísica de partículas, esta desigualdade permite uma compreensão qualitativa departículas virtuais que transportamimpulso, troca pelo qual e com partículas reais, é responsável pela criação de todas as conhecidasforças fundamentais (mais precisamente conhecido comointerações fundamentais).fótons virtuais (que são simplesmente menor mecânica quânticaestado de energia dosfótons) também são responsáveis pela interação eletrostática entrecargas elétricas(o que resulta emlei de Coulomb), pordecaimento radiativo espontânea de estados atômicos e nucleares saíram, para aforça de Casimir, porforças de van der Waals obrigacionistase alguns outros fenômenos observáveis.
Energia e vida
Qualquer organismo vivo depende de uma fonte externa de energia por radiação do Sol, no caso de plantas verdes; energia química de alguma forma, no caso de animais de ser capaz de crescer e reproduzir-se. As diárias 1500-2000 calorias (6-8 MJ) recomendadas para um adulto humano são tomadas como uma combinação de moléculas de oxigénio e de alimentos, este último principalmente hidratos de carbono e gorduras, dos quais glucose (C 6 H 12 O 6 ) e de estearina (C 57 H 110 O 6 ) são exemplos convenientes. As moléculas de alimento são oxidados para o dióxido de carbono e água nas mitocôndrias
- C6H12O6+ 6O2→ 6CO2+ 6H2O
- C57H110O6+ 81.5O2→ 57Co2+ 55H2O
e uma parte da energia é utilizada para converterADP emATP
- ADP + HPO4 2-→ ATP + H2ó
O resto da energia química na gordura ou hidrato de carbono é convertido em calor: o ATP é utilizado como uma espécie de "moeda de energia", e uma parte da energia química que contém de divisão e quando feita reagir com água, é usado para a outra metabolismo ( em cada fase de uma via metabólica, um pouco de energia química seja convertida em calor). Apenas uma pequena fração da energia química original é usado para o trabalho:
- ganhar em energia cinética de um velocista durante uma corrida de 100 m: 4 kJ
- ganhar em energia potencial gravitacional de um peso 150 kg levantou através de 2 metros: 3KJ
- A ingestão diária de um adulto normal: 6-8 MJ
Afigura-se que os organismos vivos são notavelmente ineficientes (no sentido físico) em seu uso da energia que recebem (energia química ou radiação), e é verdade que a maioria dos reais máquinas de gerenciar uma maior eficiência. No entanto, no crescimento de organismos a energia que é convertida em calor serve um propósito fundamental, uma vez que permite que o tecido organismo a ser altamente ordenada no que diz respeito às moléculas de que é construída a partir de. A segunda lei da termodinâmica estabelece que a energia (e matéria) tende a tornar-se mais uniformemente espalhados por todo o universo: para concentrar a energia (ou matéria) em um lugar específico, é necessário para se espalhar uma quantidade maior de energia (como o calor) através do restante do universo ("o ambiente"). Organismos mais simples podem alcançar eficiências de energia mais elevados do que outros mais complexos, mas os organismos complexos podem ocupar nichos ecológicos que não estão disponíveis para seus irmãos mais simples. A conversão de uma parte da energia química ao calor em cada etapa de uma via metabólica é a razão física atrás da pirâmide de biomassa observada em ecologia : tomar apenas o primeiro passo na cadeia alimentar, a estimativa de 124,7 pg / um de carbono que é fixado por fotossíntese , 64,3 pg / A (52%) são utilizadas para o metabolismo das plantas verdes, ou seja reconvertido em dióxido de carbono e de calor.