
Estrôncio
Você sabia ...
Crianças SOS, que corre cerca de 200 sos escolas no mundo em desenvolvimento, organizado esta selecção. Um link rápido para o patrocínio criança é http://www.sponsor-a-child.org.uk/
| Estrôncio | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
38 Sr | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aparência | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
metálico branco prateado  | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades gerais | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nome, símbolo, número | estrôncio, Sr, 38 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pronúncia | / s t r ɒ n ʃ ⁱ ə m / -sh Stron (ee) -əm; / s t r ɒ n t Eu ə m / Stron -tee-əm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Categoria elemento | metal alcalino-terroso | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo, período, bloco | (2) de metais alcalino-terrosos , 5, s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Peso atômico padrão | 87.62 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuração eletrônica | [ Cr ] 5s 2 2, 8, 18, 8, 2  | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| História | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Descoberta | William Cruickshank (1787) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Primeiro isolamento | Humphry Davy (1808) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades físicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase | sólido | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidade (perto RT) | 2,64 g cm -3 · | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Líquido densidade no pf | 2,375 g · cm -3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto de fusão | 1050 K , 777 ° C, 1431 ° F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto de ebulição | 1655 K, 1382 ° C, 2520 ° F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor de fusão | 7,43 kJ mol -1 · | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor de vaporização | 136,9 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacidade calorífica molar | 26,4 J · · mol -1 K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressão de vapor | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades atômicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estados de oxidação | 2, 1 (fortemente óxido de base) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eletronegatividade | 0,95 (escala de Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energias de ionização | 1º: 549,5 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2: 1064,2 kJ · mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3: 4138 kJ · mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raio atômico | 215 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| O raio de covalência | 195 ± 22:00 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals raio | 249 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscelânea | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A estrutura de cristal | cúbica de face centrada  | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordenamento magnético | paramagnético | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Resistividade elétrica | (20 ° C) 132 Nco · m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Condutividade térmica | 35,4 W · m -1 · K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Expansão térmica | (25 ° C) de 22,5 pM · · K -1 m -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| O módulo de Young | 15,7 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Módulo de cisalhamento | 6,03 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rácio de Poisson | 0.28 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureza de Mohs | 1,5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Número de registo CAS | 7440-24-6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A maioria dos isótopos estáveis | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ver artigo principal: Isótopos de estrôncio | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Estrôncio (pron .: / s t r ɒ n t Eu ə m / Stron -tee-əm) é um elemento químico com o símbolo Sr e número atômico 38. Um metal alcalino-terroso , o estrôncio é um elemento metálico de prata-branco ou amarelado macio que é altamente reactivo quimicamente. O metal torna-se amarela quando exposta ao ar. O estrôncio tem propriedades físicas e químicas similares aos seus dois vizinhos cálcio e bário. Ocorre naturalmente nos minerais celestine e strontianite. Enquanto estrôncio natural é estável, o sintética 90 Sr isótopo está presente em radioativo precipitação e tem uma meia-vida de 28,90 anos.
Ambos estrôncio e strontianite são nomeados após Strontian, uma aldeia na Escócia perto da qual o mineral foi descoberto pela primeira vez em 1790 por Crawford e Adair William Cruickshank. A produção de açúcar a partir de beterraba sacarina foi no século 19 o maior aplicação. Compostos de estrôncio são hoje utilizado principalmente para a produção de tubos de raios catódicos. O deslocamento de tubos de raios catódicos por outros métodos de exibição em aparelhos de televisão está mudando o consumo geral.
Características

O estrôncio é um metal cinzento, prateado que é mais suave do que o cálcio e ainda mais reactivos com água , com a qual ele reage em contato para produzir hidróxido de estrôncio e hidrogênio do gás. Ele queima no ar para produzir tanto e óxido de estrôncio nitreto de estrôncio, mas uma vez que não reagem com azoto abaixo de 380 ° C, à temperatura ambiente, ele só irá formar o óxido espontaneamente. Três allotropes de estrôncio metálico existir, com pontos de transição em 235 e 540 ° C.
Devido à sua extrema reactividade com o oxigénio e água, este elemento ocorre naturalmente somente em compostos com outros elementos, tais como nos minerais strontianite e celestite. Ele é mantido sob um hidrocarboneto líquido, tal como óleo mineral ou querosene para evitar oxidação; recém exposta do metal estrôncio transforma rapidamente um cor amarelada, com a formação de óxido. Finamente estrôncio em pó de metal é significando pyrophoric ele vai inflamar espontaneamente no ar à temperatura ambiente. Sais de estrôncio voláteis conferir um brilhante de cor vermelha para as chamas , e estes sais são utilizados em pirotecnia e na produção de flares. Estrôncio natural é uma mistura de quatro estáveis isótopos .
História
Estrôncio é nomeado após a vila escocesa de Strontian (gaélico SRON uma t-Sithein), tendo sido descoberto nos minérios retirados das minas de chumbo lá. Em 1790, Adair Crawford, um médico que trabalha na preparação de bário, e seu colega William Cruickshank, reconheceu que os minérios Strontian propriedades que diferiam dos normalmente visto em outros "longarinas pesados" fontes exibido. Isto permitiu Adair concluir na página 355 "... é provável, de fato, que o mineral scotch é uma nova espécie de terra que não tenha até agora sido suficientemente analisados." O coletor médico e mineral Friedrich Gabriel Sulzer analisadas em conjunto com Johann Friedrich Blumenbach o mineral de Strontian e nomeou-strontianite. Ele também chegou à conclusão de que era distinta da witherite e continha uma nova terra (neue Grunderde). Em 1793 Thomas Charles Hope, professor de química na Universidade de Glasgow propôs o nome strontites. Ele confirmou que o trabalho anterior de Crawford e contou: "... Considerando que a terra peculiar, julguei necessário para dar-lhe um nome que eu tê-lo chamado Strontites, a partir do local onde foi encontrado, um modo de derivação na minha opinião,. plenamente como adequada como qualquer qualidade pode possuir, que é a moda atual. " O elemento foi finalmente isolado por Sir Humphry Davy em 1808 pela eletrólise de uma mistura contendo e cloreto de estrôncio óxido de mercúrio, e anunciado por ele em uma palestra para a Royal Society em 30 de junho de 1808. De acordo com a nomenclatura dos outros terrosos, ele mudou o nome para estrôncio.
A primeira aplicação em grande escala de estrôncio foi na produção de açúcar a partir de beterraba sacarina . Apesar de um hidróxido de estrôncio processo de cristalização utilizando foi patenteado por Augustin-Pierre Dubrunfaut em 1849 a introdução em grande escala veio com a melhoria do processo no início dos anos 1870. A indústria do açúcar alemã usou o processo até o século 20. Antes da Primeira Guerra Mundial a indústria de açúcar de beterraba utilizada 100.000 a 150.000 toneladas de hidróxido de estrôncio para este processo por ano. O hidróxido de estrôncio foi reciclado no processo, mas a demanda para perdas de substituição durante a produção foi alta o suficiente para criar uma demanda significativa de iniciar mineração de no strontianite Münsterland. A mineração de strontianite na Alemanha terminou quando a mineração dos depósitos em celestite Gloucestershire iniciado. Estas minas fornecido a maior parte do fornecimento de estrôncio mundo de 1884 a 1941. Embora os depósitos celestite no Bacia Granada foram conhecidos há algum tempo a mineração em grande escala não começou antes de 1950.
Durante a atmosférica armas nucleares de teste, observou-se que o estrôncio-90 é um dos mais produtos de fissão nuclear com um elevado rendimento relativo. A semelhança com o cálcio ea chance de que o estrôncio-90 pode se tornar enriquecido em ossos feitas pesquisas sobre o metabolismo de estrôncio um tópico importante.
Ocorrência
Estrôncio comumente ocorre na natureza, o 15º mais elemento abundante na Terra, estima-se que em média cerca de 360 partes por milhão na Crosta terrestre e é encontrado principalmente como a forma de o sulfato de mineral celestita (SrSO 4) e o carbonato strontianite (SrCO3). Dos dois, celestite ocorre muito mais frequentemente em depósitos sedimentares de tamanho suficiente para tornar o desenvolvimento de instalações de mineração atraente. Porque o estrôncio é utilizado na maioria das vezes sob a forma de carbonato, strontianite seria o mais útil dos dois minerais comuns, mas alguns depósitos foram descobertos que são adequados para o desenvolvimento.
O teor de estrôncio média da água do oceano é de 8 mg / l. A uma concentração entre 82 e 90 umol / l de estrôncio é considerável a concentração mais baixa do que a concentração de cálcio, que é normalmente entre 9,6 e 11,6 mmol / l.
Produção
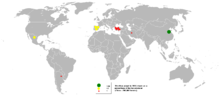
De acordo com Pesquisa Geológica Britânica, a China foi o maior produtor de estrôncio em 2007, com mais de dois terços share mundial, seguido pela Espanha, México, Turquia, Argentina, e do Irã.
Grandes quantidades de a minado celestita (SrSO 4) são convertidos para o carbonato por dois processos. Ou o celestita está directamente lixiviado com uma solução de carbonato de sódio ou o celestita é torrado com o carvão para formar o sulfureto. O segundo processo resulta um material de cor escura contendo sulfeto principalmente de bário. Este assim chamado cinza negra é dissolvido em água e filtrou-se. Carbonato de bário é precipitado a partir da solução de sulfureto de bário por introdução de dióxido de carbono. O sulfato é reduzida para o sulfureto pela redução carbotérmica:
- SrSO 4 + C → SrS + 2 CO 2
Cerca de 300.000 toneladas são processados desta maneira anualmente.
O metal é produzido comercialmente através da redução de estrôncio com óxido de alumínio . O estrôncio é destilada a partir da mistura. O estrôncio metálico pode em princípio ser preparadas por electrólise de uma solução de cloreto de estrôncio no fundido cloreto de potássio:
- Sr 2+ + 2 e - → Sr
- 2 Cl - → Cl 2 + 2 e -
Isótopos
O estrôncio tem quatro estáveis, que ocorrem naturalmente isótopos : 84 Sr (0,56%), 86 Sr (9,86%), 87 Sr (7,0%) e 88 Sr (82,58%). Apenas 87 Sr é radiogenic; é produzido pela decomposição do metal alcalino radioactivo 87 Rb , que tem uma meia-vida de 4,88 × 10 10 anos. Assim, existem duas fontes de 87 Sr em qualquer material: a primeira porção formada em estrelas, juntamente com os isótopos 84 Sr Sr, 86, 88 e Sr; e segundo a parcela formada por decaimento radioativo do 87 Rb. O Sr proporção 87/86 Sr é o parâmetro tipicamente relatada em geológicos investigações; proporções em minerais e rochas tem valores que variam entre cerca de 0,7 e maior do que 4,0. Porque tem um estrôncio raio atómico semelhante ao do cálcio , que facilmente substitui Ca em minerais .
Dezesseis isótopos instáveis são conhecidos de existir. De maior importância são 90 Sr com uma meia-vida de 28,78 anos e 89 Sr com uma semi-vida de 50,5 dias. 90 Sr é um subproduto da fissão nuclear encontrada no precipitação nuclear e apresenta um problema de saúde, uma vez que substitui o cálcio em osso, impedindo a expulsão do corpo. Este isótopo é um dos melhores alta-energia de longa duração emissores beta conhecidos, e é usado em SNAP ( Sistemas para aparelhos Nuclear auxiliar de energia). Estes dispositivos são promissores para uso em nave espacial, estações meteorológicas remotas, bóias de navegação, etc., onde é necessária uma fonte de vida longa de pouco peso,, nuclear-elétrico de potência. O acidente nuclear de Chernobyl em 1986 contaminado uma vasta área com 90 Sr. 90 Sr confinado dentro de uma placa de prata côncava também é usado para o tratamento médico de um ressecado pterígio.
89 Sr é um radioisótopo de vida curta artificial que é utilizado no tratamento de câncer ósseo. Nos casos em que pacientes de câncer têm óssea generalizada e dolorosa metástases (secundários), a administração de 89 resultados Sr na entrega das emissões radioactivas ( partículas beta, neste caso) diretamente para a área de problema ósseo (cálcio, onde o volume de negócios é o maior). O Sr 89 é fabricado como o sal cloreto (que é solúvel), e quando dissolvido em solução salina normal pode ser injectado por via intravenosa. Tipicamente, os pacientes de cancro será tratado com uma dose de 150 MBq. Os pacientes devem tomar precauções seguintes isto porque sua urina torna-se contaminado com radioatividade, para que eles devem sentar-se para urinar e double-puxar o autoclismo. O partículas beta viajar cerca de 3,5 mm de osso (energia 0.583 MeV) e 6,5 mm de tecido, por isso não há necessidade de isolar os pacientes terem sido tratados, exceto para dizer que eles não devem ter qualquer um (especialmente crianças) que senta-se no colo de 10-40 dias. A variação no tempo resulta a partir do momento de compensação variável para 89 Sr, que depende da função renal e o número de metástases ósseas. Com uma grande quantidade de metástases ósseas, a totalidade da dose 89 Sr pode ser levado para o osso e assim a radioactividade retida é a decair mais de uma meia-vida de 50,5 dias. Demora cerca de 10 meias-vidas ou cerca de 500 dias para 99,9% do estrôncio radioativo à deterioração. No entanto, onde há poucas metástases ósseas, a grande proporção de Sr 89 não ocupado pelo osso vai ser filtrado pelo rim, a fim de que a meia-vida eficaz (uma combinação de a semi-vida física e biológica) será muito mais mais curto.
Aplicações

Consumir 75% da produção, o principal uso para o estrôncio é em vidro para cor televisão tubos de raios catódicos. Ela impede Emissão de raios-X. Todas as partes do tubo CRT tem que absorvem os raios X. No pescoço do funil e do tubo, de vidro de chumbo é utilizado para este fim, mas este tipo de vidro mostra um efeito de escurecimento devido à interacção dos raios X com o vidro. Portanto, o painel frontal tem de utilizar uma mistura de vidro diferente, em que o estrôncio e bário são os materiais de absorção de raios-X. Os valores médios para a mistura vidro determinado para um estudo sobre a reciclagem em 2005 é de 8,5% óxido de estrôncio e 10% óxido de bário. A quantidade de estrôncio utilizado para a produção de tubo de raios catódicos é decrescente porque os CRTs são substituídos por outros métodos de apresentação. Esta descida tem uma influência significativa sobre a mineração e refino de estrôncio.
Pirotecnia
Carbonato de estrôncio ou outros estrôncio sais são usados no fabrico de fogos, em que conferem uma cor vermelho escuro para o fogo de artifício. Este aplicativo consome cerca de 5% da produção mundial.
Usa para estrôncio radioativo
89 Sr é o ingrediente activo em Metastron (a versão genérica de Metastron, genérica cloreto de estrôncio Sr-89 de injecção, a sua fabricado pela Bio-Nucleonics Inc.), uma radiofármaco utilizado para dor óssea secundária a metastático câncer ósseo. O estrôncio actua como cálcio e está preferencialmente incorporado no osso em locais de aumento osteogênese. Esta localização concentra-se a exposição a radiação na lesão cancerosa.

90 Sr tem sido usado como uma fonte de energia para geradores de radioisótopos termelétricos (RTGs). 90 Sr produz cerca de 0,93 watts de calor por grama (que é menor para a forma de 90 Sr usado em RTGs, que é fluoreto de estrôncio). No entanto, 90 Sr tem uma duração de aproximadamente 3 vezes mais curto e tem uma densidade mais baixa do que 238 Pu, outro combustível RTG. A principal vantagem de 90 Sr é que é mais barato do que 238 Pu e é encontrado em resíduos nucleares. União Soviética implantou cerca de 1.000 desses RTGs na costa norte como fonte de energia para faróis e estações de meteorologia.
Sr 90 também é utilizado em cancro da terapia. Sua emissão beta e meia-vida longa é ideal para superficial radioterapia.
Porque estrôncio é tão semelhante ao cálcio, é incorporado no osso. Todos os quatro são incorporados isótopos estáveis, em proporções mais ou menos semelhantes, como são encontradas na natureza. No entanto, a actual distribuição dos isótopos tende a variar muito de uma localização geográfica para outra. Assim, analisando o osso de um indivíduo pode ajudar a determinar a região de onde veio. Essa abordagem ajuda a identificar os padrões de migração antigos, bem como a origem do ser humano misturados permanece no campo de batalha locais de sepultamento. Estrôncio, assim, ajuda a cientistas forenses também.
87 Sr / 86 Sr rácios são comumente usados para determinar as áreas prováveis de proveniência de sedimentos em sistemas naturais, especialmente em ambientes marítimos e fluviais. Dasch (1969) mostrou que os sedimentos superficiais do Atlântico exibidos 87 Sr / 86 Sr índices que poderiam ser consideradas como médias em massa de 87 Sr / 86 Sr rácios de terrenos geológicos do continente adjacente. Um bom exemplo de um sistema flúvio-marinha para que estudos de proveniência de isótopos de Sr têm sido empregados com sucesso é o sistema-Mediterrânica Rio Nilo, devido às diferentes idades das rochas que constituem a maioria da azul e branca do Nilo, áreas de captação do mudando proveniência de sedimentos atingindo o delta do rio Nilo e do Leste Mar Mediterrâneo podem ser discernidos através de estudos isotópicos Sr. Tais mudanças são climaticamente controlada na tarde Quaternário.
Mais recentemente, 87 Sr / 86 Sr rácios também têm sido usados para determinar a origem de materiais arqueológicos, tais como madeiras e milho em Chaco Canyon, no Novo México. 87 Sr / 86 Sr rácios em dentes também pode ser usado para rastrear as migrações animais ou em perícia criminal.
Aplicações de nicho
Cloreto de estrôncio é por vezes usado em cremes dentais para dentes sensíveis. Uma marca popular inclui 10% hexahydrate total de cloreto de estrôncio em peso.
Pequenas quantidades são usados na refinação de zinco, para remover pequenas quantidades de impurezas de chumbo.
Tendências de pesquisa
Outras aplicações possíveis seguir:
- Titanato de estrôncio tem um extremamente alto índice de refracção e um dispersão óptica maior do que a de diamante , tornando-se úteis numa variedade de aplicações ópticas. Essa qualidade também levou ao seu corte estar em pedras preciosas, em particular, como um simulador de diamante. No entanto, é muito suave e facilmente arranhões de modo que é raramente usada.
- Ímãs de ferrite.
- Aluminato de estrôncio é utilizado como um branco brilhante fósforo com longa persistência de fosforescência.
- Óxido de estrôncio é, por vezes, utilizados para melhorar a qualidade de alguns cerâmica esmaltes.
- O ranelato de estrôncio é utilizado no tratamento da osteoporose. É um medicamento de prescrição na UE, mas não nos EUA.
- Estrôncio niobato de bário podem ser usados ao ar livre em ecrãs 3D holográficas como uma "tela".
O estrôncio metálico é utilizado em estrôncio 90% 10% alumínio- ligas de um composição eutética para a modificação de ligas de fundição de alumínio-silício. AJ62, um bem durável, resistente ao creep- liga de magnésio utilizado em motores de carros e motos por BMW, contém 2% de estrôncio em peso.
O estrôncio é utilizado em estudos científicos de liberação de neurotransmissores nos neurônios. Como o cálcio, estrôncio facilita fusão das vesículas sinápticas com a membrana sináptica. Mas, ao contrário do cálcio, estrôncio provoca a fusão das vesículas assíncrona. Por conseguinte, a substituição de cálcio em um meio de cultura com estrôncio permite aos cientistas para medir os efeitos de um único evento de fusão de vesículas, por exemplo, o tamanho da resposta pós-sináptica eliciada pelo neurotransmissor conteúdo de uma única vesícula.
O conceito importante para o rastreio isotópica é que Sr derivado de qualquer mineral por meio de reacções que resistem terá o mesmo 87 Sr / 86 Sr como o mineral. Portanto, as diferenças de 87 Sr / 86 Sr entre as águas subterrâneas exigem tanto (a) diferenças na mineralogia contrastante ao longo flowpaths ou (b) diferenças nas quantidades relativas de Sr resistido a partir do mesmo conjunto de minerais. Esta última situação pode surgir de várias formas. Em primeiro lugar, as diferenças na composição química da água inicial dentro de uma unidade de rocha homogênea vai afetar as taxas de intemperismo relativos dos minerais. Por exemplo, as secções da zona do solo afectado pela concentração por evaporação das águas de recarga ou por diferenças em pCO 2 pode-se esperar que têm diferentes 87 Sr / 86 Sr. Em segundo lugar, as diferenças nas mobilidades relativas de água em escalas que vão de poros inter-grão à escala de captação também pode afectar profundamente a 87 Sr / 86 Sr (Bullen et al., 1996). Por exemplo, a composição química e a resultante 87 Sr / 86 Sr em águas imóveis em um limite de grão plagioclase-horneblenda contra um limite de quartzo-mica será diferente. Em terceiro lugar, a diferença em relação às áreas de superfície "eficaz" de minerais em uma porção da unidade de rocha também causará diferenças de composição química e isotópica; "Envenenamento" de superfícies reactivas por revestimentos orgânicos é um exemplo deste tipo de processo. Em um sentido fundamental, porque as águas rasas em sistemas não estão em equilíbrio químico com as rochas, é irrealista esperar que as águas ao longo flowpaths dentro até mesmo uma unidade constante mineralogia deve ter uma constante 87 Sr / 86 Sr. Em vez disso, as águas se deslocam ao longo flowpaths específicas lentamente reagir com as rochas e aproximar-se progressivamente equilíbrio químico sobre períodos de tempo longos.
Compostos

Formas de estrôncio uma variedade de sais, que possuem propriedades que são sempre intermédia entre as de bário e cálcio . Os sais tendem a ser incolor. O sulfato e carbonato são pouco solúveis, daí a sua ocorrência como minerais. A maior parte dos compostos são derivados a partir do carbonato ou o sulfureto, o qual é obtido a partir dos minerais. Típico para um derivado de alcalino-terroso, o sulfureto de hidrolisa prontamente:
- SrS + 2 H2O → Sr (OH) 2 + H 2 S
Reacções semelhantes são usados na produção de compostos comercialmente úteis, incluindo o composto de estrôncio mais útil, carbonato de estrôncio.
- SrS + H 2 O + CO 2 → SrCO 3 + H 2 S
Nitrato de estrôncio pode também ser preparado desta forma.
Papel biológico
Acantharea um grande grupo relativo de marinha radiolarian protozoários produzir intrincado mineral esqueletos composto de sulfato de estrôncio. Em sistemas biológicos, o cálcio é substituído numa pequena medida, por estrôncio. No corpo humano, a maior parte do estrôncio absorvida é depositado nos ossos. A proporção de estrôncio para o cálcio nos ossos humanos está entre 1: 1.000 e 1: 2.000 ou menos na mesma gama como no soro sanguíneo.
Efeito sobre o corpo humano
O humano corpo absorve estrôncio como se fosse cálcio . Devido à semelhança química dos elementos, as formas estáveis de estrôncio pode não constituir uma ameaça significativa saúde - de facto, os níveis encontrados naturalmente pode realmente ser benéfico (ver abaixo) - mas a radioactivos 90 Sr pode levar a várias doenças ósseas e doenças , incluindo câncer ósseo. O unidade de estrôncio é usado para medir a radioatividade absorvida a partir de 90 Sr.
Um recente estudo in vitro realizado o NY Faculdade de Odontologia usando estrôncio em osteoblastos mostraram melhora acentuada em osteoblastos na construção óssea.
A droga ranelato de estrôncio, feita através da combinação de estrôncio com ácido ranélico, foi encontrado para ajudar crescimento ósseo, aumento da densidade óssea, e para diminuir vertebral, periférico, e quadril fraturas. As mulheres que receberam a droga mostraram um aumento de 12,7% da densidade óssea. As mulheres que receberam um placebo tiveram uma diminuição de 1,6%. Metade do aumento na densidade do osso (medido por densitometria de Raio-X) é atribuído ao peso atómico superior de Sr em comparação com o cálcio, enquanto que a outra metade de um verdadeiro aumento na massa óssea. O ranelato de estrôncio é registrado como um medicamento de prescrição na Europa e muitos países do mundo. Ele deve ser prescrito por um médico, deve ser entregue por um farmacêutico, e requer rigorosa supervisão médica.
Há uma longa história de pesquisa médica sobre os benefícios do estrôncio, começando na década de 1950. Os estudos indicam uma falta de efeitos secundários indesejáveis. Vários outros sais de estrôncio tais como citrato de estrôncio e carbonato de estrôncio estão disponíveis nos Estados Unidos sob a suplementos dietéticos Saúde e Lei de Educação de 1994, proporcionando perto do conteúdo de estrôncio recomendado, cerca de 680 miligramas por dia, de ranelato de estrôncio. A sua segurança e eficácia a longo prazo não foram avaliadas em seres humanos em ensaios clínicos de grande escala. No entanto, algumas empresas que fabricam pílulas de estrôncio para aumentar a saúde óssea.
