
Chimie
Contexte des écoles Wikipédia
Ce contenu de Wikipedia a été sélectionné par SOS Enfants d'aptitude dans les écoles à travers le monde. Avant de vous décider à propos de parrainer un enfant, pourquoi ne pas en apprendre davantage sur différents organismes de parrainage premier ?


Chimie (à partir de Keme égyptienne (chem), sens «Terre») est le scientifique concerné avec la composition, la structure et les propriétés de la matière , ainsi que les changements qu'elle subit au cours des réactions chimiques . Historiquement, la chimie moderne a évolué à partir de l'alchimie après la révolution chimique (1773). La chimie est une science physique se rapportant aux études de divers atomes , molécules , cristaux et d'autres agrégats de la matière si en isolation ou une combinaison, qui intègre les concepts de l'énergie et de l'entropie par rapport à la spontanéité des procédés chimiques.
Disciplines dans la chimie sont traditionnellement groupées par le type de la matière étudiée ou le genre d'étude. Il se agit notamment de la chimie inorganique , l'étude des inorganique matière; chimie organique , l'étude de l' organique la matière; la biochimie , l'étude de substances présentes dans les organismes biologiques ; chimie physique, les énergies études liées à des systèmes chimiques aux échelles de macro, moléculaires et submolecular; chimie analytique , l'analyse des échantillons matériels pour gagner une compréhension de leur composition chimique et structure. Beaucoup de disciplines spécialisées ont émergé ces dernières années, par exemple, neurochimie l'étude chimique du système nerveux (voir les sous-disciplines ).
Vue d'ensemble
La chimie est l'étude scientifique de l'interaction des des substances chimiques qui sont constitués d' atomes ou les composants subatomiques qui composent atomes: protons , électrons et des neutrons . Atomes se combinent pour produire des molécules ou des cristaux . La chimie peut être appelé " la science centrale "parce qu'elle relie l'autre sciences naturelles, telles que l'astronomie , la physique , la science des matériaux , la biologie et la géologie .
La genèse de la chimie peut être attribuée à certaines pratiques, connues sous le nom alchimie , qui avaient été pratiquées pour plusieurs millénaires dans diverses parties du monde, notamment au Moyen-Orient.
La structure des objets que nous utilisons couramment et les propriétés de la matière dont nous interagissons avec souvent, sont une conséquence des propriétés des substances chimiques et de leurs interactions. Par exemple, l'acier est dur que le fer parce que ses atomes sont liés ensemble dans un plus rigide réseau cristallin; le bois brûle ou subit rapide oxydation, car il peut réagir spontanément avec l'oxygène dans une réaction chimique au-dessus d'une certaine température ; sucre et le sel se dissolvent dans l'eau parce que leurs propriétés moléculaires / ioniques sont telles que la dissolution est préférée dans les conditions ambiantes.
Les transformations qui sont étudiées dans la chimie sont le résultat de l'interaction, soit entre différentes substances chimiques ou entre la matière et de l'énergie . La chimie traditionnelle implique l'étude des interactions entre substances dans une chimie laboratoire en utilisant diverses formes de verrerie de laboratoire.

Une réaction chimique est une transformation de certaines substances dans une ou plusieurs autres substances. Il peut être représenté symboliquement par un équation chimique. Le nombre d'atomes de gauche et de droite de l'équation pour une transformation chimique est le plus souvent égal. La nature des réactions chimiques d'une substance peut subir et les changements d'énergie qui peuvent l'accompagner sont contraints par certaines règles de base, appelés lois chimiques.
Énergie et entropie considérations sont toujours important dans presque toutes les études chimiques. Les substances chimiques sont classées en fonction de leur la structure, la phase ainsi que leur compositions chimiques. Ils peuvent être analysés en utilisant les outils de l'analyse chimique , par exemple spectroscopie et chromatographie .
La chimie est une partie intégrante de la la science à la fois au programme l'école secondaire ainsi que le niveau collégial tôt. A ces niveaux, il est souvent appelé «chimie générale» qui est une introduction à une grande variété de concepts fondamentaux qui permettent à l'étudiant d'acquérir des outils et des compétences utiles aux niveaux avancés, de sorte que la chimie est toujours étudié dans une de ses différents sous- disciplines. Les scientifiques, engagés dans l'industrie chimique la recherche sont connus comme chimistes. La plupart des chimistes se spécialisent dans un ou plusieurs sous-disciplines.
Histoire
La genèse de la chimie peut être tracée au phénomène largement observé de combustion qui a conduit à la métallurgie - l'art et la science de minerais de traitement pour obtenir des métaux (par exemple, la métallurgie dans l'Inde ancienne). L'avidité pour l'or a conduit à la découverte de son procédé de purification, même si, les principes sous-jacents ne ont pas été bien compris - il a été pensé pour être une transformation plutôt que la purification. De nombreux chercheurs dans ces jours pensaient-il raisonnable de croire qu'il existe des moyens pour transformer (de base) des métaux moins coûteux en or. Ce qui donna lieu à l'alchimie, et la recherche de la Pierre Philosophale, qui a été censé apporter une telle transformation par simple contact.
Certains considèrent musulmans médiévaux pour être les premiers chimistes, qui ont introduit précise observation et contrôlée l'expérimentation sur le terrain, et a découvert de nombreux substances chimiques. Les chimistes musulmans les plus influents étaient Geber (d. 815), al-Kindi (d. 873), al-Razi (d. 925), et al-Biruni (d. 1048). Les travaux de Geber devenus plus largement connus en Europe à travers latine traductions par un pseudo-Geber au 14ème siècle en Espagne , qui a également écrit certains de ses propres livres sous le nom de plume "Geber". La contribution de Alchimistes indiennes et métallurgistes dans le développement de la chimie était également très importante.
L'émergence de la chimie en Europe est principalement attribuable à l'incidence récurrente de la peste et fléaux là pendant la dite Âge Des Ténèbres. Ceci a donné lieu à un besoin de médicaments. On pensait qu'il existe une médecine universelle appelée Élixir de vie qui peut guérir toutes les maladies, mais comme la pierre philosophale, il n'a jamais été trouvé.
Pour certains praticiens, l'alchimie était une poursuite intellectuelle, au fil du temps, ils ont obtenu de mieux en mieux. Paracelse (1493-1541), par exemple, a rejeté la théorie 4 élémentaire et avec seulement une vague compréhension de ses produits chimiques et médicaments, formé un hybride de l'alchimie et la science dans ce qui allait être appelé iatrochimie. De même, les influences des philosophes tels que Sir Francis Bacon (1561-1626) et René Descartes (1596-1650), qui a exigé plus de rigueur en mathématiques et dans l'élimination des biais d'observations scientifiques, conduit à une révolution scientifique. En chimie, cela a commencé avec Robert Boyle (1627-1691), qui est venu avec un équations connues sous le nom La loi de Boyle sur les caractéristiques de l'état gazeux. Chimie vient en effet d'âge où Antoine Lavoisier (1743-1794), a développé la théorie de Conservation de la masse en 1783; et le développement de la Théorie atomique par John Dalton vers 1800. La loi de conservation de la masse a abouti à la reformulation de la chimie basée sur cette loi et la théorie de l'oxygène de la combustion, qui a été en grande partie basée sur les travaux de Lavoisier. Contributions fondamentales de Lavoisier à la chimie étaient le résultat d'un effort conscient pour se adapter à toutes les expériences dans le cadre d'une théorie unique. Il a établi l'utilisation constante de l'équilibre chimique, utilisé l'oxygène pour renverser le théorie du phlogistique, et a développé un nouveau système de nomenclature chimique et a apporté une contribution au système métrique moderne. Lavoisier a également travaillé pour traduire la langue archaïque et technique de la chimie en quelque chose qui pourrait être facilement compris par les masses incultes largement, conduisant à un intérêt accru du public en chimie. Tous ces progrès de la chimie ont conduit à ce qui est habituellement appelé le révolution chimique. Les contributions de Lavoisier ont conduit à ce qu'on appelle maintenant la chimie moderne - de la chimie qui est étudié dans les institutions éducatives du monde entier. Ce est à cause de ces et d'autres contributions que Antoine Lavoisier est souvent célébré comme le " Père de la chimie moderne ". La découverte ultérieure de Friedrich Wöhler que de nombreuses substances naturelles, composés organiques , peuvent en effet être synthétisés dans une chimie laboratoire a également aidé la chimie moderne à maturité de son enfance.
Le découvertes des éléments chimiques a une longue histoire depuis les jours de l'alchimie et a abouti à la création de la table périodique des éléments chimiques par Dmitri Mendeleev (1834-1907) et plus tard de certaines découvertes des éléments de synthèse.
Étymologie
Le mot vient de la chimie de l'étude antérieure de l'alchimie, qui est essentiellement la quête pour faire de l'or à partir de matériaux de départ terre. Quant à l'origine du mot "alchimie" la question est plus discutable; il peut certainement faire remonter aux Grecs, et certains, à la suite E. Wallis Budge, ont également affirmé égyptiens origines. Alchemy, généralement, dérive de l'ancien alkemie français de l'arabe al-kimia - «l'art de la transformation». Les Arabes ont emprunté le mot «Kimia" des Grecs quand ils ont conquis Alexandrie en l'an 642 AD. Un plan provisoire est le suivant:
- Alchimie égyptienne [3000 BCE - 400 BCE], de formuler "élément" théories début comme le Ogdoad.
- L'alchimie grecque [332 BCE - 642 CE], le roi grec Alexandre le Grand conquiert l'Egypte et fonde Alexandrie, ayant la plus grande bibliothèque du monde, où des érudits et des sages se réunissent pour étudier.
- Alchimie Arabe [642 CE - 1200], les Arabes se emparent d'Alexandrie; Jabir est le chimiste principale
- L'alchimie européenne [1300 - présent], Pseudo-Geber se appuie sur la chimie Arabe
- Chimie [1661], Boyle écrit son texte de la chimie classique La Chymist Sceptique
- Chimie [1787], Lavoisier écrit ses éléments classiques de la chimie
- Chimie [1803], Dalton publie sa théorie atomique
Ainsi, un alchimiste a été appelé un «chimiste» dans le langage populaire, et plus tard le suffixe "-ry" a été ajouté à ce pour décrire l'art du chimiste que «chimie».
Définitions
En rétrospective, la définition de la chimie semble changer invariablement par décennie, que de nouvelles découvertes et théories ajouter à la fonctionnalité de la science. Ci-dessous sont quelques-unes des définitions standard utilisés par divers chimistes relevées:
- Alchimie (330) - l'étude de la composition des eaux, le mouvement, la croissance, incarnant, désincarnant, tirant les esprits de corps et lier les esprits au sein des organes ( Zosime).
- Chymistry (1661) - le sujet des principes matériels des organes Mixtes ( Boyle ).
- Chymistry (1663) - un art scientifique, par lequel on apprend à dissoudre les organes, et en tirer les différentes substances sur leur composition, et comment les unir à nouveau, et d'exalter les à une plus grande perfection ( Glaser).
- Chimie (1730) - l'art de résoudre mixte, composé ou organismes globaux dans leurs principes; et de composer ces organes de ces principes ( Stahl).
- Chimie (1837) - la science concernée avec les lois et les effets des forces moléculaires ( Dumas).
- Chimie (1947) - la science des substances: leur structure, leurs propriétés, et les réactions qui les changent en d'autres substances ( Pauling ).
- Chimie (1998) - l'étude de la matière et les changements qu'elle subit ( Chang).
Concepts de base
Plusieurs notions sont essentielles pour l'étude de la chimie, certains d'entre eux sont:
Atome
Un atome est l'unité de base d'un élément. Ce est une collecte de la matière consistant en un noyau chargé positivement (le noyau atomique ), qui contient des protons et des neutrons , et qui maintient un certain nombre d' électrons pour équilibrer la charge positive dans le noyau. L'atome est aussi la plus petite entité qui peut être envisagée de conserver une partie de la les propriétés chimiques de l'élément, tels que électronégativité, potentiel d'ionisation, préféré état d'oxydation (s), nombre de coordination, et les types préférés de liens pour former (par exemple, métallique , ionique , covalente).
Élément
Le concept d'élément chimique est liée à celle de la substance chimique. Un élément chimique est caractérisé par un nombre particulier de protons dans les noyaux de ses atomes. Ce nombre est connu sous le numéro atomique de l'élément. Par exemple, tous les atomes avec 6 protons dans leur noyau sont des atomes de l'élément chimique carbone , et les atomes avec 92 protons dans leur noyau sont des atomes de l'élément uranium . Cependant, plusieurs isotopes d'un élément, qui diffèrent les uns des autres dans le nombre de neutrons présents dans le noyau, peuvent exister.
La présentation la plus commode des éléments chimiques est dans la table périodique des éléments chimiques, qui regroupe des éléments de numéro atomique. Grâce à sa disposition ingénieuse, groupes, ou des colonnes, et périodes, ou rangées, d'éléments dans le tableau soit part plusieurs propriétés chimiques, ou de suivre une certaine tendance dans les caractéristiques telles que rayon atomique, électronégativité, etc. La liste des éléments par nom , par le symbole, et par numéro atomique sont également disponibles.
Composé
Un composé est une substance avec un rapport particulier des atomes de certains éléments chimiques qui détermine sa composition, et notamment une organisation qui détermine les propriétés chimiques. Par exemple, l'eau est un composé contenant de l'hydrogène et de l'oxygène dans un rapport de deux à un, avec de l'oxygène entre les atomes d'hydrogène, et un angle de 104,5 ° entre eux. Les composés sont formés et une interconversion par des réactions chimiques .
Substance
Une substance chimique est une sorte de matière avec une certaine composition et un ensemble de propriétés. Strictement parlant, un mélange de composés, des éléments ou des composés et des éléments ne est pas une substance chimique, mais il peut être appelé un produit chimique. La plupart des substances que nous rencontrons dans notre vie quotidienne sont une sorte de mélange, par exemple l'air , alliages, biomasse, etc.
Nomenclature des substances est un élément essentiel de la langue de la chimie. En général, il se réfère à un système de dénomination des composés chimiques . Plus tôt dans l'histoire de substances chimiques ont été donnés par leur nom découvreur, qui a souvent conduit à une certaine confusion et difficulté. Cependant, aujourd'hui, le système IUPAC de nomenclature chimique permet aux chimistes de préciser par des composés spécifiques de nom parmi l'infinie variété de produits chimiques possibles. La nomenclature standard des substances chimiques est fixé par le Union internationale de chimie pure et appliquée (UICPA). Il existe des systèmes bien définis en place pour nommer les espèces chimiques. composés organiques sont nommés selon le système de nomenclature organique. composés inorganiques sont nommés selon le système de nomenclature inorganique. En outre, le Chemical Abstracts Service a mis au point une méthode à la substance indice chimique. Dans ce schéma, chaque substance chimique est identifiable par un certain nombre numérique connu sous le nom Numéro de registre CAS.
Molécule
Une molécule est la plus petite partie indivisible, à côté d'un atome, d'un pur substance chimique qui a son ensemble unique de propriétés chimiques, ce est, de son potentiel de subir une certaine un ensemble de réactions chimiques avec d'autres substances. Les molécules peuvent exister comme unités électriquement neutres contrairement ions . Les molécules sont généralement un ensemble d'atomes liés par des liaisons covalentes, telles que la structure est électriquement neutre et tous les électrons de valence sont jumelés avec d'autres électrons soit en obligations ou en paires libres.

Une des caractéristiques principale d'une molécule est sa géométrie souvent appelée son structure. Bien que la structure des molécules atomiques diatomiques, triatomiques ou tétra peut être insignifiante, (linéaires, angulaires pyramidale etc.) la structure des molécules polyatomiques, qui sont constitués de plus de six atomes (de plusieurs éléments) peut être cruciale pour sa nature chimique.
Taupe
Une mole est la quantité d'un substance qui contient autant d'entités élémentaires (atomes, molécules ou ions) qu'il ya d'atomes dans 0,012 kilogramme (ou 12 g) de où les atomes de carbone 12 sont non liés, au repos et en carbone-12, leur état fondamental. Ce nombre est connu comme la constante d'Avogadro , et est déterminé de manière empirique. La valeur actuellement acceptée est 6.02214179 (30) × 10 23 mol -1 (2007 CODATA). Ce est un peu comme le terme " douzaine "en ce qu'elle est un nombre absolu (sans unité) et peut décrire tout type d'objet élémentaire, même si l'utilisation de la taupe est généralement limitée à la mesure de subatomique, atomique et moléculaire structures.
Le nombre de moles d'une substance dans un litre d'une solution est connue sous son molarité. Molarité est l'unité couramment utilisée pour exprimer la concentration d'une solution en chimie physique.
Les ions et les sels
Un ion est une espèce chargée, un atome ou une molécule, qui a perdu ou gagné un ou plusieurs électrons. Chargé positivement cations (par exemple sodium cations Na +) et chargés négativement anions (par exemple, chlorure Cl -) peut former un réseau cristallin de neutre des sels (par exemple chlorure de sodium NaCl). Des exemples de ions polyatomiques qui ne fractionnent au cours des réactions acide-base sont l'hydroxyde (OH -) et phosphate (PO 4 3-).
Les ions dans la phase gazeuse est souvent connu sous plasma .
Phase
En plus des propriétés chimiques spécifiques qui permettent de distinguer différentes catégories de produits chimiques produits chimiques peuvent exister en plusieurs phases. Pour la plupart, les classifications chimiques sont indépendant de ces classifications de phase en vrac; Toutefois, certaines phases plus exotiques sont incompatibles avec certaines propriétés chimiques. Une phase est un ensemble des états d'un système chimique qui ont des propriétés structurelles similaires en vrac, sur une gamme de conditions, telles que la pression ou la température . Les propriétés physiques, telles que la densité et indice de réfraction ont tendance à tomber dans les valeurs caractéristiques de la phase. La phase de matière est définie par la transition de phase, qui est l'énergie lorsque mis en prise ou hors du système entre dans le réarrangement de la structure du système, au lieu de changer les conditions vrac.
Parfois, la distinction entre les phases peut être continue au lieu d'avoir une frontière discrète, dans ce cas, la matière est considérée comme étant dans un état supercritique. Quand trois états répondent basées sur les conditions, il est connu en tant que point triple et puisque ce est invariant, ce est un moyen pratique de définir un ensemble de conditions.
Les exemples les plus connus de phases sont solides , liquides et gaz . De nombreuses substances présentent plusieurs phases solides. Par exemple, il ya trois phases de solide fer (alpha, gamma et delta) qui varient en fonction de la température et de la pression. Une différence principale entre les phases solides est la structure cristalline, ou d'un arrangement, des atomes. Phases moins familières incluent des plasmas , Condensats de Bose-Einstein et condensats fermioniques et la paramagnétique et phases ferromagnétiques magnétiques des matériaux. Bien que la plupart des phases familières traitent les systèmes tridimensionnels, il est également possible de définir des analogues dans des systèmes à deux dimensions, qui a reçu une attention pour sa pertinence à des systèmes en biologie .
Liaison chimique
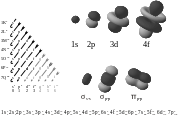
Une liaison chimique est un concept pour comprendre comment les atomes dans les molécules collent ensemble. Il peut être visualisé comme la équilibre multipolaire entre les charges positives dans les noyaux et les charges négatives oscillant autour d'eux. Plus qu'une simple attraction et de répulsion, les énergies et les distributions caractérisent la disponibilité d'un électron à se lier à un autre atome. Ces potentiels créent le les interactions qui maintient ensemble les atomes dans des molécules ou des cristaux . Dans de nombreux composés simples, Valence Bond Theory, le modèle Valence Shell paires d'électrons Répulsion ( VSEPR), et le concept de nombre d'oxydation peut être utilisée pour prédire la structure moléculaire et la composition. De même, les théories de la physique classique peut être utilisé pour prédire de nombreuses structures ioniques. Avec des composés plus complexes, tels que complexes métalliques, la théorie de la liaison de valence échoue et les approches alternatives, basée principalement sur les principes de la chimie quantique comme le théorie des orbitales moléculaires, sont nécessaires. Voir le schéma à orbitales électroniques.
Réaction chimique
Réaction chimique est un concept lié à la transformation d'un substance chimique par son interaction avec un autre, ou comme conséquence de son interaction avec certains forme d'énergie. Une réaction chimique peut se produire naturellement ou menée dans un laboratoire par les chimistes dans des récipients spécialement conçus qui sont souvent verrerie de laboratoire. Il peut en résulter la formation ou dissociation de molécules, ce est-molécules se briser afin de former deux ou plusieurs petites molécules, ou le réarrangement des atomes dans ou à travers les molécules. Les réactions chimiques impliquent généralement la fabrication ou la rupture des liaisons chimiques . L'oxydation, la réduction, dissociation, acide-base neutralisation et moléculaire réarrangement sont quelques-uns des types couramment utilisés de réactions chimiques.
Une réaction chimique peut être représenté symboliquement par un équation chimique. Alors que dans une réaction chimique non-nucléaire le nombre et type d'atomes des deux côtés de l'équation sont égaux, pour une réaction nucléaire ce ne est vrai que pour les particules nucléaires à savoir. protons et de neutrons.
La séquence d'étapes dans lesquelles la réorganisation des liaisons chimiques peut avoir lieu dans le cadre d'une réaction chimique est appelé de son mécanisme. Une réaction chimique peut être envisagé de prendre place dans un certain nombre de mesures, dont chacun peut avoir une vitesse différente. Beaucoup les intermédiaires de réaction ayant une stabilité variables peuvent donc être envisagées au cours d'une réaction. mécanismes de réaction sont proposées pour expliquer la cinétique et la composition relative de produit d'une réaction. Beaucoup physico-chimistes se spécialisent dans l'exploration et de proposer les mécanismes de diverses réactions chimiques. Plusieurs règles empiriques, comme le Règles Woodward-Hoffmann viennent souvent à portée de main tout en proposant un mécanisme pour une réaction chimique.
Une définition plus stricte, ce est que "une réaction chimique est un processus qui aboutit à l'interconversion des espèces chimiques". Selon cette définition, une réaction chimique peut être un réaction élémentaire ou d'un réaction par étapes. Une mise en garde supplémentaire est effectuée, en ce que cette définition inclut les cas où interconversion de conformères est observable expérimentalement. Ces réactions chimiques décelables impliquent normalement des ensembles d'entités moléculaires comme indiqué par cette définition, mais il est souvent conceptuellement commode d'utiliser le terme également des changements impliquant des entités moléculaires simples (ce est à dire 'événements chimiques microscopiques »).
Énergie
Une réaction chimique se accompagne inévitablement d'une augmenter ou diminution de l'énergie des substances impliquées. De l'énergie est transférée entre les environs et les réactifs de la réaction sous la forme de chaleur ou léger, les produits d'une réaction peuvent avoir plus ou moins d'énergie que les réactifs. Une réaction est dit être exothermique si l'état final est inférieur sur l'échelle d'énergie que l'état initial; en cas de réactions endothermiques la situation est autrement.
Les réactions chimiques sont toujours pas possible à moins que les réactifs surmontent une barrière d'énergie connu sous le nom d'énergie d'activation . La vitesse d'une réaction chimique (à une température donnée T) est liée à l'énergie d'activation E, par le coefficient de la population de Boltzmann  - Qui est la probabilité d'avoir de molécule énergie supérieure ou égale à E, à la température donnée T. Cette dépendance exponentielle de la vitesse de réaction la température est connue comme la Équation d'Arrhenius. L'énergie nécessaire à une réaction chimique d'activation peut être sous forme de chaleur, la lumière, l'électricité ou mécanique vigueur sous la forme de ultrasons.
- Qui est la probabilité d'avoir de molécule énergie supérieure ou égale à E, à la température donnée T. Cette dépendance exponentielle de la vitesse de réaction la température est connue comme la Équation d'Arrhenius. L'énergie nécessaire à une réaction chimique d'activation peut être sous forme de chaleur, la lumière, l'électricité ou mécanique vigueur sous la forme de ultrasons.
Un concept connexe l'énergie libre, qui incorpore aussi des considérations d'entropie, est un moyen très utile pour prévoir la possibilité d'une réaction et la détermination de l'état d'équilibre d'une réaction chimique, thermodynamique chimique. Une réaction ne est possible que si le changement total dans l' énergie libre de Gibbs est négatif, 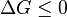 ; si elle est égale à zéro, la réaction chimique est dit être à l'équilibre .
; si elle est égale à zéro, la réaction chimique est dit être à l'équilibre .
Il n'y a que les états possibles limités d'énergie pour les électrons, les atomes et les molécules. Ceux-ci sont déterminés par les règles de la mécanique quantique , qui exigent quantification de l'énergie d'un système lié. Les atomes / molécules dans un état d'énergie plus élevée sont dits être excité. Les molécules / atomes de la substance dans un état d'énergie excité sont souvent beaucoup plus réactive, qui se prête à des réactions chimiques.
La phase d'une substance est invariablement déterminée par son énergie et de ses environs. Lorsque les forces intermoléculaires d'une substance sont telles que l'énergie de l'environnement ne est pas suffisante pour les surmonter, il se produit dans une phase plus ordonné comme liquide ou solide comme ce est le cas avec de l'eau (H 2 O), d'un liquide à la température ambiante car ses molécules sont liées par des liaisons hydrogène. Alors que de l'hydrogène sulfuré (H 2 S) est un gaz à température ambiante et à la pression standard, en tant que ses molécules sont liées par plus faible interactions dipôle-dipôle.
Le transfert d'énergie d'une substance chimique avec une autre dépend de la taille de l'énergie quanta émis par une substance. Cependant, l'énergie thermique est facilement transféré à partir de presque ne importe quelle substance à l'autre principalement parce que les niveaux d'énergie de vibration et de rotation dans une substance sont placés très près. Parce que les niveaux d'énergie électroniques ne sont pas étroitement espacées, le rayonnement électromagnétique ultraviolet ne est pas transféré avec un égal bonheur, comme ce est également le cas avec l'énergie électrique.
L'existence de niveaux d'énergie caractéristiques de différents substances chimiques sont utiles pour leur identification par l'analyse de raies spectrales de différents types de spectres souvent utilisés en spectroscopie chimique par exemple IR, micro-ondes, RMN, ESR etc. Ce est utilisé pour identifier la composition des objets distants - comme des étoiles et des galaxies lointaines - en analysant leur rayonnement (voir spectroscopie ).

Le terme énergie chimique est souvent utilisé pour indiquer le potentiel d'une substance chimique à subir une transformation par une réaction chimique ou transformer d'autres substances chimiques.
lois chimiques
Les réactions chimiques sont régies par certaines lois, qui sont devenus des concepts fondamentaux de la chimie. Certains d'entre eux sont:
- Droit de conservation de la masse, selon la physique moderne ce est en fait l'énergie qui est conservée, et que l'énergie et la masse sont liée; un concept qui devient important dans chimie nucléaire.
- Loi de la conservation de l'énergie conduit à des concepts importants de l'équilibre , la thermodynamique , et cinétique.
- Loi de composition définie, bien que dans de nombreux systèmes (notamment Biomacromolecules et minéraux) les ratios ont tendance à exiger un grand nombre, et sont souvent représentés comme une fraction.
- Loi des proportions multiples
- La loi de Hess
- Loi de Beer-Lambert
- La loi de diffusion de Fick
- La loi de Raoult
- La loi de Henry
- La loi de Boyle (1662, pression et volume relatif)
- Loi de Charles (1787, concernant le volume et la température)
- Loi de Gay-Lussac (1809, concernant la pression et de la température)
- La loi d'Avogadro
Sous-disciplines
Chimie est généralement divisé en plusieurs grandes sous-disciplines. Il ya également plusieurs grands domaines interdisciplinaires et plus spécialisées de la chimie.
- Chimie analytique est l'analyse des échantillons matériels pour gagner une compréhension de leur composition chimique et structure. Chimie analytique intègre des méthodes expérimentales normalisées en chimie. Ces procédés peuvent être utilisés dans toutes les sous-disciplines de la chimie, à l'exclusion chimie purement théorique.
- Biochimie est l'étude des produits chimiques , des réactions chimiques et chimiques interactions qui ont lieu dans vivant organismes . Biochimie et chimie organique sont étroitement liés, comme dans chimie médicinale ou neurochimie. Biochemistry est également associée à la biologie moléculaire et la génétique .
- Chimie inorganique est l'étude des propriétés et des réactions de composés inorganiques. La distinction entre les disciplines organiques et inorganiques ne est pas absolue et il ya beaucoup de chevauchement, surtout dans le sous-discipline de chimie organométallique.
- Chimie des matériaux est la préparation, la caractérisation et la compréhension des substances avec une fonction utile. Le champ est une nouvelle largeur d'étude dans les programmes d'études supérieures, et il intègre des éléments de tous les domaines classiques de la chimie avec un accent sur les questions fondamentales qui sont uniques aux matériaux. Les systèmes primaires de l'étude incluent la chimie des phases condensées (solides, liquides, polymères) et les interfaces entre différentes phases.
- Chimie nucléaire est l'étude de la façon dont les particules subatomiques viennent ensemble et font noyaux. Moderne La transmutation est une composante importante de la chimie nucléaire et le table des nucléides est un résultat important et un outil pour ce domaine.
- La chimie organique est l'étude de la structure, les propriétés, la composition, les mécanismes et les réactions de composés organiques . Un composé organique est défini comme ne importe quel composé à base d'un squelette carboné.
- Physico-chimie est l'étude de la base physique et fondamentale des systèmes et des processus chimiques. En particulier, l'énergétique et la dynamique de ces systèmes et processus sont d'intérêt pour les chimistes physiques. Les domaines importants de l'étude incluent thermodynamique chimique, la cinétique chimique, électrochimie, la mécanique statistique et la spectroscopie . Chimie physique a un grand chevauchement avec la physique moléculaire . Chimie physique implique l'utilisation de calcul pour dériver les équations. Il est généralement associée à la chimie quantique et la chimie théorique. Chimie physique est une discipline distincte de la physique chimique.
- Chimie théorique est l'étude de la chimie par le raisonnement théorique fondamental (habituellement dans les mathématiques ou la physique ). En particulier, l'application de la mécanique quantique à la chimie se appelle la chimie quantique . Depuis la fin de la Seconde Guerre mondiale , le développement des ordinateurs a permis un développement systématique de la chimie computationnelle , qui est l'art de développer et d'appliquer programmes informatiques pour résoudre les problèmes chimiques. Chimie théorique a le grand chevauchement avec (théorique et expérimentale) physique de la matière condensée et physique moléculaire .
Autres domaines comprennent Astrochimie, La chimie atmosphérique, Ingénieur Chimiste, la biologie chimique, Chimio-informatique, Électrochimie, Chimie de l'environnement, Débit chimie, Géochimie, La chimie verte, Histoire de la chimie, la science des matériaux , La chimie mathématique, Chimie médicinale, Biologie Moléculaire, La nanotechnologie, Oenologie, Chimie organométallique, Pétrochimie, Pharmacologie , Photochimie, Phytochimie, La chimie des polymères, La chimie du solide, Sonochemistry, La chimie supramoléculaire, La chimie de surface, Immunochimie et Thermochimie.
L'industrie chimique
Le industrie chimique représente une activité économique importante. Les 50 premiers producteurs mondiaux de produits chimiques en 2004 ont réalisé des ventes de 587 milliards de dollars américains avec une marge de 8,1% de profits et Les dépenses de recherche et développement de 2,1% des ventes totales de produits chimiques.
Les associations professionnelles
- American Chemical Society
- Institut de chimie du Canada
- Chemical Society du Pérou
- Union internationale de chimie pure et appliquée
- Institut Royal Australian Chemical
- Royal Society of Chemistry
- Society of Chemical Industry
- Association mondiale des chimistes théoriques et informatiques

