
Terbium
Renseignements généraux
Enfants SOS bénévoles ont aidé à choisir des articles et faites autre matériel de programme de parrainage d'enfants aide les enfants du monde en développement à apprendre aussi.
| Terbium | ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
65 Tb | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| Apparence | ||||||||||||||||||||||||||||
blanc argenté  | ||||||||||||||||||||||||||||
| Propriétés générales | ||||||||||||||||||||||||||||
| Nom, symbole, nombre | terbium, Tb, 65 | |||||||||||||||||||||||||||
| Prononciation | / t ɜr b Je ə m / TUR -bee-əm | |||||||||||||||||||||||||||
| Élément Catégorie | lanthanides | |||||||||||||||||||||||||||
| Groupe, période, bloc | n / a, 6, fa | |||||||||||||||||||||||||||
| Poids atomique standard | 158,92535 | |||||||||||||||||||||||||||
| Configuration électronique | [ Xe ] 4f 9 6s 2 2, 8, 18, 27, 8, 2  | |||||||||||||||||||||||||||
| Histoire | ||||||||||||||||||||||||||||
| Découverte | Carl Gustaf Mosander (1842) | |||||||||||||||||||||||||||
| Premier isolement | Carl Gustaf Mosander (1842) | |||||||||||||||||||||||||||
| Propriétés physiques | ||||||||||||||||||||||||||||
| Phase | solide | |||||||||||||||||||||||||||
| Densité (à proximité rt) | 8,23 g · cm -3 | |||||||||||||||||||||||||||
| Liquid densité au mp | 7,65 g · cm -3 | |||||||||||||||||||||||||||
| Point de fusion | 1629 K , 1356 ° C, 2473 ° F | |||||||||||||||||||||||||||
| Point d'ébullition | 3503 K, 3230 ° C, 5846 ° F | |||||||||||||||||||||||||||
| La chaleur de fusion | 10,15 kJ · mol -1 | |||||||||||||||||||||||||||
| Chaleur de vaporisation | 293 kJ · mol -1 | |||||||||||||||||||||||||||
| Capacité thermique molaire | 28,91 J · mol -1 · K -1 | |||||||||||||||||||||||||||
| La pression de vapeur | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| Propriétés atomiques | ||||||||||||||||||||||||||||
| États d'oxydation | 4, 3, 2, 1 (Faiblement oxyde de base) | |||||||||||||||||||||||||||
| Électronégativité | ? 1,2 (échelle de Pauling) | |||||||||||||||||||||||||||
| énergies d'ionisation | 1er: 565,8 kJ · mol -1 | |||||||||||||||||||||||||||
| 2ème: 1110 kJ · mol -1 | ||||||||||||||||||||||||||||
| 3ème: 2114 kJ · mol -1 | ||||||||||||||||||||||||||||
| Rayon atomique | 177 h | |||||||||||||||||||||||||||
| Rayon covalente | 194 ± 17 heures | |||||||||||||||||||||||||||
| Miscellanées | ||||||||||||||||||||||||||||
| Crystal structure | hexagonale compacte | |||||||||||||||||||||||||||
| Ordre magnétique | paramagnétique à 300 K | |||||||||||||||||||||||||||
| Résistivité électrique | ( rt) (α, poly) 1,150 μΩ · m | |||||||||||||||||||||||||||
| Conductivité thermique | 11,1 W · m -1 · K -1 | |||||||||||||||||||||||||||
| Dilatation thermique | ( rt) (α, poly) 10,3 um / (m · K) | |||||||||||||||||||||||||||
| Vitesse du son (tige mince) | (20 ° C) 2,620 m · s -1 | |||||||||||||||||||||||||||
| Le module d'Young | (Formulaire de α) 55,7 GPa | |||||||||||||||||||||||||||
| Module de cisaillement | (Formulaire de α) 22,1 GPa | |||||||||||||||||||||||||||
| Module Bulk | (Formulaire de α) 38,7 GPa | |||||||||||||||||||||||||||
| Coefficient de Poisson | (Formulaire de α) 0,261 | |||||||||||||||||||||||||||
| Dureté Vickers | 863 MPa | |||||||||||||||||||||||||||
| Dureté Brinell | 677 MPa | |||||||||||||||||||||||||||
| Numéro de registre CAS | 7440-27-9 | |||||||||||||||||||||||||||
| La plupart des isotopes stables | ||||||||||||||||||||||||||||
| Article détaillé: Isotopes de terbium | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
Terbium est un élément chimique avec le symbole Tb et de numéro atomique 65. Ce est un blanc argenté terre rare métal qui est malléable, ductile et assez souple pour être coupés avec un couteau. Terbium est jamais trouvé dans la nature comme un élément libre, mais il est contenu dans de nombreux minéraux , y compris cerite, gadolinite, monazite, xénotime et euxénite.
Terbium est utilisé pour dope le fluorure de calcium, le calcium et le tungstate de strontium molybdate, les matériaux qui sont utilisés dans dispositifs à l'état solide, et en tant que stabilisant des cristaux de les piles à combustible qui fonctionnent à des températures élevées. En tant que composante de Terfenol-D (un alliage qui dilate et se contracte quand il est exposé à des champs magnétiques plus que tout autre alliage), le terbium est utilisé dans actionneurs, dans navale systèmes sonar et capteurs.
La plupart de l'approvisionnement de terbium du monde est utilisé dans luminophores verts. Terbium est en oxyde lampes et tubes de télévision fluorescent. Terbium verte luminophores sont combinés avec divalent europium luminophores bleus et l'europium trivalent luminophores rouges pour fournir la technologie d'éclairage "trichrome", une lumière blanche à haute efficacité utilisé pour l'éclairage standard dans l'éclairage intérieur.
Caractéristiques
Propriétés physiques
Terbium est un blanc argenté terre rare métal qui est malléable, ductile et assez souple pour être coupés avec un couteau. Il est relativement stable à l'air par rapport aux autres lanthanides. Terbium existe dans deux cristaux formes allotropiques dont la température de transformation de 1289 ° C entre eux.
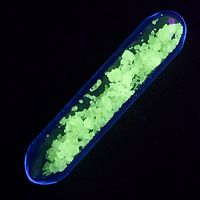
Le terbium (III) cation est brillamment fluorescent, dans une couleur jaune citron brillant qui est le résultat d'un vert forte raie d'émission en combinaison avec d'autres lignes à l'orange et le rouge. Le yttrofluorite de la variété minérale fluorite doit sa fluorescence jaune crème en partie à terbium. Terbium oxyde facilement, et est donc utilisé dans sa forme élémentaire spécifiquement pour la recherche. Atomes simples Tb ont été isolés en leur implantation dans molécules de fullerène.
Terbium a simple ordre ferromagnétique à des températures inférieures 219 K.-dessus de 219 K, il se transforme en une hélice état antiferromagnétique dans lequel tous les moments atomiques dans un particulier couche de plan de base sont parallèles et orientés selon un angle fixe les moments de couches adjacentes. Ce antiferromagnétisme inhabituelle transforme en désordre état paramagnétique à 230 K.
Propriétés chimiques
L'état de valence le plus commun de terbium est trois, comme dans Tb 2 O 3. L'état 4 est connu dans TbO 2 et 4 TbF. Terbium brûle aisément pour former un mélange terbium (III, IV) de l'oxyde:
- 8 Tb + 7 O 2 → 2 Tb 4 O 7
En solution, les formulaires de terbium seuls les ions trivalents. Terbium est assez électropositive et réagit lentement avec l'eau froide et assez rapidement avec de l'eau chaude pour former de l'hydroxyde de terbium:
- 2 Tb + 6 H 2 O → 2 Tb (OH) 3 + 3 H 2 ↑
Terbium métal réagit avec tous les halogènes, formant trihalogénures blancs:
Terbium se dissout facilement dans diluée de l'acide sulfurique pour former des solutions contenant le terbium rose pâle (III) des ions, qui existent comme [Tb (OH 2) 9] 3+ complexes:
- 2 Tb (s) + 3 H 2 SO 4 → 2 Tb 3+ + 3 SO 2-
4 + 3 H 2 ↑
Composés

Terbium se combine avec l'azote, le carbone, le soufre, le phosphore, le bore, le sélénium, le silicium et l'arsenic à des températures élevées, en formant divers composés binaires tels que TbH 2, 3 TbH, TbB 2, Tb 2 S 3, TBSE, et TbTe TbN. Dans ces composés, la plupart du temps Tb présentent états d'oxydation 3 et parfois deux. Terbium (II) halogénures sont obtenus par recuit Tb (III) en présence des halogénures métalliques Tb dans des conteneurs de tantale. Terbium forme également le sesquichlorure Tb 2 Cl 3, qui peut être encore réduit à TBCL par recuit à 800 ° C. Ce terbium (I) chlorure formes plaquettes avec une structure de type graphite en couches.
D'autres composés comprennent
- Chlorures: TBCL 3
- Bromures: TbBr 3
- Iodures: TBi 3
- Fluorures: TbF 3, TbF 4
Terbium (IV) fluorure est un agent de fluoration solide, émettant fluor atomique relativement pur au chauffage plutôt que le mélange de vapeurs de fluorure émis par CoF 3 ou CeF 4.
Isotopes
Naturellement terbium survenant est composé de sa seule stable isotope , le terbium-159; l'élément est donc appelé mononuclidic et monoisotopique. 36 des radio-isotopes ont été caractérisés, à être le plus lourd terbium-171 (avec masse atomique de 170,95330 (86) u) et le plus léger être terbium 135 (exacte inconnue masse). Le plus stable radio-isotope synthétique de terbium sont terbium-158, avec une demi-vie de 180 ans et terbium-157, avec une demi-vie de 71 ans. Tout le reste isotopes radioactifs ont des demi-vies qui sont bien moins d'un quart un an, et la majorité d'entre eux ont des demi-vies qui sont moins d'une demi-minute. Le primaire mode de désintégration avant l'isotope stable le plus abondant, 159 Tb, est capture d'électrons, ce qui conduit à la production de gadolinium isotopes, et le mode primaire est-après désintégration bêta moins, résultant en dysprosium isotopes.
L'élément 27 comporte également isomères nucléaires, avec des masses de 141 à 154, 156 et 158 (pas tous un numéro de masse correspond à un seul isomère). Le plus stable d'entre eux sont terbium 156m, avec demi-vie de 24,4 heures et de terbium-156m2, avec demi-vie de 22,7 heures; ce est plus longue que la demi-vie de la plupart des états fondamentaux d'isotopes radioactifs de terbium, sauf que ceux qui ont des nombres de masse de 155 à 161.
Histoire
Terbium a été découvert en 1843 par la Suède chimiste Carl Gustaf Mosander, qui détecté comme une impureté dans L'oxyde d'yttrium, Y 2 O 3, et nommé d'après le village Ytterby en Suède . Il n'a pas été isolé sous forme pure jusqu'à l'avènement récent de techniques d'échange d'ions.
Lorsque Mosander premier partitionné "yttrium" en trois fractions, "terbia" était la fraction qui contenait la couleur rose (en raison de ce qui est maintenant connu comme l'erbium), et "erbia" était la fraction qui était essentiellement incolore en solution, mais a donné une l'oxyde brun teinté. Plus tard, les travailleurs avaient de la difficulté à observer cette dernière, mais la fraction rose était impossible de manquer. Arguments allaient et venaient de savoir si "erbia" a même existé. Dans la confusion, les noms originaux se sont inversés, et l'échange des noms bloqués. On pense maintenant que les travailleurs qui ont utilisé la double sodium ou des sulfates de potassium pour éliminer les "oxyde cérique" de "l'oxyde d'yttrium" perdue par inadvertance, la teneur en terbium du système dans le précipité contenant l'oxyde de cérium. En tout cas, ce qui est maintenant connu comme le terbium était que d'environ 1% de l'oxyde d'yttrium originale, mais ce était suffisant pour conférer une couleur jaunâtre à l'oxyde. Ainsi, le terbium est un composant mineur dans la fraction originale de terbium, dominé par ses voisins immédiats, le gadolinium et dysprosium . Par la suite, chaque fois que d'autres terres rares ont été taquiné dehors de ce mélange, selon fraction a donné l'oxyde brun conservé le nom de terbium, jusqu'à ce qu'enfin il était pur. Les enquêteurs du 19ème siècle ne ont pas l'avantage de la technologie de fluorescence, de quoi observer la fluorescence brillante qui aurait rendu cet élément beaucoup plus facile à suivre dans des mélanges.
Occurrence

Terbium est jamais trouvé dans la nature par elle-même, mais est contenu avec d'autres éléments des terres rares dans de nombreux minéraux, y compris monazite ((Ce, La, Th, Nd, Y) PO 4 avec jusqu'à 0,03% de terbium), xénotime (YPO 4) et euxenite ((Y, Ca, Er, La, Ce, U, Th) (Nb, Ta, Ti) 2 O 6 avec 1% ou plus du terbium). L'abondance de croûte de terbium est estimé à 1,2 mg / kg.
Actuellement, les sources commerciales les plus riches de terbium sont les ions adsorption argiles de sud de la Chine; les concentrés avec les deux tiers environ de l'oxyde d'yttrium en poids sont d'environ 1% oxyde de terbium. De petites quantités de terbium se produisent dans bastnäsite et monazite; lorsque celles-ci sont traitées par extraction par solvant pour récupérer les lanthanides lourds précieux comme le samarium - europium - gadolinium concentré, le terbium y est récupéré. En raison des grands volumes de bastnäsite transformés par rapport aux argiles ions adsorption, une proportion importante de l'approvisionnement de terbium du monde vient de bastnäsite.
Production
Crushed minéraux contenant terbium sont traités avec concentré chaud de l'acide sulfurique pour produire des sulfates de terres rares solubles dans l'eau. Les filtrats acides sont partiellement neutralisés avec de la soude caustique à un pH de 3-4. thorium précipite dans la solution sous forme d'hydroxyde et est enlevée. Après que la solution est traitée avec oxalate d'ammonium pour convertir les terres rares dans leur insoluble oxalates. Les oxalates sont convertis en oxydes par recuit. Les oxydes sont dissous dans de l'acide nitrique qui exclut l'un des principaux composants, le cérium, dont l'oxyde est insoluble dans HNO 3. Terbium est séparé comme un double sel avec du nitrate d'ammonium par cristallisation.
La routine de séparation la plus efficace pour le sel de terbium à partir de la solution de sel de terre rare est l'échange d'ions. Dans ce procédé, les ions de terres rares sont adsorbés sur la résine échangeuse d'ions appropriée, par échange avec de l'hydrogène, l'ammonium ou des ions cuivriques présents dans la résine. Les ions de terre rare sont ensuite lavées de façon sélective par un agent complexant approprié. Comme avec d'autres terres rares, le terbium métallique est produit par la réduction du chlorure ou du fluorure anhydre avec le métal de calcium. De calcium et de tantale impuretés peuvent être éliminés par refusion sous vide, la distillation, la formation ou l'amalgame fusion de zone.
Applications
Terbium est utilisé comme En dopant le fluorure de calcium, le calcium et le tungstate de strontium molybdate, les matériaux qui sont utilisés dans des dispositifs à semi-conducteurs, et en tant que stabilisant des cristaux de les piles à combustible qui fonctionnent à des températures élevées, ainsi que ZrO 2.
Terbium est également utilisé dans alliages et dans la production de dispositifs électroniques. En tant que composante de Terfenol-D, le terbium est utilisé dans actionneurs, dans navale systèmes sonar, des capteurs, dans le Dispositif Soundbug (sa première application commerciale de), et d'autres dispositifs magnétomécaniques. Terfenol-D est un alliage qui se dilate ou se contracte en présence d'un champ magnétique. Il a le plus haut magnétostriction selon l'une quelconque alliage.
Terbium oxyde est utilisé en vert phosphores dans des tubes de lampes fluorescentes et TV couleur. Sodium terbium borate est utilisé en dispositifs à l'état solide. La fluorescence brillante terbium permet d'être utilisé comme sonde dans la biochimie, où il ressemble quelque peu calcium dans son comportement. Terbium luminophores "verts" (qui fluorescent un citron jaune brillante) sont combinés avec l'europium divalent luminophores bleus et l'europium trivalent luminophores rouges pour fournir le " «La technologie d'éclairage trichrome qui est de loin le plus grand consommateur de l'approvisionnement de terbium du monde. Trichromatic d'éclairage fournit une sortie beaucoup plus de lumière pour une quantité donnée d'énergie électrique que ne le fait éclairage incandescent.
Précautions
Comme avec les autres lanthanides , composés de terbium sont de toxicité faible à modérée, bien que leur toxicité n'a pas été étudiée en détail. Terbium a pas connu rôle biologique.

