
Darmstadtium
À propos de ce écoles sélection Wikipedia
Cette sélection écoles a été choisi par SOS Enfants pour les écoles dans le monde en développement ne ont pas accès à Internet. Il est disponible en téléchargement intranet. Parrainage d'enfants aide les enfants du monde en développement à apprendre aussi.
| Darmstadtium | |||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
110 Ds | |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| Apparence | |||||||||||||||||||||||||||||||||||||
| inconnu | |||||||||||||||||||||||||||||||||||||
| Propriétés générales | |||||||||||||||||||||||||||||||||||||
| Nom, symbole, nombre | darmstadtium, Ds, 110 | ||||||||||||||||||||||||||||||||||||
| Prononciation | / ré ɑr m ʃ t ɑː t Je ə m / Darm- SHTAHT -ee-əm | ||||||||||||||||||||||||||||||||||||
| Catégorie Metallic | inconnu mais probablement un métal de transition | ||||||||||||||||||||||||||||||||||||
| Groupe, période, bloc | 10, 7, ré | ||||||||||||||||||||||||||||||||||||
| Poids atomique standard | [281] | ||||||||||||||||||||||||||||||||||||
| Configuration électronique | [ Rn ] 5f 14 6d 8 7s 2 (Prévue) 2, 8, 18, 32, 32, 16, 2 (Prévue) ![coquilles d'électrons de darmstadtium (2, 8, 18, 32, 32, 16, 2 (prévue) [2])](../../images/1190/119044.png) | ||||||||||||||||||||||||||||||||||||
| Histoire | |||||||||||||||||||||||||||||||||||||
| Découverte | Gesellschaft für Schwerionenforschung (1994) | ||||||||||||||||||||||||||||||||||||
| Propriétés physiques | |||||||||||||||||||||||||||||||||||||
| Phase | solide (prévue) | ||||||||||||||||||||||||||||||||||||
| Densité (à proximité rt) | 34,8 (prévue) g · cm -3 | ||||||||||||||||||||||||||||||||||||
| Propriétés atomiques | |||||||||||||||||||||||||||||||||||||
| États d'oxydation | 8, 6, 4, 2, 0 (prévue) | ||||||||||||||||||||||||||||||||||||
| énergies d'ionisation ( plus) | 1er: 955,2 (estimation) kJ · mol -1 | ||||||||||||||||||||||||||||||||||||
| 2ème: 1891,1 (estimation) kJ · mol -1 | |||||||||||||||||||||||||||||||||||||
| 3ème: 3029,6 (estimation) kJ · mol -1 | |||||||||||||||||||||||||||||||||||||
| Rayon atomique | 118 (estimation) h | ||||||||||||||||||||||||||||||||||||
| Rayon covalente | 128 (estimation) h | ||||||||||||||||||||||||||||||||||||
| Miscellanées | |||||||||||||||||||||||||||||||||||||
| Numéro de registre CAS | 54083-77-1 | ||||||||||||||||||||||||||||||||||||
| La plupart des isotopes stables | |||||||||||||||||||||||||||||||||||||
| Article détaillé: Isotopes de darmstadtium | |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
Darmstadtium est un élément chimique avec le symbole Ds et de numéro atomique 110. Ce est un très radioactif élément synthétique (un élément qui peut être créé dans un laboratoire, mais ne se trouve pas dans la nature). Le connue plus stable isotope , darmstadtium-281, a une demi-vie d'environ 11 secondes, mais il est possible que cette isotopes darmstadtium peut avoir un isomère avec une demi-vie plus longue, 3,7 minutes. Darmstadtium a été créé en 1994 par le Centre de recherche sur les ions lourds proximité Darmstadt, Allemagne. Il a été nommé d'après la ville de Darmstadt, où il a été découvert.
Dans le tableau périodique , ce est un D-Block Transactinide. Ce est un membre de la Septième période et est placé dans le groupe 10 éléments, même si aucune des expériences chimiques ne ont pas encore été réalisées pour confirmer qu'il se comporte comme le plus lourd homologue de platine dans le groupe 10. Darmstadtium est calculé pour avoir des propriétés semblables à ses homologues plus légers, le nickel , le palladium et le platine.
Histoire
Découverte
Darmstadtium était d'abord créé le 9 Novembre 1994, à la Institut de Recherche des Ions Lourds (Gesellschaft für Schwerionenforschung) dans Darmstadt, Allemagne , par Peter Armbruster et Gottfried Münzenberg, sous la direction de Sigurd Hofmann. L'équipe bombardé un plomb -208 cible avec noyaux accélérés nickel-62 et détecté un seul atome de l'isotope darmstadtium-269:
- 208
82 Pb + 62
28 Ni → 269
110 1 + Ds
0 n
Dans la même série d'expériences, la même équipe a également réalisé la réaction en utilisant lourds nickel-64 ions. Pendant deux points, 9 atomes de 271 Ds ont été détectés de façon convaincante par corrélation avec les propriétés de désintégration fille connus:
- 208
82 Pb + 64
28 Ni → 271
110 1 + Ds
0 n
Le UICPA / IUPAP Groupe de travail mixte (GTM) a reconnu l'équipe GSI comme découvreurs dans leur rapport de 2001.
Appellation
Le nom darmstadtium (Ds) a été proposé par l'équipe GSI en l'honneur de la ville de Darmstadt, où l'élément a été découvert. L'équipe à l'origine GSI également considéré nommer l'élément wixhausium, après la banlieue de Darmstadt connu sous le nom Wixhausen où l'élément a été découvert, mais a finalement décidé sur darmstadtium. Le nouveau nom a été officiellement recommandé par IUPAC, le 16 Août 2003.
Nucléosynthèse
Éléments super-lourds tels que darmstadtium sont produites en bombardant des éléments plus légers dans les accélérateurs de particules qui induisent les réactions de fusion. Alors que la plupart des isotopes de darmstadtium peut être synthétisé directement de cette façon, certains plus lourds ne ont été observés que les produits de désintégration d'éléments plus élevés avec des numéros atomiques .
Selon les énergies mises en jeu, les premiers sont séparés en "chaud" et "froid". Dans les réactions de fusion à chaud, très légers, projectiles à haute énergie sont accélérés vers des objectifs très lourds ( actinides ), donnant lieu à des noyaux composés à haute énergie d'excitation (~ 40-50 MeV) qui peut soit la fission ou se évaporer plusieurs (3-5) neutrons. Dans les réactions de fusion à froid, les noyaux condensés produits ont une énergie relativement faible d'excitation (~ 10 à 20 MeV), ce qui diminue la probabilité que ces produits vont subir des réactions de fission. Comme les noyaux fusionnés refroidir à la état fondamental, ils ont besoin de l'émission de seulement un ou deux neutrons, et donc, permet la génération de produits plus riches en neutrons. Cette dernière est une notion distincte de celle de la fusion nucléaire selon lequel à atteindre dans des conditions de température ambiante (voir la fusion à froid).
La fusion froide
Avant la première synthèse réussie de darmstadtium en 1994 par le Équipe GSI, les scientifiques de GSI a également essayé de synthétiser darmstadtium en bombardant plomb-208 avec du nickel-64 en 1986. Aucun atomes de darmstadtium ont été identifiés. Après une mise à niveau de leurs installations, l'équipe de GSI détecté avec succès 9 atomes de 271 Ds en deux manches de leur expérience de découverte en 1994. Cette réaction a été répétée avec succès en 2000 par GSI (4 atomes), en 2000 et 2004 par le Lawrence Berkeley National Laboratory (LBNL) (9 Les atomes au total) et en 2002 par RIKEN (14 atomes). L'équipe a étudié la GSI réaction analogue avec le nickel-62 au lieu de nickel-64 en 1994 dans le cadre de leur expérience de découverte. Trois atomes de 269 Ds ont été détectés. Une quatrième chaîne de désintégration a été mesurée, mais a par la suite rétracté.
En plus des réactions officielles de découverte, en Octobre-Novembre 2000, l'équipe de GSI a également étudié la réaction analogue en utilisant une cible de plomb-207 afin de synthétiser le nouvel isotope 270 Ds. Ils ont réussi à synthétiser huit atomes de 270 Ds, relative à un isomère de l'état du sol, 270 Ds, et un haut tourner état métastable, 270m Ds.
En 1986, une équipe à la Institut unifié de recherches nucléaires (JINR) dans Dubna, en Russie , a étudié la réaction:
- 209
83 Bi + 59
27 Co → 267
110 1 + Ds
0 n
Ils étaient incapables de détecter les atomes de darmstadtium. En 1995, l'équipe de LBNL ont indiqué qu'ils avaient réussi à détecter un seul atome de 267 Ds utilisant cette réaction. Cependant, plusieurs désintégrations ont pas été mesurés et d'autres recherches sont nécessaires pour confirmer cette découverte.
Fusion chaude
En Septembre 1994, l'équipe de Dubna détecté un seul atome de 273 Ds en bombardant une cible de plutonium-244 avec accélérés soufre -34 noyaux.
Des expériences ont été réalisées en 2004 au Laboratoire Flerov de réactions nucléaires de Doubna étudier les caractéristiques de fission du noyau composé 280 Ds, produits par la réaction nucléaire:
- 232
90 Th + 48
20 Ca → 280
110 * Ds → fission
Le résultat a révélé comment noyaux composés tel fission principalement en expulsant magie et noyaux doublement magiques tels que 132 Sn ( Z = 50, N = 82). Aucun atomes de darmstadtium ont été obtenus. Un noyau composé est une combinaison libre de nucléons qui ne ont pas eux-mêmes disposés dans coquilles nucléaires encore. Il n'a pas de structure interne et est maintenu seulement par les forces de collision entre les cibles et les noyaux de projectiles. On estime qu'il faut environ 10 -14 s pour les nucléons à se organiser dans des coquilles nucléaires, à quel point le noyau composé devient un nucléide, et ce nombre est utilisé par IUPAC comme le minimum demi-vie d'un isotope revendiqué doit avoir potentiellement être reconnu comme être découvert. Ainsi, l'isotope 280 Ds reste actuellement inconnu.
Comme produit de désintégration
| résidu d'évaporation | Observé isotope darmstadtium |
|---|---|
| 277 Cn | 273 Ds |
| Fl 285, 281 Cn | 277 Ds |
| Lv 291, 287 Fl, 283 Cn | 279 Ds |
| Lv 293, 289 Fl, 285 Cn | 281 Ds |
Darmstadtium a été observé que les produits de désintégration de copernicium . Copernicium dispose actuellement de six isotopes connus, dont quatre ont été montrés à subir alpha se désintègre pour devenir noyaux darmstadtium, avec nombres de masse entre 273 et 281. Darmstadtium isotopes à des nombres de masse 277, 279 et 281 à ce jour ne ont été générées par des noyaux de copernicium décroissance. Noyaux copernicium parents peuvent eux-mêmes les produits de désintégration être Flérovium ou Livermorium . À ce jour, pas d'autres éléments ont été connus pour se dégrader à darmstadtium. Par exemple, en 2004, l'équipe Dubna ( JINR) identifié darmstadtium-281 comme un produit de la désintégration de Livermorium via une séquence de désintégration alpha:
- 293
116 289 Lv →
114 Fl + 4
2 Il - 289
114 285 Fl →
112 Cn + 4
2 Il - 285
112 281 Cn →
110 Ds + 4
2 Il
Isotopes
| Isotope | Demi-vie | Pourriture mode | Découverte année | Réaction |
|---|---|---|---|---|
| 267 Ds? | 2,8 ps | α | 1994 | 209 Bi (59 Co, n) |
| 268 Ds | 100? ps | α? | inconnu | - |
| 269 Ds | 179 | α | 1994 | 208 Pb (Ni 62, n) |
| 270 Ds | 100 ps | α, SF | 2000 | 207 Pb (Ni 64, n) |
| 270m Ds | 6.0 ms | α, IT | 2000 | 207 Pb (Ni 64, n) |
| 271 Ds | 1,63 ms | α | 1994 | 208 Pb (Ni 64, n) |
| 271m Ds | 69 | α | 1994 | 208 Pb (Ni 64, n) |
| 272 Ds | 1? s | SF? | inconnu | - |
| 273 Ds | 170 ps | α | 1996 | 244 Pu (S 34, 5n) |
| 274 Ds | 2? s | α, SF? | inconnu | - |
| 275 Ds | 2? s | α? | inconnu | - |
| 276 Ds | 5? s | α? | inconnu | - |
| 277 Ds | 5,7 ms | α | 2010 | 285 Fl (-, 2α) |
| 278 Ds | 10? s | α, SF? | inconnu | - |
| 279 Ds | 0,18 | α, SF | 2002 | 291 Lv (-, 3α) |
| 280 Ds | 11? s | SF? | inconnu | - |
| 281 Ds | s | SF | 1999 | 289 Fl (-, 2α) |
| 281m Ds? | ~ 3,7 min | α | 1999 | 289 Fl (-, 2α) |
Darmstadtium n'a pas isotopes stables ou naturels. Plusieurs isotopes radioactifs ont été synthétisés dans le laboratoire, soit par fusion de deux atomes ou en observant la décroissance des éléments plus lourds. Huit isotopes différents de darmstadtium ont été rapportés avec les masses atomiques 267, 269-271, 273, 277, 279, et 281, bien que darmstadtium-267 ne est pas confirmée. Trois isotopes de darmstadtium, darmstadtium-270, darmstadtium-271, et darmstadtium-281, ont connu états métastables (bien que celle de darmstadtium-281 est non confirmée). La plupart de ces Decay principalement par désintégration alpha, mais certains subissent une fission spontanée.
La stabilité et la demi-vie
Tous les isotopes de darmstadtium sont extrêmement instables et radioactives; En général, les isotopes plus lourds sont plus stables que le briquet. L'isotope de darmstadtium connue plus stable, 281 Ds, est aussi le plus lourd isotope darmstadtium connu; il a une demi-vie de 11 secondes, même si un état métastable, 281m Ds, a été rapporté pour avoir une demi-vie plus longue d'environ 3,7 minutes. L'isotope 279 Ds a respectivement une demi-vie de 0,18 secondes. Les six isotopes restants et deux états métastables ont des demi-vies entre 1 microseconde et 70 millisecondes. Certains isotopes inconnus dans cette région, tels que 272 Ds, Ds, 274-276 et 280, Ds sont prédit également avoir assez longues demi-vies de quelques secondes. Avant sa découverte, 277 Ds a été prévu d'avoir aussi une longue demi-vie d'environ 5 secondes; cependant, il a depuis été trouvé avoir une demi-vie très courte de seulement 5,7 millisecondes.
L'isotope inconnue 284 Ds a été prévu pour être le plus stable vers désintégration bêta; cependant, aucun isotope darmstadtium connu a été observé à subir désintégration bêta. Calcul théorique dans un modèle de tunnel quantique reproduit la désintégration alpha expérimentale des données de demi-vie pour les isotopes de darmstadtium connus. On prévoit également que l'isotope 294 Ds inconnu, qui a un nombre magique de neutrons (184), aurait une demi-vie désintégration alpha de l'ordre de 311 années.
Isomérie nucléaire
- 281 Ds
La production de 281 Ds par la désintégration de 289 Fl ou 293 Lv a produit deux modes de désintégration très différentes. Le mode le plus commun et facilement confirmé est fission spontanée avec une demi-vie de 11 s. Un mode beaucoup plus rare et encore non confirmée est la désintégration alpha par l'émission d'une particule alpha d'énergie 8,77 MeV avec une demi-vie observée à environ 3,7 min. Cette décroissance est associée à une voie de désintégration unique à partir des nucléides parents et doit être associée à un niveau d'isomères. La demi-vie suggère qu'il doit être affecté à un état isomère mais d'autres recherches sont nécessaires pour confirmer ces informations.
- 271 Ds
données de déclin de la synthèse directe de 271 Ds indique clairement la présence de deux isomères nucléaires. La première émet des particules alpha avec des énergies 10,74 et 10,69 MeV et a une demi-vie de 1,63 ms. L'autre ne émet paricles alpha avec une énergie de 10,71 MeV et a une demi-vie de 69 ms. Le premier a été attribué à l'état du sol et ce dernier à un niveau d'isomères. Il a été suggéré que la proximité des énergies de désintégration alpha indique que le niveau d'isomères peut se décomposer essentiellement par un retard transition isomérique à l'état du sol, résultant en une énergie alpha mesurée identiques et une demi-vie combinée pour les deux processus.
- 270 Ds
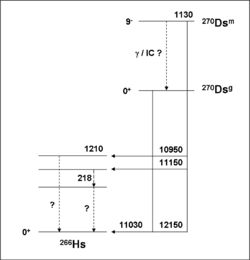
La production directe de 270 Ds a clairement identifié deux isomères nucléaires. L'état fondamental se désintègre par émission alpha dans l'état de 266 HS fondamental en émettant une particule alpha d'énergie 11,03 MeV et a une demi-vie de 0,10 ms. L'état métastable se désintègre par émission alpha, émettant des particules alpha avec des énergies de 12,15, 11,15 et 10,95 MeV, et a une demi-vie de 6 ms. Lorsque l'état métastable émet une particule alpha d'énergie 12,15 MeV, il se désintègre en l'état de 266 HS au sol, indiquant qu'il a 1,12 MeV de l'énergie excédentaire.
Propriétés prédites
Chimique
Darmstadtium est le huitième membre de la série 6d des métaux de transition . Depuis copernicium (élément 112) a été établi pour être un métal de transition, il est prévu que tous les éléments de 104 à 112 formeraient une quatrième série de métal de transition, avec darmstadtium dans le cadre de la des métaux du groupe du platine. Calculs sur son potentiels d'ionisation et atomique et rayons ioniques sont similaires à celle de son homologue briquet platine , ce qui implique que les propriétés de base de darmstadtium se apparentent à ceux de l'autre groupes 10 éléments, le nickel , le palladium et le platine.
Prédiction des propriétés chimiques probables de darmstadtium n'a pas reçu beaucoup d'attention récemment. Darmstadtium devrait être un métal noble. Basé sur des états d'oxydation les plus stables du groupe plus léger 10 éléments, états d'oxydation les plus stables de darmstadtium sont prévus pour être les six, quatre et deux États; Cependant, l'état neutre est prévu pour être le plus stable des solutions aqueuses. En comparaison, seulement platine est connue pour montrer l'état d'oxydation maximal dans le groupe, six, tandis que les Etats les plus stables sont quatre et deux à la fois pour le nickel et le palladium. Il est en outre attendu que les états d'oxydation maximal d'éléments de bohrium (élément 107) à darmstadtium (élément 110) peuvent être stables dans la phase gazeuse, mais pas en solution aqueuse. Hexafluorure darmstadtium (DSF 6) est supposé avoir des propriétés très similaires à son homologue plus léger platine hexafluorure (FTC 6), ayant des structures électroniques très similaires et potentiels d'ionisation.
Physique atomique et
Darmstadtium devrait être un solide dans des conditions normales. Il devrait être un métal très lourd avec une densité d'environ 34,8 g / cm 3. En comparaison, l'élément le plus dense connue qui a eu sa densité mesurée, l'osmium , a une densité de seulement 22,61 g / cm 3. Ceci résulte du poids atomique élevé de darmstadtium, le lanthanides et des actinides contractions, et effets relativistes, bien que la production d'une quantité suffisante darmstadtium pour mesurer cette quantité ne serait pas pratique, et l'échantillon serait rapidement se dégrader.
L'extérieur configuration électronique de darmstadtium est calculée comme étant de 8 7s 6d 2, qui obéit à la Principe Aufbau et ne suit pas la configuration électronique externe de platine 5d 9 6s 1. Ce est en raison de la stabilisation relativiste de la paire d'électrons 7s 2 sur toute la septième période, de sorte qu'aucun des éléments 104 à 112 ont des configurations d'électrons violer le principe Aufbau. Le rayon atomique de darmstadtium devrait se situer autour de 118 h.
Chimie expérimentale
De déterminer sans ambiguïté les caractéristiques chimiques de darmstadtium a encore ont été établis en raison de la courte demi-vie des isotopes de darmstadtium et un nombre limité de composés volatils susceptibles qui pourraient être envisagées sur une très petite échelle. Un des rares composés darmstadtium qui sont susceptibles d'être suffisamment volatile est darmstadtium hexafluorure (DSF 6), comme son platine hexafluorure homologue légers (FTC 6) est volatile supérieure à 60 ° C et donc le composé analogue de darmstadtium pourrait également être suffisamment volatile; un octafluoride volatile (DSF 8) pourrait également être possible. Pour les études chimiques à effectuer sur un transactinide, au moins quatre atomes doivent être produits, la demi-vie de l'isotope utilisé doit être d'au moins 1 seconde, et le taux de production doivent être au moins un atome par semaine. Même si la demi-vie de 281 Ds, isotope le plus stable confirmée de darmstadtium, est 11 secondes, assez longtemps pour effectuer des études chimiques, un autre obstacle est la nécessité d'augmenter le taux de production des isotopes de darmstadtium et de permettre des expériences de poursuivre pendant des semaines ou mois de sorte que des résultats statistiquement significatifs peuvent être obtenus. Séparation et de détection doivent être effectuées en continu pour séparer les isotopes de darmstadtium et les systèmes automatisés peuvent ensuite expérimenter sur la phase gazeuse et la chimie de la solution du darmstadtium que les rendements des éléments plus lourds sont prévus pour être inférieures à celles des éléments plus légers; quelques-unes des techniques de séparation utilisées pour bohrium et hassium peuvent être réutilisés. Cependant, la chimie expérimentale de darmstadtium n'a pas reçu autant d'attention que celle des éléments plus lourds copernicium et Flérovium .
Les plus neutrons riches en isotopes de darmstadtium sont les plus stables et sont donc plus prometteur pour les études chimiques; cependant, ils ne peuvent être produits indirectement de la désintégration alpha d'éléments plus lourds, et les méthodes de synthèse indirects ne sont pas favorables pour les études chimiques. Le plus riche en neutrons isotopes 276 et 277 Ds Ds peut être produit directement dans la réaction entre le thorium et -232 On se attend calcium-48, mais le rendement est faible. En outre, cette réaction a déjà été testé sans succès, et les expériences les plus récentes qui ont synthétisés avec succès 277 Ds utilisant des méthodes indirectes montrer qu'il a une demi-vie courte de 5,7 ms, pas assez de temps pour effectuer des études chimiques.

