
Étain
Saviez-vous ...
SOS Enfants, un organisme de bienfaisance de l'éducation , a organisé cette sélection. parrainage SOS enfant est cool!
| Étain | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
50 Sn | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apparence | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
argenté (à gauche, beta) ou gris (à droite, alpha)  | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés générales | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nom, symbole, nombre | étain, Sn, 50 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Prononciation | / t ɪ n / | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Élément Catégorie | post-métal de transition | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Groupe, période, bloc | 14, 5, p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poids atomique standard | 118,710 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuration électronique | [ Kr ] 4d 10 5s 2 5p 2 2, 8, 18, 18, 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Histoire | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Découverte | autour 3500 BC | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés physiques | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phase | solide | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densité (à proximité rt) | (Blanc) 7,365 g · cm -3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densité (à proximité rt) | (Gris) 5,769 g · cm -3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liquid densité au mp | 6,99 g · cm -3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point de fusion | 505,08 K , 231,93 ° C, 449,47 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point d'ébullition | 2875 K, 2602 ° C, 4716 ° F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| La chaleur de fusion | (Blanc) 7,03 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chaleur de vaporisation | (Blanc) 296,1 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacité thermique molaire | (Blanc) 27,112 J · mol -1 .K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| La pression de vapeur | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés atomiques | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| États d'oxydation | 4, 3, 2, 1, -4 ( l'oxyde amphotère) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Électronégativité | 1,96 (échelle de Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| énergies d'ionisation | 1e: 708,6 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2ème: 1411,8 kJ · mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3ème: 2943,0 kJ · mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon atomique | 140 h | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon covalente | 139 ± 16 heures | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon de Van der Waals | 217 h | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscellanées | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Crystal structure | quadrilatère  blanc | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Diamant gris | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordre magnétique | (Gris) diamagnétique, (blanc) paramagnétique | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Résistivité électrique | (0 ° C) 115 nΩ · m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivité thermique | 66,8 W · m -1 · K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dilatation thermique | (25 ° C) 22,0 um · m -1 · K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vitesse du son (tige mince) | ( rt) (laminés) 2730 m · s -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Le module d'Young | 50 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Module de cisaillement | 18 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Module Bulk | 58 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Coefficient de Poisson | 0,36 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureté Mohs | 1,5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureté Brinell | ~ 350 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numéro de registre CAS | 7440-31-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| La plupart des isotopes stables | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Article détaillé: Isotopes de l'étain | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
L'étain est un élément chimique avec le symbole Sn (pour latine : stannum) et de numéro atomique 50. C'est un groupe principal en métal groupe 14 du tableau périodique . Tin montre similarité chimique à la fois voisin groupe 14 éléments, le germanium et entraîner et a deux possibles états d'oxydation , deux et un peu plus stable 4. Tin est l'élément le plus abondant 49e et a, avec 10 isotopes stables, le plus grand nombre de stables isotopes dans le tableau périodique. Tin est obtenue principalement de la minérale cassitérite, où il se produit comme dioxyde d'étain, SnO 2.
Ce argenté, malléable post-métal de transition ne est pas facile oxyder à l'air et est utilisé pour revêtir d'autres métaux pour empêcher la corrosion . La première alliage, utilisés à grande échelle depuis 3000 BC, était bronze, un alliage d'étain et de cuivre . Après 600 BC pur étain métallique a été produit. Étain, qui est un alliage de 85 à 90% d'étain avec le reste couramment constitué par le cuivre, l'antimoine et le plomb, a été utilisé pour coutellerie du Âge du Bronze jusqu'au 20e siècle. Dans les temps modernes étain est utilisé dans de nombreux alliages, notamment l'étain / plomb doux les soudures, contenant typiquement 60% ou plus de l'étain. Une autre grande demande d'étain est résistant à la corrosion étamage de l'acier. En raison de sa faible toxicité, le métal étamé est également utilisé pour l'emballage alimentaire, ce qui donne le nom à Boîtes de conserve, qui sont faites principalement de l'acier.
Caractéristiques
Propriétés physiques

L'étain est un malléable, ductile et très cristallin blanc argenté métallique . Lorsqu'une barre d'étain est pliée, un crépitement connu sous le nom étain cri peut être entendu en raison de la jumelage des cristaux. Étain fond à une température basse d'environ 232 ° C (449,6 ° F), qui est en outre réduite à 177,3 ° C (351 ° F) pour des particules de 11 nm.
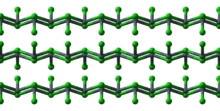
β-étain (sous forme métallique, ou de l'étain blanc), qui est stable à la température et au-dessus de la chambre, est malléable. En revanche, les α-étain (sous forme non métallique, ou de l'étain gris), qui est stable en dessous de 13,2 ° C (56 ° F), est cassants. α-étain a une Diamant la structure cristalline similaire à du diamant , du silicium ou du germanium . α-étain n'a pas de propriétés métalliques du tout parce que ses atomes forment une structure covalente où les électrons ne peuvent pas se déplacer librement. Ce est une matière pulvérulente gris mat sans utilisations courantes, autre que quelques spécialisés semi-conducteurs applications. Ces deux allotropes , α-β-étain et étain, sont plus communément connus comme l'étain et de l'étain gris blanc, respectivement. Deux autres allotropes, γ et σ, existent à des températures supérieures à 161 ° C (322 ° F) et des pressions supérieures à plusieurs GPa. Par temps froid, β-étain a tendance à se transformer spontanément en α-étain, un phénomène connu comme " étain parasite ". Bien que la température de transformation α-β est nominalement 13,2 ° C, les impuretés (par exemple, Al, Zn, etc.) abaisser la température de transition bien en dessous de 0 ° C (32 ° F), et lors de l'addition de Sb ou Bi le la transformation ne peut pas se produire du tout, ce qui augmente la durabilité de l'étain.
Les qualités commerciales d'étain (99,8%) résistent à la transformation en raison de l'effet inhibiteur des petites quantités de bismuth, d'antimoine, de plomb et d'argent présents sous forme d'impuretés. Des éléments d'alliage tels que le cuivre, l'antimoine, le bismuth, le cadmium et l'argent augmenter sa dureté. Tin tend assez facilement pour former des phases intermétalliques dures et fragiles, qui sont souvent indésirable. Il ne fait pas de larges gammes de solution solide dans d'autres métaux en général, et il existe peu d'éléments qui ont une solubilité appréciable dans l'étain solide. Simple systèmes eutectiques, cependant, se produisent avec le bismuth , le gallium , le plomb , le thallium et le zinc .
Tin devient un supraconducteur en dessous de 3,72 K . En fait, l'étain était l'un des premiers supraconducteurs à étudier; la L'effet Meissner, l'un des traits caractéristiques de supraconducteurs, a été découvert dans les cristaux d'étain supraconducteur.
Propriétés chimiques
Tin résiste à la corrosion de l'eau , mais peut être attaqué par les acides et alcalis. Tin peut être hautement polie et est utilisé comme couche protectrice pour d'autres métaux. Dans ce cas, la formation d'une couche d'oxyde de protection est utilisé pour empêcher une oxydation ultérieure. Cette forme de couche d'oxyde sur l'étain et d'autres alliages d'étain. Tin agit en tant que catalyseur lors de l'oxygène est en solution et aide à accélérer l'attaque chimique.
Isotopes
L'étain est l'élément avec le plus grand nombre d' isotopes stables , dix; il se agit notamment tous ceux qui ont des masses atomiques entre 112 et 124, à l'exception de 113, 121 et 123. Parmi ceux-ci, les plus abondantes sont celles les 120 Sn (presque un tiers de tous étain), 118 Sn, Sn et 116, tandis que l'abondant moins est de 115 Sn. Les isotopes possédant même nombres de masse ne ont pas spin nucléaire tandis que les impairs ont un spin +1/2. Tin, avec ses trois isotopes communs Sn 115, 117 et 119 Sn Sn, est parmi les éléments les plus faciles à détecter et analyser par spectroscopie RMN , et son déplacements chimiques sont référencés contre SnMe 4.
Ce grand nombre d'isotopes stables est considéré comme un résultat direct de l'étain possédant un numéro atomique de 50, qui est un " nombre magique »en physique nucléaire. Il ya 28 isotopes instables supplémentaires qui sont connus, englobant tous ceux qui restent avec des masses atomiques entre 99 et 137. Mis à part 126 Sn, qui a une demi-vie de 230.000 ans, tous les isotopes radioactifs ont une demi-vie de moins d'un an. Le radioactifs 100 Sn est l'un des rares nucléides possédant un " magie doublement "noyau et a été découvert relativement récemment, en 1994. Un autre 30 isomères métastables ont été caractérisées pour les isotopes entre 111 et 131, le plus stable dont être 121m Sn, avec une demi-vie de 43,9 années.
Étymologie
Le mot anglais «étain» est Germanique; mots liés se trouvent dans l'autre germanique langues- allemande Zinn, Tenn suédois, néerlandais étain, etc. -mais non dans d'autres branches de Indo-européenne, sauf en empruntant (par exemple, Tinne irlandaise). Son origine est inconnue.
Le latine nom stannum signifiait à l'origine d'un alliage d'argent et de plomb, et est venu à signifier «étain» dans la BCE-mot latin tôt 4ème siècle car il a été plumbum candidum 'céruse. Stannum apparemment provenait d'une Stagnum plus tôt (ce qui signifie la même substance), l'origine de la Romance et Conditions celtiques pour 'étain ». L'origine de stannum / Stagnum est inconnu; il peut être pré- Indo-européenne. Le Meyers Konversationslexikon spécule au contraire que stannum est dérivé de Cornish stean, et est la preuve que Cornwall dans le premiers siècles a été la principale source d'étain.
Histoire

Extraction et l'utilisation de l'étain peuvent être datées aux débuts de l'âge du bronze vers 3000 avant JC, quand il a été observé que cuivre objets formés de polymétallique minerais ayant des teneurs en métal ont des propriétés physiques différentes. Les premiers objets en bronze ou étain avaient teneur en arsenic inférieure à 2%, et sont donc considérés comme étant le résultat d'involontaire alliage en raison de la teneur en oligo-métal dans le minerai de cuivre. L'addition d'un second métal de cuivre augmente sa dureté, abaisse la température de fusion, et améliore la Procédé de coulée en produisant une masse fondue fluide qui refroidit plus à un métal plus dense, moins spongieux. Ce était une innovation importante qui a permis aux formes beaucoup plus complexes exprimés fermé moules de l'âge du bronze. Objets en bronze arsenic apparaissent d'abord dans le Proche-Orient où l'arsenic est communément trouvée en association avec le minerai de cuivre, mais le risques pour la santé ont été rapidement réalisés et la recherche de sources de minerais beaucoup moins dangereux d'étain ont commencé au début de l'âge du bronze. Cela a créé de la demande d'étain métal rare et a formé un commerce réseau qui reliait les sources éloignées de l'étain pour les marchés de l'âge du bronze cultures .
Cassitérite (SnO 2), la forme d'oxyde d'étain d'étain, était probablement la source originale de l'étain dans les temps anciens. D'autres formes de minerais d'étain sont moins abondantes les sulfures tels que stannite qui nécessitent un plus impliqué processus de fusion. Cassitérite accumule souvent canaux alluviales comme dépôts en raison du fait qu'il est plus difficile, plus lourd et plus résistant chimiquement à la alluvionnaires granit dans laquelle il forme généralement. Ces dépôts peuvent être facilement observés dans les berges des rivières comme la cassitérite est généralement noir, violet ou autrement de couleur sombre, une caractéristique exploitée par les premiers Age du Bronze prospecteurs . Il est probable que les premiers dépôts sont alluvial dans la nature, et peut-être exploités par les mêmes procédés utilisés pour le panoramique or dans dépôts alluvionnaires.
Les composés et la chimie
Dans la grande majorité de ses composés, l'étain a l'état d'oxydation II ou IV.
Composés inorganiques
Composés halogénures sont connus pour les deux états d'oxydation. Pour Sn (IV), tous les quatre halogénures sont bien connus: SnF 4, SnCl 4, SnBr 4, et SnI 4. Les trois membres les plus lourds sont composés moléculaires volatils, alors que le tétrafluorure est polymère. Les quatre halogénures sont connus pour Sn (II) également: SnF 2, SnCl 2 , SnBr 2, et SnI 2. Tous sont des matières solides polymères. De ces huit composés, seuls les iodures sont colorés.
Tin chlorure (II) (également connu comme le chlorure stanneux) est le plus important halogénure d'étain dans un sens commercial. Illustrant les itinéraires de tels composés, le chlore réagit avec de l'étain métallique pour donner SnCl 4 tandis que la réaction de l'acide chlorhydrique et d'étain SnCl 2 et donne de l'hydrogène gazeux. Alternativement SnCl 4 et Sn se combinent pour chlorure d'étain via un processus appelé comproportionation:
- SnCl 4 + Sn → 2 SnCl 2
Tin peut former de nombreux oxydes, les sulfures et autres dérivés de chalcogénure. Le dioxyde de SnO 2 (cassitérite) lorsque les formes d'étain est chauffé en présence d' air . SnO 2 est amphotères, ce qui signifie qu'il se dissout dans des solutions acides et basiques. Il ya stannates aussi avec la structure [Sn (OH) 6] 2-, comme K 2 [Sn (OH) 6], bien que la libre stannique acide H 2 [Sn (OH) 6] est inconnue. Le sulfures d'étain existent dans les deux états d'oxydation 2 et 4: étain (II) et le sulfure de étain (IV) sulfure ( or mosaïque).
Hydrures
Stannane (SNH 4), où l'étain est dans l'état d'oxydation +4, est instable. Hydrures organostanniques sont cependant bien connus, par exemple, l'hydrure de tributylétain (Sn (C 4 H 9) 3 H). Ces radicaux transitoire tributylétain composé de libération, rares exemples de composés d'étain (III).
Les composés organostanniques
Les composés organostanniques, parfois appelés stannanes, sont composés chimiques avec des liaisons carbone-étain. Parmi les composés de l'étain, les dérivés organiques sont les plus utiles dans le commerce. Certains composés organostanniques sont très toxiques et ont été utilisés comme des biocides. Le premier composé d'organo-étain à déclarer a été diiodure diéthylétain ((C 2 H 5) 2 SnI 2), rapporté par Edward Frankland en 1849.
La plupart des composés organostanniques sont des liquides incolores ou solides qui sont stables à l'air et de l'eau. Ils adoptent la géométrie tétraédrique. Composés tétraalkyl et tetraaryltin peuvent être préparés en utilisant Des réactifs de Grignard:
- SnCl 4 + 4 RMgBr → R 4 Sn + 4 MgBrCl
Les halogénures-alkyles mixtes, qui sont plus fréquentes et plus importante dans le commerce que les dérivés de tetraorgano, sont préparés par redistribution réactions:
- SnCl 4 + 4 Sn → R 2 SnCl 2 R 2
Composés organostanniques divalent sont rares, bien plus commun que divalent connexes organogermanium et des composés organosiliciés. La plus grande stabilisation apprécié par Sn (II) est attribué au " . inerte effet de paire "composés organostanniques (II) comprennent deux stannylènes (formule: R 2 Sn, comme on le voit pour singulet carbènes) et distannylenes (R 4 Sn 2), qui sont à peu près équivalent à alcènes . Les deux classes présentent des réactions inhabituelles.
Occurrence


L'étain est générée via la longue S-processus dans les étoiles de faible à moyenne de masse (avec des masses de 0,6 à 10 fois celle du Soleil ). Il se pose par l'intermédiaire désintégration bêta du isotopes lourds de l'indium .
Tin est l'élément le plus abondant dans le 49e Terre de la croûte , ce qui représente 2 ppm contre 75 ppm pour le zinc, 50 ppm pour le cuivre, et 14 ppm pour le plomb.
Tin ne se produit pas comme l'élément d'origine, mais doit être extrait de divers matériaux. Cassitérite (SnO 2) est la seule source importante dans le commerce de l'étain, bien que de petites quantités d'étain sont récupérés à partir complexe les sulfures tels que stannite, cylindrite, franckeite, canfieldite, et teallite. Minéraux avec l'étain sont presque toujours associés à granite rock, généralement à un niveau de 1% de teneur en oxyde d'étain.
En raison de la densité plus élevée de dioxyde d'étain, environ 80% de l'étain est extrait à partir de gisements secondaires trouvés en aval des filons primaires. L'étain est souvent récupéré à partir de granulés lavés en aval dans le passé et déposé dans les vallées ou sous la mer. Les moyens les plus économiques d'étain de l'exploitation minière sont travers dragage, méthodes hydrauliques ou l'exploitation minière à ciel ouvert. La plupart des étain du monde est produite à partir dépôts alluvionnaires, qui peuvent contenir aussi peu que 0,015% d'étain.
| Pays | Réserves |
|---|---|
| | 1500000 |
| | 250000 |
| 310000 | |
| | 800000 |
| | 590000 |
| | 400000 |
| | 350000 |
| | 170000 |
| | 180000 |
| Autre | 180000 |
| Total | 4800000 |
Environ 253 000 tonnes d'étain ont été exploités en 2011, principalement en Chine (110 000 t), en Indonésie (51 000 t), le Pérou (34 600 t), la Bolivie (20 700 t) et le Brésil (12 000 t). Estimations de la production d'étain ont toujours varié avec la dynamique de la faisabilité économique et le développement de technologies minières, mais il est estimé que, à des taux et des technologies de consommation actuels, la Terre sera à court d'étain qui peut être exploité en 40 ans. Cependant Lester Brown a suggéré l'étain pourrait manquer d'ici 20 ans basée sur une extrapolation très prudente de la croissance de 2% par an.
| Année | Millions de tonnes |
|---|---|
| 1965 | 4265 |
| 1970 | 3930 |
| 1975 | 9060 |
| 1980 | 9100 |
| 1985 | 3060 |
| 1990 | 7100 |
| 2000 | 7100 |
| 2010 | 5200 |
Secondaire, ou de la ferraille, l'étain est aussi une source importante du métal. La reprise de l'étain par la production secondaire, ou le recyclage des déchets d'étain, augmente rapidement. Alors que les Etats-Unis n'a ni exploité depuis 1993, ni l'étain fondu depuis 1989, il était le plus grand producteur secondaire, recyclage près de 14 000 tonnes en 2006.
De nouveaux gisements sont signalés à être dans le sud de la Mongolie , et en 2009, de nouveaux gisements d'étain ont été découverts en Colombie, Amérique du Sud, par le groupe Seminole Colombie CI, SAS.
Production
Tin est produit par réduction carbothermique d'oxyde minerai avec du carbone ou de coke. Les deux four à réverbère et four électrique peut être utilisé.
Mining and Smelting
Industrie

Les dix plus grandes entreprises ont produit la majeure partie de l'étain au monde en 2007. Il ne est pas clair laquelle de ces entreprises comprennent l'étain fondu de la mine à Bisie, République démocratique du Congo, qui est contrôlée par une milice rebelle et produit 15 000 tonnes. La plupart des étain du monde est cotée sur le London Metal Exchange (LME), à partir de 8 pays, moins de 17 marques.
| Société | Régime politique | 2006 | 2007 | % Variation |
|---|---|---|---|---|
| Yunnan Tin | Chine | 52339 | 61129 | 16,7 |
| PT Timah | Indonésie | 44689 | 58325 | 30,5 |
| Minsur | Pérou | 40977 | 35940 | -12,3 |
| Malais | Chine | 52339 | 61129 | 16,7 |
| Malaysia Smelting Corp | Malaisie | 22850 | 25471 | 11,5 |
| Thaisarco | Thaïlande | 27828 | 19826 | -28,8 |
| Yunnan Chengfeng | Chine | 21765 | 18000 | -17,8 |
| Liuzhou China Tin | Chine | 13499 | 13193 | -2,3 |
| EM Vinto | Bolivie | 11804 | 9448 | -20,0 |
| Or groupe Bell | Chine | 4696 | 8000 | 70,9 |
Prix et bourses
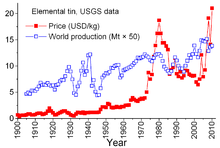
Tin est unique parmi les autres produits minéraux par les «accords» complexes entre pays producteurs et pays consommateurs datant de 1921. Les accords antérieurs avaient tendance à être quelque peu informel et sporadique; elles ont conduit à l '"Accord international sur l'étain d'abord" en 1956, la première d'une série numérotée en continu que, essentiellement, se est effondré en 1985. Grâce à cette série d'accords, les Conseil international de l'étain (ITC) a eu un effet considérable sur les prix de l'étain. L'ITC a soutenu le prix de l'étain pendant les périodes de bas prix en achetant étain pour son stock tampon et a été en mesure de retenir le prix pendant les périodes de prix élevés en vendant l'étain de la réserve. Ce était une approche anti-libre marché, destinée à assurer un flux suffisant d'étain vers les pays consommateurs et un profit décent pour les pays producteurs. Cependant, le stock tampon ne était pas suffisamment grande, et pendant la plupart de ces 29 années prix de l'étain ont augmenté, parfois fortement, en particulier de 1973 à 1980, lorsque l'inflation galopante en proie à de nombreuses économies mondiales.
À la fin des années 1970 et au début des années 1980, l'étain stocks gouvernement américain était dans un mode de vente agressive, en partie pour profiter des prix historiquement élevés de l'étain. La forte récession de 1981-1982 se est avéré être assez sévère sur l'industrie de l'étain. la consommation d'étain a diminué de façon spectaculaire. L'ITC a pu éviter des baisses vraiment raide à travers l'achat accéléré pour son stock tampon; cette activité a nécessité l'ITC d'emprunter largement auprès des banques et sociétés de négoce de métal pour augmenter ses ressources. Le CCI a continué à emprunter jusqu'à la fin de 1985, quand il a atteint sa limite de crédit. Immédiatement, un important "crise de l'étain" suivi - l'étain a été radiée de la cote de la négociation sur le London Metal Exchange pour environ 3 ans, l'ITC a dissous peu de temps après, et le prix de l'étain, maintenant dans un environnement de libre marché, a chuté brusquement à 4 $ par livres et est resté autour de ce niveau à travers des années 1990. Il a augmenté de nouveau d'ici à 2010 en raison de rebond de la consommation après la crise économique mondiale 2008-09, le repeuplement et la croissance continue de la consommation dans les économies en développement de la planète.
London Metal Exchange (LME) est le site principal de commerce de l'étain. Autres marchés de contrats d'étain sont Kuala Lumpur marché Tin (KLTM) et Indonésie Tin Exchange (INATIN).
Applications
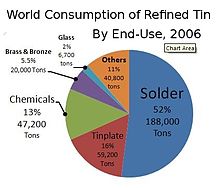
En 2006, environ la moitié de l'étain produit a été utilisé dans la soudure. Le reste a été réparti entre l'étamage, les produits chimiques de l'étain, laiton et le bronze, et les utilisations de niche.
Soudure

Étain est utilisé depuis longtemps en tant que braser sous la forme d'un alliage avec le plomb, l'étain représentant 5 à 70% en poids / poids. Tin forme un mélange eutectique de plomb contenant 63% d'étain et 37% de plomb. Ces soudures sont principalement utilisés pour les soudures pour les rejoindre tuyaux ou les circuits électriques. Depuis l'Union européenne Directive sur les déchets électroniques (directive DEEE) électrique et et Restriction of Hazardous Substances directive est entrée en vigueur le 1er Juillet 2006, l'utilisation du plomb dans ces alliages a diminué. Remplacement de plomb a de nombreux problèmes, y compris un point de fusion plus élevé, et la formation de moustaches d'étain causant des problèmes électriques. Tin ravageur peut se produire dans les soudures sans plomb, conduisant à la perte du joint soudé. alliages de remplacement sont rapidement trouvés, bien que des problèmes d'intégrité conjointe restent.
Étamage
Des liaisons étain facilement à fer et est utilisé pour le revêtement de plomb ou de zinc et de l'acier pour éviter la corrosion. Contenants en acier étamé sont largement utilisés pour la conservation des aliments, ce qui forme une grande partie du marché de l'étain métallique. Un bidon en fer blanc pour les denrées alimentaires a été fabriqué à Londres en 1812. Présidents de l'anglais britannique les appeler «boîtes», tandis que les locuteurs de l'anglais américain appellent " boîtes "ou" boîtes de conserve ". Une utilisation ainsi dérivé du terme d'argot" tinnie »ou« nasillard »signifie« canette de bière ". Le coup de sifflet de l'étain est appelé ainsi parce que ce était la première production de masse en acier étamé.
Alliages spécialisés

Tin en combinaison avec d'autres éléments formant une grande variété d'alliages utiles. Tin est le plus souvent allié avec le cuivre. L'étain est de 85 à 99% d'étain; Roulement métallique a un pourcentage élevé de l'étain ainsi. Bronze est surtout de cuivre (12% d'étain), tandis que l'addition de phosphore donne bronze phosphore. Cloche métal est également un alliage cuivre-étain contenant 22% d'étain. Tin a aussi parfois été utilisé dans la monnaie; par exemple, il a formé une fois un pourcentage de figure unique des pièces de monnaie américaines et canadiennes. Parce que le cuivre est souvent le métal majeur dans ces pièces, et le zinc est parfois présente ainsi, ceux-ci pourraient être techniquement appelés bronze et / ou en laiton alliages.

Le niobium composé -tin Nb 3 Sn est commercialement utilisé comme fils pour aimants supraconducteurs, en raison du matériau de haute température critique (18 K) et le champ magnétique critique (25 T). Aimant supraconducteur ne pesant que quelques kg est capable de produire des champs magnétiques comparables à un classique électro-aimant pesant tonnes.
Un ajout de quelques pour cent d'étain est couramment utilisé dans alliages de zirconium pour la gaine du combustible nucléaire.
La plupart des tubes métalliques dans un orgue à tuyaux sont en quantités variables d'un alliage étain / plomb, avec 50% / 50% étant le plus commun. La quantité d'étain dans la conduite définit le ton de la conduite, car l'étain est le plus tonalement résonance de tous les métaux. Quand un alliage étain / plomb refroidit, le plomb se refroidit légèrement plus rapide et produit un effet marbré ou tacheté. Cet alliage métallique est désigné comme métal tacheté. Les principaux avantages de l'utilisation de l'étain pour tuyaux comprennent son apparence, son aptitude au façonnage et résistance à la corrosion.
D'autres applications

Étain perforé, également appelé l'étain percé, est une technique artisanale originaire de l'Europe centrale pour créer des articles ménagers à la fois fonctionnel et décoratif. Motifs décoratifs perçants existent dans une grande variété, basée sur la géographie ou créations personnelles de l'artisan. Lanternes d'étain perforées sont l'application la plus courante de cette technique artisanale. La lumière d'une bougie qui brille à travers la conception percé crée un motif de lumière décorative dans la pièce où il se trouve. Lanternes d'étain perforées et autres articles d'étain perforées ont été créés dans le Nouveau Monde de la plus ancienne colonie européenne. Un exemple bien connu est le type lanterne Revere, nommé d'après Paul Revere.
Avant l'ère moderne, dans certaines régions des Alpes, une chèvre ou une corne de moutons seraient aiguisés et un panneau d'étain seraient découpés en utilisant l'alphabet et les chiffres de un à neuf. Cet outil d'apprentissage a été connue à juste titre comme «la corne». Reproductions modernes sont décorées avec des motifs tels que le cœur et les tulipes.
En Amérique, un coffre-fort à tarte et un coffre-fort alimentaires est entré en usage dans les jours avant la réfrigération. Ce étaient des armoires en bois de différents styles et de tailles - soit debout, au sol ou suspendus armoires destinées à décourager la vermine et les insectes et de garder la poussière de denrées périssables. Ces armoires ont inserts en fer blanc dans les portes et parfois sur les côtés, des coups de poing par le propriétaire, ébéniste ou ferblantier dans divers modèles pour permettre la circulation d'air. Reproductions modernes de ces articles restent populaires en Amérique du Nord.
verre de fenêtre est le plus souvent faite par flottante fondu verre sur le dessus d'étain fondu (création verre flotté) afin de produire une surface plane. Ceci est appelé la " Pilkington processus ".
Tin est également utilisé comme une électrode négative dans les batteries Li-ion. Son application est quelque peu limitée par le fait, que certaines surfaces d'étain catalysent la décomposition des électrolytes à base de carbonate utilisés dans les batteries Li-ion.
Étain (II) est ajouté du fluorure de certains produits de soins dentaires comme fluorure d'étain (SnF2). Étain (II) de fluorure peut être mélangé avec des abrasifs de calcium tandis que le plus commun le fluorure de sodium devient progressivement biologiquement inactif combiné avec des composés de calcium. Il a également été montré pour être plus efficace que le fluorure de sodium dans le contrôle de gingivite.
Les composés organostanniques
De tous les composés chimiques de l'étain, les composés organostanniques sont plus largement utilisés. La production industrielle mondiale dépasse probablement 50 000 tonnes.
Stabilisants pour PVC
L'application commerciale importante de composés organiques de l'étain est dans la stabilisation de Plastiques PVC. En l'absence de ces stabilisateurs, PVC dégraderait autrement rapidement sous la chaleur, la lumière et l'oxygène atmosphérique, pour donner décolorées, produits fragiles. Tin nettoie labile des ions chlorure (Cl -), qui, sinon, initier la perte de HCl à partir du matériau plastique. Des composés d'étain typiques sont des dérivés d'acides carboxyliques de dichlorure de dibutyl-étain, tels que le di laurate.
Biocides
composés organostanniques peuvent avoir une toxicité relativement élevée, ce qui est à la fois avantageuse et problématique. Ils ont été utilisés pour leur effets biocides / as fongicides, pesticides, algicides, préservation du bois, et agents antisalissures. l'oxyde de tributylétain est utilisé comme protection du bois. Tributylétain a été utilisé comme additif pour la peinture du navire pour empêcher la croissance des organismes marins à bord des navires, avec utilisation décroissante après composés organostanniques ont été reconnus comme les polluants organiques persistants dont la toxicité très élevé pour certains organismes marins, par exemple la buccin chien. L'UE a interdit l'utilisation de composés organostanniques en 2003, alors que les préoccupations sur la toxicité de ces composés sur la vie marine et leurs effets sur la reproduction et la croissance de certaines espèces marines, (certains rapports décrivent les effets biologiques à la vie marine à une concentration de 1 nanogramme par litre) ont conduit à une interdiction mondiale par le Organisation maritime internationale. De nombreux pays restreignent désormais l'utilisation de composés organostanniques aux navires de plus de 25 mètres de long.
Chimie organique
Certains étain les réactifs sont utiles dans la chimie organique . Dans la plus grande application, le chlorure stanneux est un réducteur commun pour la conversion de nitro et groupes oxime aux amines . Le Stille composés couples de réaction organostanniques avec organique des halogénures ou pseudohalogénures.
Les batteries Li-ion
formes d'étain plusieurs phases inter-métalliques avec du lithium métallique et il en fait un matériau potentiellement intéressante. Grand expansion volumétrique d'étain sur alliage avec Lithium et l'instabilité de l'interface d'électrolyte Tin-organique à faibles potentiels électrochimiques sont les plus grands défis dans l'employer dans les cellules commerciales. Le problème a été partiellement résolu par Sony. Composé inter-métallique Tin avec Cobalt, mélangé avec du charbon, a été mis en place par Sony dans ses cellules Nexelion publié en 2000 la fin des années. La composition des matériaux actifs est proche de Sn 0,3 Co 0,4 C 0,3. Des recherches récentes ont montré que seules certaines facettes cristallines de quadratique (beta) Sn sont responsables de l'activité électrochimique indésirable.
Précautions
Les cas d'intoxication d'étain métal, ses oxydes, et ses sels sont «presque inconnu». D'autre part, certaines composés organostanniques sont presque aussi toxiques que cyanure.

