
Dubnium
À propos de ce écoles sélection Wikipedia
Cette sélection écoles a été choisi par SOS Enfants pour les écoles dans le monde en développement ne ont pas accès à Internet. Il est disponible en téléchargement intranet. Parrainer un enfant de faire une réelle différence.
| Dubnium | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
105 Db | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apparence | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| inconnu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés générales | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nom, symbole, nombre | dubnium, Db, 105 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Prononciation | / ré U b n Je ə m / DOOB -neE-əm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Élément Catégorie | métal de transition | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Groupe, période, bloc | 5, 7, ré | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poids atomique standard | [268] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuration électronique | [ Rn ] 5f 14 6d 3 7s 2 (Prévue) 2, 8, 18, 32, 32, 11, 2 (Prévue)  | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Histoire | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Découverte | Institut unifié de recherches nucléaires (1968) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés physiques | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phase | solide (prévue) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densité (à proximité rt) | 29 (prévue) g · cm -3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés atomiques | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| États d'oxydation | 5, 4, 3 (prévue) (États d'oxydation ne en gras sont connus expérimentalement) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| énergies d'ionisation ( plus) | 1er: 664,8 (estimation) kJ · mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2ème: 1546,7 (estimation) kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3ème: 2378,4 (estimation) kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon atomique | 139 (estimation) h | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon covalente | 149 (estimation) h | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscellanées | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numéro de registre CAS | 53850-35-4 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| La plupart des isotopes stables | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Article détaillé: Isotopes de dubnium | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Dubnium est un élément chimique avec le symbole dB et de numéro atomique 105, nommé d'après la ville de Dubna en Russie , où il a été produit. C'est un élément synthétique (un élément qui peut être créé dans un laboratoire, mais ne se trouve pas dans la nature) et radioactifs; le connu plus stable isotope , dubnium-268, a une demi-vie d'environ 28 heures.
Dans le tableau périodique des éléments, ce est un élément d-bloc et dans le transactinide éléments. Ce est un membre de la 7e période et appartient à la groupe 5 élément. expériences de chimie ont confirmé que dubnium se comporte comme le plus lourd homologue de tantale dans le groupe 5. Les propriétés chimiques de dubnium se caractérisent en partie seulement. Ils sont similaires à ceux d'autres groupes 5 éléments.
Dans les années 1960, des quantités microscopiques de dubnium ont été produites dans les laboratoires de l'ex- Union soviétique et en Californie . La priorité de la découverte et donc la nommage de l'élément a été contestée entre les scientifiques soviétiques et américains, et ce ne est qu'en 1997 que Union internationale de chimie pure et appliquée (UICPA) a établi dubnium que le nom officiel de l'élément.
Histoire
Découverte
Dubnium aurait été découvert en 1968 à la Institut unifié de recherches nucléaires à Dubna (puis dans l' Union soviétique ). Les chercheurs y ont bombardé une cible américium-243 avec neon-22 ions . Ils ont rapporté un MeV 9,40 et un 9,70 MeV activité alpha et affectés les désintégrations de l'isotope 260 ou 261 Db Db:
- 243
95 Am + 22
10 Ne → 265- x
105 Db x + n
Deux ans plus tard l'équipe Dubna séparé leurs produits de réaction par Chromatographie gradient thermique après conversion en chlorures par interaction avec NbCl 5. L'équipe a identifié un 2,2 secondes activité spontanée de fission contenus dans un chlorure volatile dépeignant propriétés eka-tantale, susceptibles dubnium-261 pentachlorure, 261 DbCl 5.
Dans la même année, une équipe dirigée par Albert Ghiorso travaillant au Université de Californie, Berkeley concluante synthétisé l'élément en bombardant une cible californium 249 avec 15 ions azote. L'équipe a publié une synthèse convaincante de 260 Db dans la réaction entre cible californium-249 et azote 15 ions et mesuré la désintégration alpha de 260 Db avec une demi-vie de 1,6 secondes et une énergie de désintégration de 9,10 MeV, en corrélation avec la désintégration de fille de lawrencium -256:
- 249
98 Cf + 15
7 N → 260
105 Db + 4 n
Ces résultats par les scientifiques de Berkeley ne ont pas confirmé les soviétiques conclusions concernant l'9,40 MeV ou 9,70 MeV désintégration alpha de dubnium-260, ne laissant que dubnium-261 que possible isotope produit. En 1971, l'équipe Dubna répété leur réaction en utilisant un meilleur set-up et ont été en mesure de confirmer les données de décroissance pour 260 dB en utilisant la réaction:
- 243
95 Am + 22
10 Ne → 260
105 Db + 5 n
En 1976, l'équipe Dubna ont poursuivi leur étude de la réaction en utilisant la chromatographie gradient thermique et étaient en mesure d'identifier le produit comme dubnium-260 pentabromure, 260 DbBr 5.
En 1992, le UICPA / Groupe de travail Transfermium IUPAP évalué les demandes des deux groupes et a conclu que la confiance dans la découverte a grandi à partir des résultats des deux laboratoires et de la demande de la découverte doit être partagée.
Nommer la controverse


Le Soviet, plus tard, la Russie, l'équipe a proposé le nom nielsbohrium (Ns) en l'honneur du physicien nucléaire danois Niels Bohr . L'équipe américaine a proposé que le nouvel élément doit être nommé hahnium (Ha), en l'honneur de feu allemande chimiste Otto Hahn. Par conséquent hahnium était le nom que les scientifiques européens les plus américains et occidentaux utilisés et apparaît dans de nombreux articles publiés à l'époque, et nielsbohrium a été utilisé dans l'Union soviétique et Pays de l'Est.
Une élément nommer controverse a éclaté entre les deux groupes. Le Union internationale de chimie pure et appliquée (UICPA) de unnilpentium ainsi adopté (Unp) comme temporaire, Dénomination systématique. Tenter de résoudre le problème, en 1994, de l'UICPA a proposé le nom joliotium (Jl), d'après le physicien français Frédéric Joliot-Curie, qui a été proposé à l'origine par l'équipe soviétique pour l'élément 102, nommé plus tard nobélium . Les deux prétendants principaux toujours en désaccord sur les noms des éléments 104-106. Cependant, en 1997, ils ont résolu le litige et ont adopté le nom actuel, dubnium (Db), après la Russie ville de Dubna, l'emplacement de la Institut unifié de recherches nucléaires. Il a été soutenu par l'IUPAC que le laboratoire Berkeley avait déjà été reconnue à plusieurs reprises dans la dénomination des éléments (ce est à dire, berkelium , californium , américium ) et que l'acceptation de la noms rutherfordium et seaborgium pour les éléments 104 et 106 devrait être compensée par la reconnaissance de la Les contributions de l'équipe de Russie à la découverte d'éléments 104, 105 et 106.
Propriétés chimiques
Propriétés extrapolées
Élément 105 devrait être le troisième membre de la série 6d de métaux de transition et l'élément le plus lourd du groupe V du tableau périodique, au-dessous de vanadium , niobium et tantale . Parce qu'il est positionnée juste en dessous de tantale, il peut également être appelé eka-tantale. Tous les membres du groupe décrivent facilement leur état de cinq d'oxydation et l'état devient plus stable que le groupe est descendu. Ainsi devrait dubnium pour former un 5 état stable. Pour ce groupe, quatre et trois États sont également connus pour les membres plus lourds et dubnium peuvent également former ces états d'oxydation réducteurs.
Dans une extrapolation des chimies de niobium et de tantale , dubnium doit réagir avec l'oxygène pour former un pentoxyde inerte, Db 2 O 5. Dans alcalin, la formation d'un complexe orthodubnate, DBO 3-
4, est attendue. La réaction avec les halogènes devrait facilement former les pentahalogénures, DBX 5. Les pentachlorures de niobium et de tantale en tant que matières solides existent molécules volatiles ou pentagonale monomères dans la phase vapeur. Ainsi, DbCl 5 devrait être un solide volatile. De même, le pentafluorure, DBF 5, devrait être encore plus volatile. L'hydrolyse des halogénures est connu pour former facilement les oxyhalogénures, 3 MOX. Ainsi, les halogénures DBX 5 devraient réagir avec l'eau pour former dBox 3. La réaction avec l'ion fluorure est également bien connu pour les homologues légers et dubnium devrait former une gamme de complexes fluorés. En particulier, la réaction du pentafluorure avec HF devrait former un hexafluorodubnate ions, DBF -
6. Excès de fluorure devrait conduire à DBF 2-
7 et DBOF 2-
5. Si les propriétés eka-tantale sont représentés, des concentrations plus élevées de fluorure devraient finalement former DBF 3-
8 depuis NbF 3-
8 ne est pas connu.
Chimie expérimentale
La chimie de dubnium a été étudié pendant plusieurs années à l'aide de gaz thermochromatography. Les expériences ont étudié les caractéristiques d'adsorption relatives des isotopes de niobium , de tantale et dubnium radio-isotopes. Les résultats ont indiqué la formation de groupe typique 5 halogénures et oxyhalogénures, à savoir DbCl 5, DbBr 5, 3 et DbOCl DbOBr 3. Les rapports sur ces premières expériences se réfèrent généralement à dubnium que hahnium.
| Formule | Noms (s) |
|---|---|
| DbCl 5 | dubnium pentachlorure; dubnium (V) de chlorure |
| DbBr 5 | dubnium pentabromure; dubnium (V) de bromure |
| DbOCl 3 | oxychlorure dubnium; dubnium (V) de trichlorure d'oxyde; dubnyl (V) chloride |
| DbOBr 3 | oxybromure dubnium; dubnium (V) de l'oxyde de tribromure; dubnyl (V) bromure |
Histoire nucléosynthèse
La fusion froide
Cette section traite de la synthèse de noyaux de dubnium par ce qu'on appelle des réactions de fusion "à froid". Ce sont des processus qui créent des noyaux composés à faible énergie d'excitation (~ 10-20 MeV, donc «à froid»), conduisant à une plus grande probabilité de survie de la fission. Le noyau excité décroît alors à l'état de sol via l'émission d'un ou deux neutrons seulement.
- 209 Bi (50 Ti, xn) 259-x Db (x = 1,2,3)
Les premières tentatives de synthétisent dubnium utilisant des réactions de fusion à froid ont été effectuées en 1976 par l'équipe de FLNR, Dubna en utilisant la réaction ci-dessus. Ils étaient capables de détecter un 5 s activité spontanée fission (SF) dont ils assignés à 257 Db. Cette mission a été corrigée par la suite à 258 Db. En 1981, l'équipe de GSI étudié cette réaction en utilisant la technique améliorée de corrélation génétique parent-fille se désintègre. Ils ont pu identifier avec certitude 258 Db, le produit de la chaîne d'évaporation 1n de neutrons. En 1983, l'équipe de Dubna revisité la réaction en utilisant la méthode d'identification d'un descendant en utilisant une séparation chimique. Ils ont réussi à mesurer les désintégrations de descendants connus de la chaîne de désintégration commençant par 258 Db alpha. Cela a été considéré comme fournissant une preuve de la formation de noyaux de dubnium. L'équipe de GSI revisité la réaction en 1985 et ont été en mesure de détecter 10 atomes de 257 Db. Après une mise à niveau importante de leurs installations en 1993, en 2000, l'équipe a mesuré 120 désintégrations de 257 Db, 16 désintégrations de 256 dB et décadence de 258 dB dans la mesure des fonctions 1n, 2n et 3n excitation. Les données recueillies pour Db 257 ont permis une première étude spectroscopique de cet isotope identifiés et un isomère, 257m Db, et une première détermination d'une structure de niveau de désintégration de 257 dB. La réaction a été utilisé dans les études spectroscopiques des isotopes de mendelevium et einsteinium en 2003-2004.
- 209 Bi (49 Ti, xn) 258-x Db (x = 2?)
Cette réaction a été étudiée par Yuri Oganessian et l'équipe de Dubna en 1983. Ils ont observé une hausse de 2,6 de l'activité SF attribué provisoirement à 256 Db. Résultats plus tard suggèrent une réaffectation possible de 256 Rf, résultant de l'~ 30% branche CE 256 Db.
- 209 Bi (48 Ti, xn) 257-x Db (x = 1?)
Cette réaction a été étudiée par Yuri Oganessian et l'équipe de Dubna en 1983. Ils observer l'activité d'un 1,6 avec une branche avec un alpha ~ 20% ~ SF branche de 80%. L'activité a été provisoirement attribué à 255 Db. Résultats plus tard suggèrent une réaffectation à 256 Db.
- 208 Pb (51 V, xn) 259-x Db (x = 1,2)
L'équipe a également étudié à Dubna cette réaction en 1976 et était à nouveau en mesure de détecter la 5 de l'activité SF, d'abord attribué provisoirement à 257 dB et plus tard à 258 Db. En 2006, l'équipe de LBNL nouvelle enquête cette réaction dans le cadre de leur programme de projectile impair Z. Ils étaient capables de détecter 258 dB et 257 dB leur mesure des 1n et 2n canaux neutrons d'évaporation.
- 207 Pb (51 V, xn) 258-x Db
L'équipe a également étudié à Dubna cette réaction en 1976, mais cette fois, ils ont été incapables de détecter la 5 S Activité SF, d'abord attribué provisoirement à 257 dB et plus tard à 258 Db. Au lieu de cela, ils ont pu mesurer un 1,5 de l'activité SF, attribué provisoirement à 255 Db.
- 205 Tl (54 Cr, xn) 259-x Db (x = 1?)
L'équipe a également étudié à Dubna cette réaction en 1976 et était à nouveau en mesure de détecter la 5 de l'activité SF, d'abord attribué provisoirement à 257 dB et plus tard à 258 Db.
Fusion chaude
Cette section traite de la synthèse de noyaux de dubnium par ce qu'on appelle des réactions de fusion "à chaud". Ce sont des processus qui créent des noyaux composés à haute énergie d'excitation (~ 40-50 MeV, donc «à chaud»), conduisant à une probabilité réduite de survie de la fission et quasi-fission. Le noyau excité décroît alors à l'état de sol via l'émission de neutrons 3-5.
- 232 Th (31 P, xn) 263-x Db (x = 5)
Il ya très peu de rapports que cette réaction rare utilisant un faisceau P-31 a été étudié en 1989 par Andreev et al. au FLNR. Une source suggère pas d'atomes ont été détectées pendant une meilleure source des russes se indique que 258 Db a été synthétisé par le canal 5n avec un rendement de 120 pb.
- 238 U (27 Al, xn) 265-x Db (x = 4,5)
En 2006, dans le cadre de leur étude sur l'utilisation de cibles d'uranium dans la synthèse des éléments super-lourds, l'équipe de LBNL dirigée par Ken Gregorich étudié les fonctions d'excitation pour les canaux de 4N et 5N dans cette nouvelle réaction.
- 236 U (27 Al, xn) 263-x Db (x = 5,6)
Cette réaction a été étudiée par Andreev et al. au FLNR, Dubna en 1992. Ils ont pu observer 258 dB et 257 dB dans la canaux de 5n et de sortie de 6n avec des rendements de 450 pb et 75 pb, respectivement.
- Am 243 (22 Ne, xn) 265-x Db (x = 5)
Les premières tentatives pour synthétiser dubnium ont été effectuées en 1968 par l'équipe du Laboratoire Flerov de réactions nucléaires (FLNR) de Dubna, en Russie. Ils ont observé deux lignes alpha dont ils affectés provisoirement à 261 dB et 260 dB. Ils ont répété leur expérience en 1970 à la recherche de fission spontanée. Ils ont trouvé un 2,2 de l'activité SF dont ils assignés à 261 Db. En 1970, l'équipe a commencé à travailler sur Dubna utilisant thermochromatography gradient afin de détecter dubnium dans des expériences chimiques comme le chlorure volatile. Dans leur première course ils ont détecté une activité SF volatile avec des propriétés d'adsorption similaires à NbCl5 et contrairement HfCl4. Ceci a été pris pour indiquer la formation de noyaux de dvi-niobium DbCl 5. En 1971, on répète l'expérience en utilisant la chimie de sensibilité plus élevée et se désintègre alpha observés à partir d'un composant DVI-niobium, pris pour confirmer la formation de 260 dB. Le procédé a été répété en 1976 en utilisant la formation de bromures et a obtenu des résultats presque identiques, ce qui indique la formation d'un volatile, dvi-niobium-5 comme DbBr.
- Am 241 (22 Ne, xn) 263-x Db (x = 4,5)
En 2000, les scientifiques chinois à l'Institut de Physique Moderne (IMP), Lanzhou, ont annoncé la découverte de l'isotope inconnue 259 Db formée dans le canal neutrons d'évaporation 4n. Ils ont également été en mesure de confirmer les propriétés de désintégration pour 258 Db.
- 248 cm (19 F, xn) 267-x Db (x = 4,5)
Cette réaction a été étudiée la première fois en 1999 à l'Institut Paul Scherrer (PSI) afin de produire 262 Db pour les études chimiques. Situé à seulement 4 atomes ont été détectés avec une section de 260 pb. Les scientifiques japonais à JAERI ont étudié la réaction ultérieure en 2002 et a déterminé les rendements de l'isotope 262 Db cours de leurs efforts pour étudier la chimie aqueuse de dubnium.
- 249 Bk (18 O, xn) 267-x Db (x = 4,5)
Suite de la découverte de 260 Db par Albert Ghiorso en 1970 à l'Université de Californie (UC), la même équipe a poursuivi en 1971 avec la découverte de la nouvelle isotope 262 Db. Ils ont également observé une activité SF 25 s non affecté, probablement associé à la branche SF maintenant connu de 263 Db. En 1990, une équipe dirigée par Kratz au LBNL définitivement découvert le nouvel isotope 263 Db dans le canal neutrons d'évaporation 4n. Cette réaction a été utilisé par la même équipe à plusieurs reprises pour tenter de confirmer une capture d'électrons (CE) filiale à 263 Db conduisant à longue durée de vie 263 Rf (voir rutherfordium ).
- 249 Bk (16 O, xn) 265-x Db (x = 4)
Suite de la découverte de 260 Db par Albert Ghiorso en 1970 à l'Université de Californie (UC), la même équipe a poursuivi en 1971 avec la découverte de la nouvelle isotope 261 Db.
- 250 Cf (15 N, xn) 265-x Db (x = 4)
Suite de la découverte de 260 Db par Ghiorso en 1970 au LBNL, la même équipe a poursuivi en 1971 avec la découverte de la nouvelle isotope 261 Db.
- 249 Cf (15 N, xn) 264-x Db (x = 4)
En 1970, l'équipe du Lawrence Berkeley National Laboratory (LBNL) a étudié cette réaction et a identifié l'isotope 260 Db dans leur expérience de découverte. Ils ont utilisé la technique moderne de corrélation génétique parent-fille se désintègre pour confirmer leur affectation. En 1977, l'équipe d'Oak Ridge a répété l'expérience et ont été en mesure de confirmer la découverte par l'identification des rayons X K de la fille lawrencium .
- Es 254 (13 C, xn) 267-x Db
En 1988, les scientifiques comme le Lawrence Livermore National Laboratory (LLNL) ont utilisé la réaction de fusion à chaud asymétrique avec un objectif einsteinium-254 pour rechercher les nouveaux nucléides 264 dB et 263 dB. En raison de la faible sensibilité de l'expérience provoquée par la petite Es-254 cible, ils étaient incapables de détecter les résidus d'évaporation (ER).
Decay de nucléides lourds
Isotopes de dubnium ont également été identifiés dans la désintégration d'éléments plus lourds. Observations à ce jour sont résumés dans le tableau ci-dessous:
| Résidu d'évaporation | Observé isotope dubnium |
|---|---|
| 294 Uus | 270 Db |
| 288 Uup | 268 Db |
| 287 Uup | 267 Db |
| 282 Uut | 266 Db |
| 267 Bh | 263 Db |
| 278 Uut, 266 Bh | 262 Db |
| 265 Bh | 261 Db |
| 272 Rg | 260 Db |
| 266 Mt, 262 Bh | 258 Db |
| 261 Bh | 257 Db |
| 260 Bh | 256 Db |
Isotopes
| Isotope | Année découvert | réaction de découverte |
|---|---|---|
| 256 Db | 1983 ?, 2000 | 209 Bi (50 Ti, 3n) |
| 257 g Db | 1985 | 209 Bi (50 Ti, 2n) |
| 257 Db m | 2000 | 209 Bi (50 Ti, 2n) |
| 258 Db | 1976 ?, 1981 | 209 Bi (50 Ti, n) |
| 259 Db | 2001 | Am 241 (22 Ne, 4n) |
| 260 Db | 1970 | 249 Cf (15 N, 4n) |
| 261 Db | 1971 | 249 Bk (16 O, 4n) |
| 262 Db | 1971 | 249 Bk (18 O, 5n) |
| 263 Db | 1971 ?, 1990 | 249 Bk (18 O, 4n) |
| 264 Db | inconnu | |
| 265 Db | inconnu | |
| 266 Db | 2006 | 237 Np (48 Ca, 3n) |
| 267 Db | 2003 | Am 243 (48 Ca, 4n) |
| 268 Db | 2003 | Am 243 (48 Ca, 3n) |
| 269 Db | inconnu | |
| 270 Db | 2009 | 249 Bk (48 Ca, 3n) |
Isomerism
- 260 Db
Des données récentes sur la désintégration de 272 Rg a révélé que certaines chaînes de désintégration continuent à 260 Db avec extraordinaires de plus longues durées de vie que prévu. Ces désintégrations ont été liés à une décomposition de niveau isomère par la désintégration alpha avec une demi-vie de ~ 19 s. Des recherches complémentaires sont nécessaires pour permettre une tâche définie.
- 258 Db
Preuve d'un état isomère de 258 Db ont été recueillies à partir de l'étude de la désintégration de 266 Mt et 262 Bh. Il a été noté que ces désintégrations affectées à une branche capture d'électrons (CE) possède une demi-vie significativement différents de ceux décomposition par émission alpha. Cela a été pris à suggérer l'existence d'un état isomère décomposition par CE avec une demi-vie de ~ 20 s. D'autres expériences sont nécessaires pour confirmer cette mission.
- 257 Db
Une étude de la formation et de la décomposition de 257 Db a prouvé l'existence d'un état isomère. Initialement, 257 Db a été prise à la pourriture par émission alpha avec des énergies 9.16,9.07 et 8,97 MeV. Une mesure de la corrélation de ces désintégrations avec ceux de 253 Lr ont montré que la décroissance de 9,16 MeV appartient à un isomère séparé. L'analyse des données en collaboration avec la théorie ont attribué cette activité à un état stable méta, 257m Db. L'état fondamental désintègre par émission alpha avec des énergies 9,07 et 8,97 MeV. Fission spontanée de 257m, g Db n'a pas été confirmée par des expériences récentes.
régimes de niveau de désintégration spectroscopiques
- 257 Db
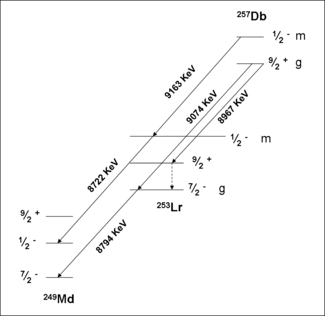
Isotopes rétractées
- 255 Db
En 1983, des scientifiques de Dubna a effectué une série d'expériences de soutien dans leur quête de la découverte de Bohrium . Dans deux de ces expériences, ils ont affirmé qu'ils avaient détecté un ~ 1,5 s activité spontanée de fission de la réaction 207 Pb (51 V, xn) et 209 Bi (48 Ti, xn). L'activité a été affectée à 255 Db. Des recherches ultérieures a suggéré que la cession devrait être modifiée pour 256 Db. En tant que tel, l'isotope 255 Db ne est actuellement pas reconnu sur la carte des radionucléides et des recherches supplémentaires sont nécessaires pour confirmer cet isotope.

