
Térbio
Informações de fundo
Crianças SOS voluntários ajudaram a escolher artigos e fez outro material currículo Patrocinar filhos ajuda as crianças no mundo em desenvolvimento para aprender também.
| Térbio | ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
65 Tb | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| Aparência | ||||||||||||||||||||||||||||
branco prateado  | ||||||||||||||||||||||||||||
| Propriedades gerais | ||||||||||||||||||||||||||||
| Nome, símbolo, número | térbio, Tb, 65 | |||||||||||||||||||||||||||
| Pronúncia | / t ɜr b Eu ə m / TUR -bee-əm | |||||||||||||||||||||||||||
| Categoria elemento | lantanídeos | |||||||||||||||||||||||||||
| Grupo, período, bloco | n / D, 6, f | |||||||||||||||||||||||||||
| Peso atômico padrão | 158,92535 | |||||||||||||||||||||||||||
| Configuração eletrônica | [ Xe ] 6s 4f 9 2 2, 8, 18, 27, 8, 2  | |||||||||||||||||||||||||||
| História | ||||||||||||||||||||||||||||
| Descoberta | Carl Gustaf Mosander (1842) | |||||||||||||||||||||||||||
| Primeiro isolamento | Carl Gustaf Mosander (1842) | |||||||||||||||||||||||||||
| Propriedades físicas | ||||||||||||||||||||||||||||
| Fase | sólido | |||||||||||||||||||||||||||
| Densidade (perto RT) | 8,23 g cm -3 · | |||||||||||||||||||||||||||
| Líquido densidade no pf | 7,65 g cm -3 · | |||||||||||||||||||||||||||
| Ponto de fusão | 1629 K , 1356 ° C, 2473 ° F | |||||||||||||||||||||||||||
| Ponto de ebulição | 3503 K, 3230 ° C, 5846 ° F | |||||||||||||||||||||||||||
| Calor de fusão | 10.15 kJ mol -1 · | |||||||||||||||||||||||||||
| Calor de vaporização | 293 kJ mol -1 · | |||||||||||||||||||||||||||
| Capacidade calorífica molar | 28,91 J · · mol -1 K -1 | |||||||||||||||||||||||||||
| Pressão de vapor | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| Propriedades atômicas | ||||||||||||||||||||||||||||
| Estados de oxidação | 4, 3, 2, 1 (Fracamente óxido de base) | |||||||||||||||||||||||||||
| Eletronegatividade | ? 1,2 (escala de Pauling) | |||||||||||||||||||||||||||
| Energias de ionização | 1º: 565,8 kJ · mol -1 | |||||||||||||||||||||||||||
| Segunda: 1110 kJ mol -1 · | ||||||||||||||||||||||||||||
| 3: 2114 kJ · mol -1 | ||||||||||||||||||||||||||||
| Raio atômico | 177 pm | |||||||||||||||||||||||||||
| O raio de covalência | 194 ± 17:00 | |||||||||||||||||||||||||||
| Miscelânea | ||||||||||||||||||||||||||||
| A estrutura de cristal | hexagonal repleto de perto | |||||||||||||||||||||||||||
| Ordenamento magnético | paramagnético a 300 K | |||||||||||||||||||||||||||
| Resistividade elétrica | ( RT) (α, poli) 1,150 μΩ · m | |||||||||||||||||||||||||||
| Condutividade térmica | 11.1 W · m -1 · K -1 | |||||||||||||||||||||||||||
| Expansão térmica | ( RT) (α, poli) 10.3 uM / (mK) | |||||||||||||||||||||||||||
| Velocidade do som (haste fina) | (20 ° C) 2.620 m · s -1 | |||||||||||||||||||||||||||
| O módulo de Young | (Forma α) 55,7 GPa | |||||||||||||||||||||||||||
| Módulo de cisalhamento | (Forma α) 22,1 GPa | |||||||||||||||||||||||||||
| Massa de módulo | (Forma α) 38,7 GPa | |||||||||||||||||||||||||||
| Rácio de Poisson | (Forma α) 0,261 | |||||||||||||||||||||||||||
| Dureza de Vickers | 863 MPa | |||||||||||||||||||||||||||
| Dureza Brinell | 677 MPa | |||||||||||||||||||||||||||
| Número de registo CAS | 7440-27-9 | |||||||||||||||||||||||||||
| A maioria dos isótopos estáveis | ||||||||||||||||||||||||||||
| Ver artigo principal: Isótopos de térbio | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
O térbio é um elemento químico com o símbolo Tb e número atômico 65. É um branco prateado terra rara de metal que é maleável, dúctil e macio o suficiente para ser cortada com uma faca. Térbio nunca é encontrado na natureza como de um elemento livre, mas ele está contido em muitos minerais , incluindo cerite, gadolinite, monazita, xenotime e euxenite.
Térbio é usado para narcótico fluoreto de cálcio, o cálcio tungstato e estrôncio molibdato, materiais que são usados em Os dispositivos de estado sólido, e como um estabilizador de cristal células de combustível que operam a temperaturas elevadas. Como um componente de Terfenol-D (uma liga que se expande e contrai quando expostos a campos magnéticos mais do que qualquer outra liga), térbio é de uso em atuadores, em naval sistemas de sonar e em sensores.
A maior parte do fornecimento de térbio do mundo é usado em fósforos verdes. Térbio óxido é em lâmpadas fluorescentes e tubos de TV. Verde Terbium fósforos são combinados com bivalente európio trivalente azuis e fósforos de európio fósforos vermelhos para fornecer "trichromatic" tecnologia de iluminação, uma luz branca de alta eficiência utilizados em iluminação padrão em iluminação interior.
Características
Propriedades físicas
O térbio é um branco prateado terra rara de metal que é maleável, dúctil e macio o suficiente para ser cortada com uma faca. É relativamente estável no ar, em comparação com outros lantanídeos. Térbio existe em duas cristal allotropes com uma temperatura de transformação de 1289 ° C entre eles.
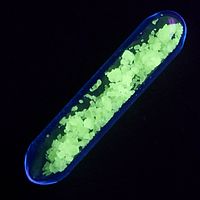
O térbio (III) cátion é brilhantemente fluorescente, uma cor amarelo-limão brilhante que é o resultado de um verde forte linha de emissão em combinação com outras linhas no laranja e vermelho. O yttrofluorite variedade do mineral fluorite deve a sua fluorescência brancas-amareladas, em parte, para térbio. Térbio facilmente oxida e, portanto, é usado na sua forma elementar especificamente para a investigação. Tb átomos individuais foram isolados por implantá-las em moléculas de fulereno.
Térbio tem um simples ordenamento ferromagnético a temperaturas inferiores a 219 K. Acima de 219 K, ele se transforma em um helicoidal antiferromagnetic estado em que todos os momentos atómicos em um determinado plano basal camada são paralelas e orientadas em um ângulo fixo para os momentos de camadas adjacentes. Este antiferromagnetismo incomum transforma em uma desordenada estado paramagnética a 230 K.
Propriedades químicas
O estado de valência mais comum de térbio é três, como em Tb 2 O 3. O estado 4 é conhecido na TBO 2 e 4 TBF. Térbio queima prontamente para formar um misto térbio (III, IV):
- 8 Tb + 7 O 2 → 2 Tb 4 O 7
Em solução, formulários de térbio apenas iões trivalentes. O térbio é bastante electropositive e reage lentamente com água fria e muito rapidamente com água quente para formar hidróxido de térbio:
- 2 Tb + 6 H 2 O → 2 Tb (OH) 3 + 3 H 2 ↑
Térbio de metal reage com todos os halogéneos, formando trialogenetos branco:
Térbio se dissolve facilmente em diluída de ácido sulfúrico para formar soluções contendo o térbio rosa pálido (III) íons, que existem como um [Tb (OH 2) 9] 3+ complexos:
- 2 Tb (s) 3 + H 2 SO 4 → 2 Tb 3+ + 3 SO 2-
4 + 3 H 2 ↑
Compostos

Térbio combina-se com azoto, carbono, enxofre, fósforo, boro, selénio, silício e arsénio a temperaturas elevadas, formando vários compostos binários, tais como TbH 2, TbH 3, TBB 2, Tb 2 S 3, TbSe, e TbTe TBN. Nesses compostos, principalmente Tb apresentam estados de oxidação três e às vezes dois. Térbio (ii) halogenetos são obtidos por emparelhamento halogenetos Tb (III) na presença de Tb em recipientes metálicos de tântalo. Térbio também forma sesquicloreto Tb 2 Cl 3, que pode ser ainda mais reduzida para TbCl por recozimento a 800 ° C. Este térbio (I) de cloreto de formulários plaquetas com estrutura de grafite-como camadas.
Outros compostos incluem
- Cloretos: TbCl 3
- Brometos: TbBr 3
- Iodetos: TBi 3
- Fluoretos: TBF 3, TBF 4
Térbio (IV) o flúor é um forte agente de fluoração, emitindo flúor atômico relativamente puro quando aquecido, em vez de a mistura de vapores de fluoreto emitidos a partir de CoF 3 ou 4 CEF.
Isótopos
Naturalmente que ocorre térbio é composto de sua única estável isótopo , térbio-159; o elemento é assim chamada mononuclidic e monoisotópico. 36 radioisótopos foram identificados, sendo o ser mais pesado térbio-171 (com massa atômica de 170,95330 (86) u) e mais leve ser térbio-135 (exata desconhecido massa). O mais estáveis radioisótopo sintético de térbio são térbio-158, com uma meia-vida de 180 anos e térbio-157, com uma meia-vida de 71 anos. Todos os restantes isótopos radioativos apresentam meias-vidas que são bem menos do que trimestre do ano, ea maioria destes com meias-vidas que são menos de meio minuto. O primário modo de decaimento antes do isótopo estável mais abundante, 159 Tb, é captura de elétrons, o que resulta na produção de gadolínio isótopos, eo primeiro modo após é decaimento beta menos, resultando em disprósio isótopos.
O elemento também tem 27 isômeros nucleares, com massas de 141-154, 156, e 158 (não todos os número de massa corresponde a apenas um isômero). A maioria deles são estáveis térbio-156m, com uma semi-vida de 24,4 horas e térbio-156m2, com uma semi-vida de 22,7 horas; isso é mais do que meias-vidas da maioria dos estados fundamentais de isótopos radioativos de térbio, com exceção apenas aqueles com números de massa 155-161.
História
Térbio foi descoberto em 1843 pelo sueco químico Carl Gustaf Mosander, que detectou como uma impureza no O óxido de ítrio, Y 2 O 3, e nomeado após a vila Ytterby na Suécia . Não foi isolado na forma pura até a recente advento de técnicas de troca iônica.
Quando Mosander primeiro particionado "yttria" em três fracções, "térbia" foi a fração que continha a cor-de-rosa (devido ao que hoje é conhecido como érbio), e "érbia" foi a fração que era essencialmente incolor em solução, mas deu um óxido castanho tingido. Trabalhadores posteriores tiveram dificuldade em observar o último, mas a fração rosa era impossível de perder. Argumentos ia e voltava para saber se "érbia" sequer existia. Na confusão, os nomes originais foi revertida, ea troca de nomes preso. Pensa-se agora que os trabalhadores que usaram o dobro de sódio ou sulfatos de potássio para remover "ceria" de "yttria" inadvertidamente perdeu o conteúdo térbio do sistema no precipitado contendo ceria. Em qualquer caso, o que é agora conhecido como térbio foi apenas cerca de 1% da ítria original, mas que foi suficiente para conferir uma cor amarelada ao óxido. Assim, térbio foi um componente menor da fração de térbio original, dominado por seus vizinhos imediatos, gadolínio e disprósio . Depois disso, sempre que outras terras raras foram separadas do esta mistura, o que deu a fração de óxido marrom manteve o nome térbio, até que finalmente foi puro. Os pesquisadores do século 19 não têm o benefício da tecnologia de fluorescência, com o qual a observar a fluorescência brilhante que teria feito este elemento muito mais fácil de controlar em misturas.
Ocorrência

Térbio nunca é encontrado na natureza, por si só, mas está contido, juntamente com outros elementos de terras raras em muitos minerais, incluindo monazita ((Ce, La, Th, Nd, Y) PO 4 com até 0,03% térbio), xenotime (YPO 4) e euxenita ((Y, Ca, Er, La, Ce, U, Th) (Nb, Ta, Ti) 2 O 6 com 1% ou mais térbio). A abundância crosta de térbio é estimado como 1,2 mg / kg.
Atualmente, as mais ricas fontes comerciais de térbio são as íon-adsorção argilas de sul da China; os concentrados com cerca de dois terços óxido de ítrio por peso têm cerca de 1% térbia. Pequenas quantidades de térbio ocorrer em bastnäsite e monazita; quando estes são processados por extracção com solvente para recuperar os lantanídeos pesados valiosos como samário - európio - gadolínio concentrado, térbio é aí recuperadas. Devido aos grandes volumes de bastnäsite transformados em relação ao das argilas de iões de adsorção, uma proporção significativa de fornecimento térbio do mundo vem de bastnäsite.
Produção
Sais minerais contendo térbio esmagadas são tratados com ácido sulfúrico concentrado quente de ácido sulfúrico para produzir sulfatos solúveis em água de terras raras. Os filtrados ácidos são parcialmente neutralizados com soda cáustica para um pH de 3-4. Tório precipita da solução como hidróxido e é removido. Depois que a solução é tratada com oxalato de amónio para converter terras raras em sua insolúvel oxalatos. Os oxalatos são convertidos em óxidos por recozimento. Os óxidos são dissolvidos em ácido nítrico que exclui um dos principais componentes, de cério, cujas óxido é insolúvel em HNO 3. O térbio é separado como um sal duplo com de nitrato de amónio por meio de cristalização.
A rotina de separação mais eficiente para térbio sal da solução de sal de terras raras é de permuta iónica. Neste processo, os iões de terras raras está sorvido sobre resina de permuta iónica adequada por permuta com hidrogénio, de amónio ou iões cúpricos presentes na resina. Os íons de terras raras são então lavados seletivamente pelo agente de complexação adequado. Tal como acontece com outras terras raras, térbio de metal é produzido pela redução do cloreto de anidro ou fluoreto de cálcio-metal. Cálcio e tântalo impurezas podem ser removidas por refusão de vácuo, a destilação, a formação de amálgama ou fusão zona.
Aplicações
Térbio é usado como um Dopante em fluoreto de cálcio, o cálcio tungstato e estrôncio molibdato, os materiais que são usados em dispositivos de estado sólido, e como um estabilizador de cristal células de combustível, que operam a temperaturas elevadas, em conjunto com ZrO 2.
Térbio também é usado em ligas e na produção de dispositivos electrónicos. Como um componente de Terfenol-D, térbio é de uso em atuadores, em naval sistemas de sonar, sensores, no Dispositivo SoundBug (a sua primeira aplicação comercial), e outros dispositivos magnetomecânicos. Terfenol-D é uma liga que se expande ou contrai na presença de um campo magnético. Ele tem a maior magnetoestricção de qualquer liga.
Térbio óxido é utilizado em verde fósforos em lâmpadas e TV a cores fluorescentes. sódio térbio borato é usado em dispositivos de estado sólido. A fluorescência brilhante permite térbio para ser utilizado como uma sonda em bioquímica, em que se assemelha um pouco de cálcio no seu comportamento. Térbio fósforos "verdes" (que apresentam fluorescência um amarelo-limão brilhante) são combinados com európio bivalente fósforos azuis e európio trivalente fósforos vermelhos para fornecer o " trichromatic "tecnologia de iluminação que é de longe o maior consumidor de abastecimento de térbio do mundo. iluminação Trichromatic fornece muito maior saída de luz para uma determinada quantidade de energia elétrica que faz iluminação incandescente.
Precauções
Tal como acontece com os outros lantanídeos , térbio compostos são de baixa toxicidade a moderada, embora a sua toxicidade não foi investigado em pormenor. Térbio não tem papel biológico conhecido.
