
Néon
Informações de fundo
Crianças SOS feita esta seleção Wikipedia ao lado de outras escolas recursos . Patrocinar crianças ajuda crianças no mundo em desenvolvimento para aprender também.
| Néon | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
10 Ne | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Aparência | |||||||||||||||||||||||||
gás incolor que exibe um brilho vermelho-alaranjado quando colocado num campo eléctrico de alta tensão  Gás de néon em um tubo de descarga, a chamada luz de néon. Linhas espectrais de neon na região visível | |||||||||||||||||||||||||
| Propriedades gerais | |||||||||||||||||||||||||
| Nome, símbolo, número | néon, Ne, 10 | ||||||||||||||||||||||||
| Pronúncia | / n Eu ɒ n / | ||||||||||||||||||||||||
| Categoria elemento | gases nobres | ||||||||||||||||||||||||
| Grupo, período, bloco | 18 (gases nobres) , 2, p | ||||||||||||||||||||||||
| Peso atômico padrão | 20,1797 (6) | ||||||||||||||||||||||||
| Configuração eletrônica | [ Ele ] 2s 2p 2 6 2, 8 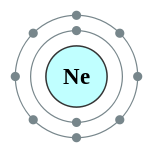 | ||||||||||||||||||||||||
| História | |||||||||||||||||||||||||
| Predição | William Ramsay (1897) | ||||||||||||||||||||||||
| Descoberta | William Ramsay & Morris Travers (1898) | ||||||||||||||||||||||||
| Primeiro isolamento | William Ramsay e Morris Travers (1898) | ||||||||||||||||||||||||
| Propriedades físicas | |||||||||||||||||||||||||
| Fase | gás | ||||||||||||||||||||||||
| Densidade | (0 ° C, 101,325 kPa) 0,9002 g / L | ||||||||||||||||||||||||
| Líquido densidade no pb | 1.207 g cm -3 · | ||||||||||||||||||||||||
| Ponto de fusão | 24,56 K , -248,59 ° C, -415,46 ° F | ||||||||||||||||||||||||
| Ponto de ebulição | 27,07 K, -246,08 ° C, -410,94 ° F | ||||||||||||||||||||||||
| Ponto Triplo | 24,5561 K (-249 ° C), 43 kPa | ||||||||||||||||||||||||
| Ponto crítico | 44,4 K, 2,76 MPa | ||||||||||||||||||||||||
| Calor de fusão | 0,335 kJ mol -1 · | ||||||||||||||||||||||||
| Calor de vaporização | 1,71 kJ mol -1 · | ||||||||||||||||||||||||
| Capacidade calorífica molar | 5 R / 2 = 20,786 J · · mol -1 K -1 | ||||||||||||||||||||||||
| Pressão de vapor | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Propriedades atômicas | |||||||||||||||||||||||||
| Estados de oxidação | 1, 0 | ||||||||||||||||||||||||
| Energias de ionização ( Mais) | 1º: 2080,7 kJ · mol -1 | ||||||||||||||||||||||||
| 2: 3952,3 kJ · mol -1 | |||||||||||||||||||||||||
| 3: 6122 kJ · mol -1 | |||||||||||||||||||||||||
| O raio de covalência | 58 pm | ||||||||||||||||||||||||
| Van der Waals raio | 154 pm | ||||||||||||||||||||||||
| Miscelânea | |||||||||||||||||||||||||
| A estrutura de cristal | cúbica de face centrada  | ||||||||||||||||||||||||
| Ordenamento magnético | diamagnetic | ||||||||||||||||||||||||
| Condutividade térmica | 49.1x10 -3 W · m -1 · K -1 | ||||||||||||||||||||||||
| Velocidade do som | (Gás, 0 ° C) 435 m · s -1 | ||||||||||||||||||||||||
| Massa de módulo | 654 GPa | ||||||||||||||||||||||||
| Número de registo CAS | 7440-01-9 | ||||||||||||||||||||||||
| A maioria dos isótopos estáveis | |||||||||||||||||||||||||
| Ver artigo principal: Isótopos de néon | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
Neon é um elemento químico com o símbolo Ne e número atômico 10. É no grupo 18 (gases nobres) da tabela periódica . Neon é um gás incolor e inodoro sob monatomic condições padrão, com cerca de dois terços a densidade do ar. Foi descoberto (juntamente com o crípton e xénon), em 1898, como um dos três elementos inertes raras residuais restantes em ar seco, depois de azoto, oxigénio, árgon e dióxido de carbono são removidos. Neon foi o segundo dos três gases raros para serem descobertos, e foi imediatamente reconhecido como um novo elemento de seu vermelho brilhante espectro de emissão. O nome de Neon é derivado das palavras gregas que significa "novo." Neon é quimicamente inerte e formas não há compostos químicos não carregados.
Durante cósmica nucleogenesis dos elementos, grandes quantidades de néon são construídas a partir do processo de captura de fusão-alfa em estrelas. Apesar de néon é um elemento muito comum no universo e do sistema solar (é quinto em abundância cósmica depois de hidrogênio, hélio, oxigênio e carbono), é muito raro na Terra. Ele constitui cerca de 18,2 ppm de ar em volume (este é quase o mesmo que a fracção molecular ou mole), e uma fracção menor da crosta. A razão para a escassez relativa de neon na Terra e os (terrestres) planetas internos, é que não há formas de néon compostos para corrigi-lo aos sólidos, e é altamente volátil, portanto, escapar do planetesimais sob o calor do Sol recém-acendeu no início do Sistema Solar. Mesmo a atmosfera de Júpiter é um pouco esgotado de neon, provavelmente por este motivo.
Neon dá uma nítida avermelhado brilho laranja quando utilizado em qualquer baixa tensão lâmpadas de brilho de néon ou de alta tensão ou tubos de descarga publicidade sinais de néon. A linha de emissão de néon vermelho também é responsável pela luz vermelha bem conhecido de lasers de hélio-neon. Néon é utilizado em algumas aplicações de tubos de refrigerante e plasma, mas tem alguns outros usos comerciais. É extraída comercialmente pela destilação fracionada do ar líquido. É consideravelmente mais caro do que o hélio, uma vez que o ar é a sua única fonte.
História

Neon (νέον grego (néon) que significa "novo") foi descoberto em 1898 pelos químicos britânico Sir William Ramsay (1852-1916) e Morris W. Travers (1872-1961) em Londres. Néon foi descoberto quando Ramsay refrigerados uma amostra de ar até que se tornou um líquido, em seguida, aqueceu-se o líquido e os gases capturados como eles fervida. A estufa de azoto , oxigénio e árgon foram identificados, mas os gases restantes foram isolados em aproximadamente a sua ordem de abundância, em um período de seis semanas, começando na extremidade de Maio de 1898. O primeiro a ser identificado foi o crípton . A seguir, depois de crípton tinha sido removida, foi um gás que deu uma luz vermelha brilhante sob descarga espectroscópica. Este gás, identificados em junho, foi nomeado neon, o análogo grego de "novum", (novo), filho o nome de Ramsay sugeriu. A característica brilhante cor vermelho-laranja que é emitida por neon gasoso quando animado eletricamente foi notado imediatamente; Travers escreveu mais tarde, "o chama de luz carmesim do tubo contou sua própria história e foi uma visão de me debruçar sobre e nunca se esqueça." Finalmente, a mesma equipa de xénon descoberto pelo mesmo processo, em Julho.
Escassez de Neon impedido a sua aplicação pronta para a iluminação ao longo das linhas de Tubos de Moore, que usou nitrogênio e que foram comercializados no início de 1900. Depois de 1902, A empresa de Georges Claude, Air Liquide, foi produzir quantidades industriais de neon como um subproduto de seu negócio de liquefacção de ar. Em dezembro 1910 Claude demonstrado moderno neon iluminação com base em um tubo selado de néon. Claude tentou brevemente para obter tubos de néon para ser usado para a iluminação interna, devido à sua intensidade, mas não conseguiu, como imóveis rejeitado fontes de luz de néon, devido à sua cor. Finalmente, em 1912, associado de Claude começou a vender tubos de descarga de néon como placas de propaganda, onde foram imediatamente mais bem sucedido como coletores de olho. Eles foram introduzidos para os EUA em 1923, quando dois grandes sinais de néon foram comprados por uma concessionária de carros Los Angeles Packard. O brilho e prendendo cor vermelho feito publicidade neon completamente diferente da concorrência.
Néon desempenhou um papel na compreensão básica da natureza dos átomos em 1913, quando JJ Thomson , como parte da sua exploração para a composição de raios canal, canalizado correntes de íons de néon através de um campo magnético e um campo elétrico e mediram seu desvio, colocando uma chapa fotográfica em seu caminho. Thomson observou duas manchas separadas de luz na chapa fotográfica (ver imagem), que sugeriu duas parábolas diferentes de deflexão. Thomson, eventualmente, concluir-se que alguns dos átomos no néon gás foram de massa mais elevado do que o resto. Apesar de não ser compreendido na época por Thomson, esta foi a primeira descoberta de isótopos de estáveis átomos. Ela foi feita usando uma versão em bruto de um instrumento agora nós denominamos como um espectrômetro de massa .
Isótopos

Neon é o segundo mais leve gás inerte. Neon tem três isótopos estáveis :. 20 Ne (90,48%), 21 Ne (0,27%) e 22 Ne (9,25%) e 21 Ne 22 Ne são parcialmente primordial e em parte nucleogenic (isto é, feita por meio de reacções nucleares de outros nuclídeos com neutrões ou outras partículas no ambiente) e suas variações em abundância natural são bem compreendidos. Em contraste, 20 Ne (o chefe isótopo primordial feita em estelar nucleosíntese) não é conhecido por ser ou nucleogenic radiogenic (salvo produção deterioração do conjunto, que é pensado para produzir apenas uma pequena quantidade). As causas da variação de 20 Ne na Terra , assim, sido muito debatido.
O diretor da escola reacções nucleares que geram néon nucleogenic isótopos começar a partir de 24 mg e 25 mg, que produzem 21 e Ne 22 Ne, respectivamente, depois captura de nêutrons e emissão imediata de um partícula alfa. Os nêutrons que produzem as reacções são na sua maioria produzidos por reações secundárias de espalação partículas alfa, por sua vez derivado de urânio série E cadeias de desintegração. O resultado líquido produz uma tendência a menor Ne 20/22 Ne e superior 21 Ne / 22 Ne proporções observadas em rochas ricas em urânio, como granitos . Néon-21 pode também ser produzida numa reacção nucleogenic, quando 20 Ne absorve um neutrão de várias fontes naturais de neutrões terrestres.
Além disso, as análises isotópicas dos terrestres expostas rochas demonstrou a cosmogênico produção (raios cósmicos), de 21 de Ne. Este isótopo é gerado pela reacções de fragmentação e desprendimento de magnésio , de sódio , de silício e de alumínio . Ao analisar as três isótopos, o componente cosmogênico pode ser resolvido a partir magmática néon e neon nucleogenic. Isto sugere que neon será uma ferramenta útil para determinar as idades de exposição cósmicos de rochas superficiais e meteoritos.
Semelhante ao xénon , néon conteúdo observada em amostras de vulcânicas gases é enriquecido em 20 Ne, bem como nucleogenic 21 Ne, em relação ao teor de 22 Ne. O conteúdo isotópico de néon destas amostras derivados do manto representa uma fonte não-atmosférica de néon. Os 20 componentes Ne-enriquecidos são atribuídos a componentes dos gases raros exóticos primordiais na Terra, possivelmente representando neon solar. 20 abundâncias elevados de NE são encontrados em diamantes , sugerindo ainda um reservatório de néon solar na Terra.
Características

Neon é o segundo mais leve gás nobre, depois de hélio . Ele brilha laranja-avermelhado em um tubo de descarga a vácuo. Além disso, néon tem a gama mais estreita de líquido de qualquer elemento: a partir de 24,55 a 27,05 K K (-248,45 ° C a -245,95 ° C, ou -415,21 ° F a -410,71 ° F). Tem mais de 40 vezes a capacidade de refrigeração de líquido hélio e três vezes maior do que o líquido de hidrogênio (em uma base por unidade de volume). Na maioria das aplicações, é um menos caro refrigerante de hélio.

Néon plasma tem a mais intensa descarga luz com tensões normais e correntes de todos os gases nobres. A cor média da luz para o olho humano é vermelho-laranja, devido a muitas linhas nesta faixa; ele também contém uma forte linha verde que está escondido, a menos que os componentes visuais são dispersas por um espectroscópio.
Dois tipos muito diferentes de iluminação de neon são de uso comum. Lâmpadas de incandescência de néon são geralmente pequenas, com mais operando a cerca de 100-250 volts . Eles têm sido largamente utilizados como poder-em indicadores e em equipamento de teste de circuito, mas diodos emissores de luz (LEDs) agora dominam em tais aplicações. Estes dispositivos de néon simples foram os precursores dos telas de plasma e telas de televisão de plasma. Sinais de néon tipicamente operar a voltagens muito mais elevadas (2-15 KV ), e os tubos luminosos são comumente metros de comprimento. O tubo de vidro é frequentemente formado em formas e letras para sinalização, bem como aplicações arquitetônicas e artísticas.
Ocorrência
Isótopos estáveis de neon são produzidos em estrelas. 20 Ne é criado na fusão de hélio e oxigênio no processo alfa, que requer temperaturas acima de 100 mega- kelvins e massas superior a 3 massas solares.
Neon é abundante em uma escala universal; é o quinto elemento mais abundante no universo químico em massa, depois de hidrogênio, hélio, oxigênio e carbono (ver elemento químico ). A sua relativa raridade na Terra, como a de hélio, é devido à sua leveza relativa, alta pressão de vapor a temperaturas muito baixas, e inércia química, todas as propriedades que tendem a mantê-lo de ficar preso nas nuvens de condensação de gás e poeira que resultou em a formação dos planetas sólidos menores e mais quentes como a Terra.
Neon é monatomic, tornando-o mais leve do que as moléculas de nitrogênio e oxigênio diatômico que formam a maior parte da atmosfera da Terra; Um balão cheio de neon vai subir no ar, embora mais lentamente do que um balão de hélio.
Abundância de massa no universo é cerca de 1 parte em 750 e na Sun e, presumivelmente, na nebulosa sistema proto-solar, cerca de 1 parte em 600. O Sonda Galileo sonda entrada na atmosfera descobriram que mesmo na alta atmosfera de Júpiter, a abundância de neon é reduzida (esgotado) por um fator de 10, para um nível de 1 parte em 6000, em massa. Isso pode indicar que mesmo o ice- planetesimais que trouxeram neon em Jupiter do sistema solar exterior, formado em uma região que estava demasiado quente para que eles têm mantido seu neon (abundâncias de gases inertes mais pesados em Júpiter são várias vezes que foram encontrados no Sol).
Neon é raro na Terra, encontrado na atmosfera da Terra em uma parte em 55.000, ou 18,2 ppm por volume (isto é aproximadamente o mesmo que a molécula ou fração molar), ou uma parte em 79.000 de ar em massa. Ele compreende uma fracção menor da crosta. É produzido industrialmente por criogénico destilação fracionada do ar liquefeito.
Aplicações

Neon é frequentemente usado em sinais e produz uma luz brilhante laranja-avermelhado inconfundível. Apesar de ainda ser referida como "néon", todas as outras cores são geradas com os outros gases nobres ou por muitas cores de iluminação fluorescente.
Néon é usado em tubos de vácuo, indicadores de alta tensão, pára-raios, tubos metros de ondas, de televisão e câmaras de ar, lasers de hélio-neon. Neon liquefeito é comercialmente utilizado como um criogênico refrigerante em aplicações que não exijam a faixa de temperatura inferior atingível com mais extremo de refrigeração hélio líquido.
Ambos gás néon e neon líquido são relativamente caros - para pequenas quantidades, o preço do néon líquido pode ser mais do que 55 vezes maior do que o hélio líquido. O driver para despesa de néon é a raridade de neon, que ao contrário de hélio, só pode ser obtido a partir do ar.
O temperatura do ponto triplo de neon (24,5561 K) é um ponto fixo de definição na Escala Internacional de Temperatura de 1990.
Compostos
Neon é o primeiro bloco de p-gás nobre. Néon é geralmente considerado como sendo inerte. Nenhum verdadeiro compostos neutros de neon são conhecidos. No entanto, os iões Ne +, (Ne Ar ) +, (Ne H ) +, e ( Ele Ne +) foram observados a partir de óptica e de espectrometria de massa estudos, e existem alguns relatórios não verificados de uma instável hidrato.

