
Mercúrio (elemento)
Você sabia ...
Crianças SOS feita esta seleção Wikipedia ao lado de outras escolas recursos . Um link rápido para o patrocínio criança é http://www.sponsor-a-child.org.uk/
| Mercúrio | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
80 Hg | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aparência | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
argênteo  Linhas espectrais de mercúrio (UV não visto) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades gerais | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nome, símbolo, número | mercúrio, Hg, 80 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pronúncia | / m ɜr k j ər Eu / MER -kyə-ree; / k w ɪ k s ɪ l v ər /; / h aɪ d r ɑr dʒ ɨ r ə m / hy- Drar -ji-rəm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Categoria elemento | de metal de transição | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo, período, bloco | 12, 6, d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Peso atômico padrão | 200,59 (2) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuração eletrônica | [ Xe ] 4f 14 5d 10 6s 2 2, 8, 18, 32, 18, 2  | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| História | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Descoberta | Chinês antigo e índios (antes 2000 aC) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades físicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase | líquido | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidade (perto RT) | 13,534 g · cm -3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto de fusão | 234.3210 K , -38,8290 ° C, -37,8922 ° F | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto de ebulição | 629,88 K, 356,73 ° C, 674,11 ° F | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto Triplo | 234.3156 K (-39 ° C), de 1,65 x 10 -7 kPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto crítico | 1,750 K, 172,00 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor de fusão | 2.29 kJ mol -1 · | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor de vaporização | 59,11 kJ · mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacidade calorífica molar | 27,983 J · · mol -1 K -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressão de vapor | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades atômicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estados de oxidação | 4, 2 (mercúrio), 1 (mercuroso) (Levemente óxido de base) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eletronegatividade | 2,00 (escala de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energias de ionização | 1º: 1007,1 kJ · mol -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2: 1810 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3: 3300 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raio atômico | 151 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| O raio de covalência | 132 ± 17:00 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals raio | 155 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscelânea | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A estrutura de cristal | rhombohedral  | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordenamento magnético | diamagnetic | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Resistividade elétrica | (25 ° C) 961nΩ · m | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Condutividade térmica | 8,30 W · m -1 · K -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Expansão térmica | (25 ° C) 60,4 uM · · K -1 m -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidade do som | (Líquido, 20 ° C) 1451.4 m · s -1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Número de registo CAS | 7439-97-6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A maioria dos isótopos estáveis | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ver artigo principal: Isótopos de mercúrio | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
O mercúrio é um elemento químico com o símbolo Hg e número atômico 80. É comumente conhecido como mercúrio e foi nomeado anteriormente hydrargyrum (do grego " "a água e" hydr- Argyros "prata). Um pesado, prateado elemento d-bloco, o mercúrio é o único metal que é líquido à condições normais de temperatura e pressão; O único outro elemento que é líquido sob estas condições é bromo , embora os metais tais como césio , gálio , e rubídio derreter apenas acima da temperatura ambiente. Com um ponto de congelação de -38,83 ° C e o ponto de ebulição de 356,73 ° C, o mercúrio tem um dos intervalos mais estreitos no seu estado líquido de qualquer metal.
O mercúrio ocorre em depósitos em todo o mundo como principalmente cinábrio ( sulfeto de mercúrio). O pigmento vermelho vermelhão, uma forma pura de sulfureto de mercúrio, é principalmente obtido por reacção de mercúrio (produzido por redução de cinnabar) com enxofre. Cinábrio é altamente tóxico por ingestão ou inalação do pó. O envenenamento por mercúrio também pode resultar da exposição a formas de mercúrio solúveis em água (tal como ou cloreto de mercúrio metilmercúrio), a inalação de vapor de mercúrio, ou comer frutos do mar contaminados com mercúrio.
O mercúrio é utilizado em termômetros, barómetros, manómetros, esfigmomanômetros, flutuar válvulas, disjuntores de mercúrio, lâmpadas fluorescentes e outros dispositivos embora preocupações sobre a toxicidade do elemento levaram a termômetros de mercúrio e esfigmomanômetros sendo em grande parte eliminados em ambientes clínicos em favor do álcool -filled, cheio de galinstan, digital, ou Os instrumentos baseados no termistor. Ele permanece em uso em aplicações de pesquisa científica e em material de amálgama para restauração dentária. É utilizada na iluminação: electricidade passada através de vapor de mercúrio de uma lâmpada fluorescente de onda curta produz luz ultravioleta que, em seguida, faz com que o fósforo no tubo de fluorescência, fazendo a luz visível.
Propriedades
Propriedades físicas

O mercúrio é um pesado, metal branco-prateado. Em comparação com outros metais, é um mau condutor de calor, mas um condutor de electricidade justo. Mercúrio tem um excepcionalmente baixo ponto de fusão e temperaturas de ebulição para um metal d-bloco. Uma explicação completa deste mergulha profundamente no reino da física quântica , mas ele pode ser resumido da seguinte forma: o mercúrio tem uma configuração eletrônica única, onde elétrons preenchem todos os disponíveis 1S, 2S, 2p, 3s, 3p, 3d, 4s, 4p , 4d, 4F, 5s, 5p, 5d e 6s subshells. Como tal configuração resiste fortemente a remoção de um elétron, o mercúrio se comporta de forma semelhante ao gás nobre elementos, que formam ligações fracas e sólidos assim que derretem facilmente. A estabilidade do reservatório 6s é devido à presença de um escudo 4f preenchido. Um shell f mal telas a carga nuclear que aumenta o atrativo interação Coulomb do shell 6s eo núcleo (ver contracção dos lantanídeos). A ausência de uma concha f interno cheio é a razão para a temperatura de fusão um pouco mais elevado de cádmio e zinco , embora ambos estes metais ainda derreter facilmente e, além disso, têm pontos de ebulição invulgarmente baixas. Por outro lado, o ouro , que é um espaço para a esquerda de mercúrio na tabela periódica, tem átomos com um electrão 6s menos do que o mercúrio. Esses elétrons são mais facilmente removidos e são compartilhados entre os átomos de ouro formando relativamente forte ligações metálicas.
Propriedades químicas
Mercúrio não reagem com a maioria dos ácidos diluídos, tais como ácido sulfúrico , embora ácidos oxidantes, tais como concentrados de ácido sulfúrico e ácido nítrico ou água régia dissolve para dar sulfato, nitrato, e os sais de cloreto. Como prata, mercúrio reage com atmosférica sulfeto de hidrogênio. Mercúrio mesmo reage com os flocos de enxofre sólido, que são utilizados em kits de derramamento de mercúrio para absorver os vapores de mercúrio (kits de derramamento também usar carvão activado e zinco em pó).
Amálgamas

Mercúrio dissolve muitos outros metais tais como ouro e prata para formar amálgamas. O ferro é uma exceção e frascos de ferro têm sido tradicionalmente utilizados para o comércio de mercúrio. Vários outros metais primeiro período de transição, com excepção de manganês , cobre e zinco estão relutantes em formar amálgamas. Outros elementos que não são facilmente formam amálgamas com mercúrio incluem platina e alguns outros metais. Amálgama de sódio é um agente redutor em comum síntese orgânica, e também é usado em lâmpadas de sódio de alta pressão.
Mercúrio prontamente combina com o alumínio para formar um amálgama de mercúrio-alumínio em que os dois metais puros entrar em contacto. Uma vez que a amálgama destrói o óxido de alumínio da camada que protege da oxidação de metal de alumínio em profundidade (como em ferro ferrugem), mesmo pequenas quantidades de mercúrio pode corroer seriamente alumínio. Por esta razão, o mercúrio não é permitido a bordo de uma aeronave, porque na maioria das circunstâncias do risco de formação de um amálgama de alumínio com partes expostas do avião.
Isótopos
Há sete estáveis isótopos de mercúrio, com 202 Hg sendo o mais abundante (29,86%). A mais longa duração radioisótopos são 194 Hg com uma meia-vida de 444 anos e 203 Hg com uma meia-vida de 46,612 dias. A maioria dos radioisótopos restantes têm meias-vidas que são menos do que um dia. 199 Hg e 201 Hg são os mais frequentemente estudados RMN-núcleos activos, tendo rotações de 1/2 e 3/2, respectivamente.
História
Mercury foi encontrado em egípcias túmulos que datam de 1500 aC.
Na China e Tibete , o uso de mercúrio foi pensado para prolongar a vida, curar fraturas, e manter a saúde geralmente boa, embora sabe-se agora que a exposição ao mercúrio leva a sérios efeitos adversos à saúde. O primeiro imperador da China, Qin Shǐ Huáng Dì - supostamente enterrado em um túmulo que continha rios de mercúrio que flui em um modelo da terra que ele governou, representante dos rios da China - foi morto por beber um mercúrio e em pó jade mistura formulada por Qin alquimistas (causando insuficiência hepática, envenenamento por mercúrio, e morte cerebral), que destina-se a dar-lhe a vida eterna.
Os antigos gregos utilizado mercúrio em pomadas; o antigos egípcios e os romanos utilizaram em cosméticos que às vezes deformadas o rosto. Em Lamanai, uma vez que uma grande cidade da civilização maia , uma piscina de mercúrio foi encontrado em um marcador em um Ballcourt mesoamericana. Em 500 aC o mercúrio foi usado para fazer amálgamas (amalgama Latina Medieval, "liga de mercúrio") com outros metais.
Alquimistas pensou em como o mercúrio Em primeiro lugar importa de que foram formados todos os metais. Eles acreditam que diferentes metais podem ser produzidos através da variação da qualidade e quantidade de enxofre contido no interior do mercúrio. A mais pura delas foi ouro, mercúrio e foi chamado para em tentativas de o transmutação de base (ou impuros) metais em ouro, que era o objetivo de muitos alquimistas.
Hg é o moderno símbolo químico para o mercúrio. Ela vem de hydrargyrum, um latinizado forma do grego palavra Ύδραργυρος (hydrargyros), que é uma palavra composta que significa "prata-água" (água hydr- =, = Argyros prata) - uma vez que é líquido, como água e brilhante como prata. O elemento foi nomeado após o deus romano Mercury, conhecido por velocidade e mobilidade. É associado com o planeta Mercúrio ; o símbolo astrológico para o planeta é também um dos símbolos alquímicos para o metal; a palavra sânscrita para a alquimia é Rasavātam que significa "o caminho de mercúrio". O mercúrio é o único metal para que o nome planetária alquímico se tornou o nome comum.
As minas em Almadén (Espanha), Monte Amiata (Itália), e Idrija (agora Slovenia) dominaram a produção de mercúrio a partir da abertura da mina de Almadén em 2500 anos atrás, até que novos depósitos foram encontrados no final do século 19.
Ocorrência
O mercúrio é um elemento extremamente raro na Terra crosta , tendo uma abundância crosta média, em massa, de apenas 0,08 partes por milhão (ppm). No entanto, uma vez que não se misturam geoquimicamente com os elementos que constituem a maioria da massa crustal, minérios de mercúrio pode ser extraordinariamente concentrado, considerando a abundância do elemento na rocha comum. Os minérios mais ricos mercúrio conter até 2,5% de mercúrio em massa, e até mesmo os mais magros depósitos concentrados são pelo menos 0,1% de mercúrio (12.000 vezes média abundância crustal). Pode ser encontrada, quer como um metal nativa (raro) ou em cinábrio, corderoite, livingstonite e outros minerais , com cinnabar (HgS) sendo o minério mais comum. Minérios de mercúrio geralmente ocorrem em muito jovem cinturões orogênicos onde a rocha de alta densidade são forçados a crosta da Terra, muitas vezes em fontes termais ou outras vulcânicas regiões.
A partir de 1558, com o invento do processo de pátio para extrair prata do minério de uso de mercúrio, o mercúrio tornou-se um recurso essencial na economia da Espanha e suas colônias americanas. Mercury foi usado para extrair prata das minas lucrativas em Nova Espanha e Peru . Inicialmente, as minas da Coroa Espanhola em Almaden no sul da Espanha forneceu todo o mercúrio para as colônias. Depósitos de mercúrio foram descobertos no Novo Mundo, e mais de 100.000 toneladas de mercúrio foram extraídos da região de Huancavelica, no Peru, ao longo de três séculos após a descoberta de depósitos de lá em 1563. O processo de pátio e mais tarde processo de fusão pan continuou a criar uma grande procura de mercúrio para o tratamento de minérios de prata até o final do século 19.

Ex-minas em Itália , o Estados Unidos e México , que uma vez produziu uma grande proporção da oferta mundial já foi completamente extraído para fora ou, no caso da Eslovénia ( Idrija) e Espanha ( Almadén), encerrado devido à queda do preço do mercúrio. Nevada de McDermitt Mine, a última mina de mercúrio nos Estados Unidos, fechou em 1992. O preço do mercúrio tem sido altamente volátil ao longo dos anos e em 2006 foi de US $ 650 por 76 libras (34,46 kg) frasco.
O mercúrio é extraído por aquecimento cinnabar numa corrente de ar e condensar o vapor. A equação para esta extração é
- HgS + O 2 → Hg + SO 2
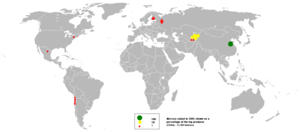
Em 2005, a China foi o maior produtor de mercúrio com quase dois terços quota global seguida de Quirguistão . Vários outros países estão acreditados para ter produção não contabilizada de mercúrio a partir de cobre electrowinning processos e pela recuperação dos efluentes.
Devido à alta toxicidade do mercúrio, tanto a mineração de cinábrio e refino de mercúrio são causas perigosas e históricos de envenenamento por mercúrio. Na China, o trabalho prisional foi utilizado por uma empresa de mineração privado como recentemente como o 1950 para criar novas minas de cinábrio mercúrio. Milhares de prisioneiros foram usados pela mineradora Luo Xi para estabelecer novos túneis. Além disso, a saúde dos trabalhadores nas minas de funcionamento é de alto risco.
A União Europeia directiva pedindo compacto lâmpadas fluorescentes a ser obrigatória em 2012 incentivou a China a reabrir as minas de cinábrio mortais para obter o mercúrio necessário para fabricação bulbo CFL. Como resultado, os perigos ambientais têm sido uma preocupação, especialmente nas cidades do sul de Foshan e Guangzhou , e no Província de Guizhou, no sudoeste.
Os locais de processamento de minas abandonadas, muitas vezes contêm mercúrio pilhas de resíduos muito perigosos de cinábrio torrado Calcines. Escoamento de água a partir de tais sites é uma fonte reconhecida de danos ecológicos. Minas de mercúrio antigos podem ser adaptados para re-uso construtivo. Por exemplo, em 1976 Santa Clara County, Califórnia comprou o histórico Almaden Quicksilver Mina e criou um parque do condado no site, após a realização de extensa segurança e análise ambiental da propriedade.
Química
Mercúrio existe em duas principais estados de oxidação, I e II. Estados de oxidação mais elevados não são importantes, mas têm sido detectados, por exemplo, mercúrio (IV) de fluoreto (HGF 4), mas apenas em condições extraordinárias.
Os compostos de mercúrio (I)
Diferente de seus vizinhos mais leves, cádmio e zinco, formas de mercúrio compostos estáveis simples com ligações metal-metal. Os mercúrio (I) são compostos diamagnetic e apresentam o cátion dimérica, Hg 2+
2. Derivados estáveis incluem o cloreto e nitrato. Tratamento de Hg (I) compostos de complexação com os ligandos fortes como o sulfeto, cianeto, etc induz a desproporcionação Hg 2+ e mercúrio elementar. Cloreto de mercúrio (i), um sólido incolor, também conhecido como calomelano, é realmente o composto com a fórmula Hg 2 Cl 2, com a conectividade Cl-Hg-Hg-Cl. É um padrão em eletroquímica. Ele reage com cloro para dar cloreto de mercúrio, o qual resiste à oxidação adicional.
Indicativa de sua tendência a relacionar a si, formas de mercúrio policatiões de mercúrio, que são constituídos por cadeias lineares de centros de mercúrio, tampado com uma carga positiva. Um exemplo é Hg 2+
3 (ASF -
6)
2.
Os compostos de mercúrio (II)
Mercúrio (II) é o estado de oxidação mais comum e é a principal delas na natureza também. Todos os quatro halogenetos de mercúrio são conhecidos. Os formulários complexos tetraédricos com outros ligantes mas os halogenetos adotar geometria de coordenação linear, um pouco como Ag + faz. O mais conhecido é mercúrio (II), cloreto, uma facilmente sublimando sólido branco. HgCl2 formas complexos de coordenação que são tipicamente tetraédrica, por exemplo, 2- HgCl
4.
De mercúrio (II) de óxido, o principal óxido de mercúrio, surge quando o metal é exposta ao ar por longos períodos a temperaturas elevadas. Ele reverte para os elementos de aquecimento em cima perto de 400 ° C, como foi demonstrado por Priestly numa síntese precoce de puro oxigênio . Hidróxidos de mercúrio são pouco caracterizados, uma vez que são por sua vizinhos ouro e prata.
Começar um metal macio, derivados formas de mercúrio muito estáveis com os Calcogênios mais pesados. Preeminente é mercúrio (II), sulfeto, HgS, que ocorre na natureza como o cinnabar minério e é o pigmento brilhante vermelhão. Como ZnS, HgS cristaliza em dois formas, forma cúbica avermelhado e preto zinco forma blende. Mercúrio (II) seleneto (HgSe) e mercúrio (II) telureto (HgTe) também são conhecidos, estes, bem como vários derivados, por exemplo, mercúrio e telureto de cádmio mercúrio telureto de zinco sendo semicondutores útil como materiais detectores infravermelhos.
Sais de mercúrio (II) formam uma variedade de derivados de complexos com amoníaco . Estas incluem bases de Millon (Hg 2N +), o polímero unidimensional (sais de HgNH +
2)
n), e "precipitado branco fusível" ou [Hg (NH3) 2] Cl 2. Conhecido como Reagente de Nessler, tetraiodomercurate de potássio (II) (2- HgI
4) ainda é ocasionalmente utilizado para testar amoníaco, devido à sua tendência para formar o sal de iodeto de profundamente colorida da base de Millon.
Fulminato de mercúrio é um detonador amplamente utilizado em explosivos.
Estados de oxidação mais elevados
Estados de oxidação acima em 2 de uma espécie não carregada são extremamente raros, embora um mercurinium cíclico (IV) de catiões, com três substituintes, podem ser um intermediário na oxymercuration reacções. Em 2007, um relatório de síntese de um (IV) composto de mercúrio, mercúrio (IV) de flúor, foi publicado. Na década de 1970, houve uma reclamação sobre a síntese de um composto de mercúrio (III), mas agora é pensado para ser falsa.
Compostos organomercuriais
Mercúrio orgânicos compostos são historicamente importantes, mas são de pouco valor industrial no mundo ocidental. Sais de mercúrio (II) são um raros exemplos de complexos de metais simples que reagem directamente com anéis aromáticos. Compostos organomercuriais são sempre bivalente e, geralmente, duas coordenadas e geometria linear. Ao contrário de compostos organocádmio e organozinco, compostos organomercuriais não reagem com a água. Eles têm geralmente a fórmula HgR 2, que muitas vezes são voláteis, ou HgRX, que são frequentemente sólidos, em que R é arilo ou alquilo e X é geralmente halogeneto ou acetato. Metilmercúrio, um termo genérico para compostos com a fórmula CH3 HGX, é perigoso uma família de compostos que muitas vezes são encontrados em poluído água. Eles surgem por um processo conhecido como biomethylation.
Aplicações

O mercúrio é utilizado principalmente para o fabrico de produtos químicos industriais, ou para aplicações eléctricas e electrónicas. Ele é utilizado em alguns termómetros, especialmente aqueles que são utilizados para medir a altas temperaturas. A quantidade continua a aumentar é usado como mercúrio gasoso em lâmpadas fluorescentes, enquanto a maioria dos outros aplicativos estão em fases lentamente devido aos regulamentos de saúde e segurança e está em algumas aplicações substituídos com menos tóxico, mas consideravelmente mais cara Galinstan liga.
Medicina
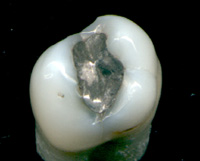

Mercúrio e seus compostos têm sido utilizados na medicina, apesar de serem muito menos comum hoje do que eram antes, agora que os efeitos tóxicos do mercúrio e seus compostos são mais amplamente compreendidas. O mercúrio é um elemento ingrediente em amálgamas dentárias. Tiomersal (chamado timerosal nos Estados Unidos) é um composto orgânico usado como um conservante em vacinas, porém este uso está em declínio. Outro composto de mercúrio Merbromin (Mercurochrome) é um anti-séptico tópico usado para pequenos cortes e arranhões ainda está em uso em alguns países.
Desde a década de 1930 alguns vacinas continham o conservante tiomersal, que é metabolizado ou degradada para acetato de mercúrio. Embora fosse amplamente especulado que este conservante à base de mercúrio pode causar ou provocar autismo em crianças, estudos científicos não mostraram nenhuma evidência apoiando qualquer link. No entanto tiomersal foi removido ou reduzido a pequenas quantidades em todas as vacinas Recomendada nos Estados Unidos para crianças de 6 anos de idade ou menos, com a excepção de vacina contra a gripe inactivada.
Mercúrio sob a forma de um dos seus minérios comuns, cinnabar, é usado em vários medicamentos tradicionais, especialmente na medicina tradicional chinesa. Avaliação da sua segurança encontrou cinábrio pode levar à intoxicação por mercúrio significativa quando aquecido, consumidos em overdose ou levado longo prazo, e pode ter efeitos adversos em doses terapêuticas, embora isso normalmente é reversível em doses terapêuticas. Embora esta forma de mercúrio parece ser menos tóxicos do que os outros, a sua utilização na medicina tradicional chinesa ainda não foi justificada como base para o uso terapêutico de cinnabar não é clara.
Hoje, o uso de mercúrio na medicina tem diminuído muito em todos os aspectos, especialmente nos países desenvolvidos. Termómetros e esfigmomanômetros com mercúrio foram inventados nos primeiros séculos 19 e 18 atrasados, respectivamente. No início do século 21, o seu uso está em declínio e foi proibido em alguns países, estados e instituições médicas. Em 2002, o Senado dos Estados Unidos aprovou legislação para eliminar progressivamente a venda de termómetros de mercúrio não sujeitos a receita. Em 2003, Washington e Maine tornaram-se os primeiros estados para proibir equipamentos de pressão arterial mercúrio. Os compostos de mercúrio são encontrados em alguns over-the-counter drogas, incluindo tópica anti-sépticos, laxantes estimulantes, fralda erupção- pomada, colírio, e sprays nasais. O FDA tem "dados insuficientes para estabelecer o reconhecimento geral da segurança e eficácia", dos ingredientes de mercúrio nesses produtos. Mercury ainda é usado em alguns diuréticos, embora já existem substitutos para a maioria dos usos terapêuticos.
Produção de cloro e soda cáustica
O cloro é produzido a partir de cloreto de sódio (sal comum, NaCl) utilizando electrólise para separar o metal de sódio a partir do gás de cloro. Normalmente, o sal é dissolvido em água para produzir uma solução salina. Os subprodutos de tais processo de cloretos alcalinos são hidrogénio (H2) e hidróxido de sódio (NaOH), o que é vulgarmente chamado de soda cáustica ou soda cáustica. De longe, o maior uso de mercúrio no final do século 20 estava em processo de célula de mercúrio (também chamado de Processo Castner-Kellner) onde sódio metálico é formado como um amálgama numa cátodo feito de mercúrio; esta sódio é então feito reagir com água para produzir hidróxido de sódio. Muitas das emissões de mercúrio industrial do século 20 veio a partir deste processo, embora as plantas modernas alegou ser segura a esse respeito. Depois de cerca de 1985, todas as novas instalações de produção de cloretos alcalinos que foram construídos nos Estados Unidos usado tanto célula de membrana ou tecnologias de célula de diafragma para produzir cloro.
Utilizações laboratoriais
Alguns termômetros médicos, especialmente aqueles para temperaturas elevadas, são preenchidos com mercúrio; no entanto, eles estão gradualmente desaparecendo. Nos Estados Unidos, a venda sem receita de termômetros de mercúrio foi banido desde 2003.
O mercúrio é também encontrado em telescópios de espelho líquido.
Alguns telescópios de trânsito usar uma bacia de mercúrio para formar um espelho plano e absolutamente horizontal, útil para determinar uma referência vertical ou perpendicular absoluta. Espelhos parabólicos horizontais côncavas podem ser formadas através da rotação de mercúrio líquido sobre um disco, a forma parabólica do líquido assim formado que reflecte e focalizar a luz incidente. Esses telescópios são mais baratos do que convencionais grandes telescópios de espelho por até um fator de 100, mas o espelho não pode ser inclinado e sempre aponta para cima.
Mercúrio líquido é uma parte de referência secundário populares eléctrodo (o chamado eléctrodo de calomelanos) em electroquímica como uma alternativa para o eléctrodo padrão de hidrogénio. O eletrodo calomel é usado para calcular o potencial de eléctrodo células meia. Por último, mas não menos importante, o ponto triplo de mercúrio, -38,8344 ° C, é um ponto fixo utilizado como um padrão de temperatura para a Escala Internacional de Temperatura ( STI-90).
Nicho usos


Mercúrio gasoso é usado em lâmpadas de vapor de mercúrio e alguns " sinal de néon "sinais tipo de publicidade e lâmpadas fluorescentes. Estas lâmpadas de baixa pressão emitem muito espectralmente linhas estreitas, que são tradicionalmente usados em espectroscopia óptica para calibração de posição espectral. Lâmpadas de calibração comerciais são vendidas para este fim; no entanto, simplesmente refletindo algumas das fluorescente lâmpada do teto luz em um espectrômetro é uma prática comum de calibração. Mercúrio gasoso também é encontrada em alguns tubos de elétrons, incluindo ignitrões, tiratrões, e retificadores de vapor de mercúrio. Ele também é usado em lâmpadas de cuidados médicos especializados para bronzeamento da pele e desinfecção (ver fotos). Mercúrio gasoso é adicionado cátodo frio argônio -filled lâmpadas para aumentar a e ionização condutividade elétrica. Uma lâmpada de argônio preenchido sem mercúrio terá manchas maçantes e vai deixar de acender corretamente. Iluminação contendo mercúrio pode ser bombardeado / forno bombeado apenas uma vez. Quando adicionado ao néon tubos cheios a luz produzida será inconsistentes vermelho / manchas azuis até que o processo de queima-in inicial é concluída; eventualmente, ele vai acender uma cor consistente maçante off-azul.
Cosméticos
Mercúrio, como tiomersal, é amplamente utilizada no fabrico de mascara. Em 2008, Minnesota se tornou o primeiro estado em os EUA para proibir mercúrio adicionado intencionalmente em cosméticos, dando-lhe um padrão mais resistente do que o governo federal.
Um estudo realizado na concentração de mercúrio na urina média geométrica identificada uma fonte não reconhecida anteriormente de exposição (produtos de cuidados da pele) para mercúrio inorgânico entre New York City residentes. Biomonitoramento de base populacional também mostrou que os níveis de concentração de mercúrio são mais elevados em consumidores de frutos do mar e peixes refeições.
Usos históricos


Muitas aplicações de histórico feito uso das propriedades físicas peculiares de mercúrio, especialmente como um líquido denso e um metal líquido:
- As quantidades de mercúrio líquido variando 90-600 gramas (3,2-21 comentários similares) foram recuperados a partir de elite Maya túmulos ou caches rituais em seis locais. Este mercúrio pode ter sido usada em taças quanto espelhos fins divinatórios. Cinco delas data do período clássico da civilização maia (c. 250-900), mas um exemplo antecedeu este.
- Em Espanha islâmica, foi utilizado para o enchimento de piscinas decorativas. Mais tarde, o artista americano Alexander Calder construiu uma fonte de mercúrio para o Pavilhão Espanhol no 1937 Exposição Mundial de Paris. A fonte está agora em exposição no Fundació Joan Miró, em Barcelona .
- Mercury foi usado dentro wobbler iscas. Sua forma pesado, líquido tornou útil, pois as iscas fez um movimento irregular atraente quando o mercúrio se moveu dentro do plugue. Esse uso foi interrompido devido a preocupações ambientais, mas a preparação ilegal de fichas de pesca modernas ocorreu.
- O As lentes de Fresnel de idade faróis usada para flutuar e girar em um banho de mercúrio, que agiu como um rolamento.
- Mercúrio esfigmomanômetros (medidores de pressão arterial), barómetros, As bombas de difusão, coulometers, e muitos outros instrumentos laboratoriais. Como um líquido opaco com uma densidade elevada e uma expansão térmica quase linear, que é ideal para esta função.
- Como um líquido condutor de electricidade, que foi utilizado em interruptores de mercúrio (incluindo interruptores de luz casa de mercúrio instaladas antes de 1970), interruptores de inclinação usados em detectores de incêndio velhos, e interruptores de inclinação em alguns termostatos domésticos.
- Devido às suas propriedades acústicas, mercúrio foi usado como meio de propagação in dispositivos de memória de linha de retardo usados em computadores digitais precoces de meados do século 20.
- Experimental turbinas a vapor de mercúrio foram instalados para aumentar a eficiência de usinas elétricas movidas a combustíveis fósseis. A usina Sul Prado em Hartford, CT empregada mercúrio como o seu fluido de trabalho, em configuração binário com um circuito de água secundário, por um número de anos a partir do final dos anos 1920, em um esforço para melhorar a eficiência da planta. Várias outras usinas foram construídas, incluindo a Estação de Schiller em Portsmouth, NH, que entrou em operação em 1950. A idéia não pegou toda a indústria devido ao peso e à toxicidade do mercúrio, bem como o advento da plantas de vapor supercrítico em anos posteriores.
- Da mesma forma, o mercúrio líquido foi usado como um refrigerante para alguns reatores nucleares; no entanto, de sódio é proposto para reactores arrefecidos com metal líquido, porque a alta densidade de mercúrio requer muito mais energia para fazer circular líquido de arrefecimento como.
- Mercury foi um propulsor para o início motores iônicos em sistemas de propulsão elétrico espaço. Vantagens eram de alto peso molecular de mercúrio, baixa energia de ionização, baixa energia dual-ionização, alta densidade do líquido e da capacidade de armazenamento líquido a temperatura ambiente. Desvantagens foram preocupações sobre o impacto ambiental associado com testes em solo e preocupações sobre a eventual arrefecimento e da condensação de alguns dos propulsor na nave espacial em operações de longa duração. O primeiro voo espacial de usar propulsão elétrica foi um propulsor de íon-abastecido mercúrio desenvolvido por NASA Lewis e voado no Teste Espaço Rocket Elétrica " SERT-1 nave espacial ", lançada pela NASA em seu Wallops Flight Facility em 1964. A SERT-1 voo foi seguido pelo vôo SERT-2 em 1970. Mercury e césio foram preferidos propulsores para motores iônicos até Laboratório de Pesquisa Hughes realizou estudos encontrando xenônio gás para ser um substituto adequado. Xénon é agora o propulsor preferido para motores de iões, uma vez que tem um elevado peso molecular, pouca ou nenhuma reactividade devido à sua gás nobre natureza, e tem uma alta densidade de armazenamento criogénico líquido sob leve.
Outras aplicações fez uso das propriedades químicas do mercúrio:
- O bateria de mercúrio é um não-recarregáveis electroquimica da bateria, uma célula primária, que era comum em toda a meados do século 20. Foi utilizado em uma ampla variedade de aplicações e estava disponível em vários tamanhos, em particular tamanhos do botão. Sua saída de tensão constante e vida útil longa deu-lhe um uso nicho para medidores de luz da câmera e aparelhos auditivos. A célula de mercúrio foi efetivamente proibida na maioria dos países da década de 1990 devido a preocupações sobre os aterros contaminantes mercúrio.
- Mercury foi usado para a preservação de madeira, desenvolvendo daguerreotypes, prateando espelhos, tintas anti-incrustantes (descontinuadas em 1990), herbicidas (descontinuadas em 1995), jogos de labirinto de mão, limpeza e dispositivos de nivelamento de estrada em carros. Os compostos de mercúrio foram utilizados em anti-sépticos, laxantes, antidepressivos, e em Antisifilíticos.
- Ele foi supostamente usado por espiões aliados para sabotar aviões da Luftwaffe: a pasta de mercúrio foi aplicada a nu de alumínio , fazendo com que o metal para rapidamente corroer ; isso causaria falhas estruturais.
- Processo alcalinos: A maior utilização industrial de mercúrio durante o século 20 foi em eletrólise para separar cloro e sódio de salmoura; mercúrio sendo o do ânodo Processo Castner-Kellner. O cloro foi usado para o branqueamento de papel (daí o local de muitas destas plantas moinhos de papel próximo) enquanto o de sódio foi usado para fazer o hidróxido de sódio para sabões e outros produtos de limpeza. Este uso tem sido largamente descontinuado, substituído com outras tecnologias que utilizam células de membrana.
- Como eléctrodos em alguns tipos de electrólise , baterias ( células de mercúrio), hidróxido de sódio e cloro de produção, jogos de mão, catalisadores , insecticidas.
- Mercury já foi usado como um cano da arma deu mais limpo.
- A partir de meados da década de 18 até meados do século 19, um processo chamado " carroting "foi usado na fabricação de chapéus de feltro. Peles de animais foram enxaguadas numa solução cor de laranja (o termo "carroting" surgiu a partir desta cor) do composto de mercúrio nitrato de mercúrio, Hg (NO 3) 2 · 2H 2 O. Este processo separou a pele da pele e emaranhado-lo juntos. Esta solução e que os vapores produzidos eram altamente tóxicos. O Estados Unidos Serviço de Saúde Pública proibiu o uso de mercúrio na indústria de feltro em dezembro de 1941. Os sintomas psicológicos associados à intoxicação por mercúrio inspirou a frase " louco como um chapeleiro ". Lewis Carroll " Mad Hatter ", em seu livro As aventuras de Alice no País das Maravilhas era um jogo de palavras com base na frase mais velho, mas o próprio personagem não apresentam sintomas de envenenamento por mercúrio.
- Mineração de ouro e prata. Historicamente, o mercúrio foi amplamente utilizado na mineração de ouro hidráulica, a fim de ajudar o ouro a afundar através da mistura de água e cascalho fluindo. Partículas finas podem formar mercúrio amálgama de mercúrio de ouro e, portanto, aumentar as taxas de recuperação de ouro. Utilização em larga escala de mercúrio parou na década de 1960. No entanto, o mercúrio é usado ainda em pequena escala, muitas vezes clandestina, prospecção de ouro. Estima-se que 45 mil toneladas métricas de mercúrio utilizado na Califórnia garimpo não foram recuperados. Mercury também foi utilizado na mineração de prata.
Usos medicinais históricos
Cloreto de mercúrio (i) (também conhecido como calomelanos ou cloreto de mercúrio) foi utilizada na medicina tradicional como um diurético, tópica desinfectante, e laxante. De mercúrio (II) cloreto de (também conhecido como cloreto de mercúrio, ou cloreto de mercúrio), uma vez foi utilizado para tratar a sífilis (juntamente com outros compostos de mercúrio), embora seja tão tóxico que, por vezes, os sintomas da sua toxicidade foram confundidos com aqueles dos sífilis era Acredita-se que tratar. É também usado como um desinfectante. massa azul, um comprimido ou xarope em que o mercúrio é o principal ingrediente, foi prescrita durante o século 19 para várias condições, incluindo prisão de ventre, depressão,-fértil e dores de dente. No início do século 20, o mercúrio foi administrada a crianças anualmente como um laxante e vermífugo, e foi usado em dentição pós para crianças. O organohalide contendo mercúrio merbromin (por vezes vendido como Mercurochrome) ainda é amplamente utilizado, mas foi proibido em alguns países, como os EUA
A toxicidade e segurança
Mercury ea maioria dos seus compostos são extremamente tóxicos e devem ser manuseados com cuidado; em casos de derrames que envolvem mercúrio (tal como de certas termômetros ou lâmpadas fluorescentes), procedimentos de limpeza específicos são usados para evitar a exposição e conter o derramamento. Protocolos chamar para mesclar fisicamente gotas menores em superfícies duras, combinando-os em um único pool maior para a remoção mais fácil com um conta-gotas, ou para empurrar delicadamente o vazamento em um recipiente descartável. Aspiradores de vassouras e causar maior dispersão do mercúrio e não devem ser usados. Depois, multa de enxofre , zinco , ou algum outro pó que prontamente forma uma amálgama (liga) com mercúrio a temperaturas normais é aspergido sobre a área antes de si mesmo sendo coletados e descartados de maneira adequada. Limpeza de superfícies porosas e roupas não é eficaz na remoção de todos os vestígios de mercúrio e, portanto, é aconselhável descartar esses tipos de itens deveriam ser expostas a um vazamento de mercúrio.
O mercúrio pode ser absorvida através da pele e das membranas mucosas e vapores de mercúrio pode ser inalada, assim recipientes de mercúrio são firmemente selado para evitar derramamentos e evaporação. Aquecimento de mercúrio, ou de compostos de mercúrio que pode se decompor quando aquecidos, é sempre realizada com ventilação adequada, a fim de evitar a exposição ao vapor de mercúrio. As formas mais tóxicos do mercúrio são seus compostos orgânicos , tais como dimethylmercury e metilmercúrio. Compostos inorgânicos, tais como cinnabar também são altamente tóxico por ingestão ou inalação. O mercúrio pode causar tanto intoxicação crônica e aguda.
Lançamentos no ambiente
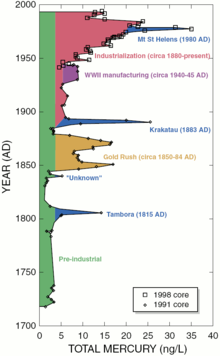
Taxas de deposição pré-industrial de mercúrio da atmosfera pode ser de cerca de 4 ng / (1 L de depósito de gelo). Apesar de que pode ser considerado um nível natural de exposição, fontes regionais ou globais têm efeitos significativos. As erupções vulcânicas pode aumentar a fonte atmosférica por 4-6 vezes.
Fontes naturais, como vulcões , são responsáveis por cerca de metade das emissões de mercúrio na atmosfera. A semi-humana gerado pode ser dividido nas seguintes percentagens estimadas:
- 65% a partir de combustão estacionária, dos quais usinas de energia movidas a carvão são a maior fonte de agregados (40% das emissões de mercúrio dos EUA em 1999). Isso inclui usinas de energia alimentado a gás, onde o mercúrio não foi removido. Emissões provenientes da queima de carvão são entre uma e duas ordens de magnitude maior do que as emissões provenientes da queima de óleo, dependendo do país.
- 11% da produção de ouro. Os três maiores fontes pontuais para as emissões de mercúrio em os EUA são os três maiores minas de ouro. Hidrogeoquímico liberação de mercúrio a partir de rejeitos de minas de ouro foi contabilizada como uma fonte significativa de mercúrio atmosférico no leste do Canadá.
- 6,8% deprodução de metais não-ferrosos, tipicamentefundições.
- 6,4% deprodução de cimento.
- 3,0% de eliminação de resíduos , incluindo municipal e resíduos perigosos, crematórios, eincineração de lamas de depuração.
- 3,0% desoda cáusticaa produção.
- 1,4% deferro-gusa eaçoprodução.
- 1,1% da produção de mercúrio, principalmente para as baterias.
- 2,0% a partir de outras fontes.
As percentagens acima são estimativas das emissões de mercúrio causadas pelo homem globais em 2000, excluindo a queima de biomassa, uma fonte importante em algumas regiões.
Contaminação por mercúrio atmosférico recente no ar urbano ao ar livre foi medido em 0,01-0,02 g / m 3 . Um estudo mediu 2.001 níveis de mercúrio em 12 locais interiores escolhidos para representar uma secção transversal de construção de tipos, locais e idades na área de Nova Iorque. Este estudo encontrou concentrações de mercúrio significativamente elevados sobre as concentrações ao ar livre, na faixa de 0,0065-0,523 ug / m 3 . A média foi de 0,069 ng / m 3 .
Mercury também entra no ambiente através da eliminação inadequada (por exemplo, aterros, incineração) de certos produtos. Os produtos que contêm mercúrio incluem: autopeças, pilhas, lâmpadas fluorescentes, produtos médicos, termômetros e termostatos. Devido a preocupações com a saúde (ver abaixo), tóxicos usar redução esforços estão a cortar ou eliminar o mercúrio nesses produtos. Por exemplo, a quantidade de mercúrio vendidos em termostatos nos Estados Unidos diminuiu de 14,5 toneladas em 2004 para 3,9 t em 2007. A maioria dos termômetros agora usar pigmentada álcool em vez de mercúrio, e termômetros liga galinstan também são uma opção. Os termómetros de mercúrio ainda são usados ocasionalmente no campo da medicina, porque eles são mais precisos do que os termômetros de álcool, embora ambos são comumente sendo substituído por termômetros eletrônicos e menos comumente por termômetros galinstan. Os termómetros de mercúrio ainda são amplamente utilizados para certas aplicações científicas devido à sua maior precisão e escala de trabalho.
Historicamente, um dos maiores lançamentos a partir da planta foi Colex, uma unidade de separação de lítio-isótopo em Oak Ridge, Tennessee. A usina operada na década de 1950 e 1960. Os registros são incompletos e imprecisos, mas as comissões governamentais estimaram que cerca de dois milhões de libras de mercúrio estão desaparecidos.
Um grave desastre industrial foi o despejo de compostos de mercúrio em Minamata Bay, Japão. Estima-se que mais de 3.000 pessoas sofreram várias deformidades, sintomas de envenenamento de mercúrio graves ou morte por que ficou conhecido como a doença de Minamata.
Exposição ocupacional
Devido aos efeitos na saúde da exposição ao mercúrio, utilizações industriais e comerciais são regulamentados em muitos países. A Organização Mundial de Saúde , OSHA, e NIOSH todos tratar o mercúrio como um risco ocupacional, e estabeleceram limites específicos de exposição ocupacional. Derramamento e descarte de mercúrio ambientais são regulamentadas em os EUA, principalmente, pela United States Environmental Protection Agency.
Estudos caso-controle têm demonstrado efeitos como tremores, danificado habilidades cognitivas e distúrbios do sono em trabalhadores com exposição crônica ao vapor de mercúrio, mesmo em baixas concentrações na gama 0,7-42 ug / m 3 . Um estudo demonstrou que a exposição aguda (4-8 horas) para os níveis de mercúrio elementar calculada de 1,1 a 44 mg / m 3 resultou em dor no peito, dispnéia, tosse, hemoptise, comprometimento da função pulmonar e evidência de intersticial pneumonite. A exposição aguda ao vapor de mercúrio foi mostrado resultar em efeitos centrais profundos do sistema nervoso, incluindo reacções psicóticas caracterizado por delírios, alucinações, e tendência suicida. A exposição ocupacional resultou em grande alcance perturbação funcional, incluindo erethism, irritabilidade, excitabilidade, timidez excessiva, e insônia. Com a exposição continuada, um tremor fino desenvolve e pode escalar para espasmos musculares violentos. Tremor inicialmente envolve as mãos e depois se espalha para o pálpebras, lábios e língua. A longo prazo, a exposição de nível baixo tem sido associada com sintomas mais subtis de erethism, incluindo fadiga, irritabilidade, perda de memória, sonhos vívidos e depressão.
Tratamento
A investigação sobre o tratamento de envenenamento com mercúrio é limitada. Actualmente as drogas disponíveis para o envenenamento agudo mercurial quelantes incluem N-acetil-D, L- penicilamina (NAP), britânica Anti-Lewisite (BAL), ácido 2,3-dimercapto-1-propanossulfónico (DMPS), e ácido dimercaptossuccínico (DMSA) . Em um pequeno estudo, incluindo 11 trabalhadores da construção expostos ao mercúrio elementar, os pacientes foram tratados com DMSA e NAP. A terapia de quelação com ambas as drogas resultou na mobilização de uma pequena fração do corpo mercúrio total estimado. DMSA era capaz de aumentar a excreção de mercúrio a uma extensão maior do que a NAP.
Peixe
Peixes e mariscos têm uma tendência natural para se concentrar mercúrio em seus corpos, muitas vezes na forma de metilmercúrio, um composto orgânico altamente tóxico do mercúrio. Espécies de peixes que estão no topo da cadeia alimentar, como o tubarão , peixe-espada, cavala, atum rabilho, atum-voador, e tilefish conter maiores concentrações de mercúrio do que outros. Como o mercúrio eo metilmercúrio são lipossolúveis, eles acumulam principalmente na vísceras, embora eles também são encontrados em todo o tecido muscular. Quando esse peixe é consumido por um predador, o nível de mercúrio é acumulado. Dado que os peixes são menos eficientes em depurating do que acumular o metilmercúrio, as concentrações de tecido de peixe aumentar ao longo do tempo. Assim, espécies que estão no topo da cadeia alimentar acumular carga corporal de mercúrio que pode ser dez vezes mais elevadas do que as espécies que consomem. Este processo é chamado biomagnificação. O envenenamento por mercúrio aconteceu desta forma, em Minamata, Japão , agora chamado de doença de Minamata.
Regulamentos
Internacional
140 países concordaram com a Convenção de Minamata pelo Programa das Nações Unidas para o Ambiente (UNEP) para evitar emissões. Convenção deverá ser aberta à assinatura em outubro de 2013.
Estados Unidos
Nos Estados Unidos, o Agência de Proteção Ambiental está encarregada de regular e gerir a contaminação por mercúrio. Várias leis dão a EPA esta autoridade, incluindo a Lei do Ar Limpo, a Lei da Água Limpa, a Conservação dos Recursos e Lei de Recuperação, eo Seguro Lei da Água de beber. Além disso, o contendo mercúrio e bateria recarregável Battery Management Act, aprovada em 1996, prevê a redução progressiva da utilização de mercúrio nas pilhas, e prevê a eliminação eficiente e eficaz em termos de custos de vários tipos de baterias usadas. América do Norte contribuiu com aproximadamente 11% do total das emissões antropogénicas de mercúrio globais em 1995.
Os Estados Unidos Clean Air Act, aprovada em 1990, colocou mercúrio em uma lista de poluentes tóxicos que precisam ser controlados, na medida do possível. Assim, as indústrias que liberam altas concentrações de mercúrio no ambiente concordaram em instalar tecnologias de controle de operação máxima (MACT). Em março de 2005, a EPA promulgou um regulamento que acrescentou usinas para a lista de fontes que devem ser controlados e instituiu um nacional cap and trade sistema. Unidos foram dados até novembro de 2006 para impor controlos mais rigorosos, mas depois de uma entrada legal de vários estados, os regulamentos foram atingido por um tribunal federal de apelações em 8 de fevereiro de 2008. A regra foi considerada insuficiente para proteger a saúde das pessoas que vivem perto usinas de energia movidas a carvão, devido aos efeitos negativos documentados no relatório do estudo EPA para o Congresso de 1998.
A EPA anunciou novas regras para usinas de energia movidas a carvão, em 22 de dezembro de 2011. Os fornos de cimento que queimam resíduos perigosos são realizadas para um padrão mais flexível do que são padrãode resíduos perigososincineradores nos Estados Unidos, e como resultado, são uma fonte desproporcional de mercúrio poluição.
União Europeia
Na União Europeia , a directiva relativa à restrição do uso de certas substâncias perigosas em equipamentos eléctricos e electrónicos (ver RoHS) proíbe o mercúrio a partir de certos produtos eléctricos e electrónicos, e limita a quantidade de mercúrio em outros produtos para menos de 1.000 ppm. Há restrições para concentração de mercúrio em embalagens (o limite é de 100 ppm para quantia de mercúrio, chumbo , crómio hexavalente e cádmio ) e baterias (o limite é de 5 ppm). Em julho de 2007, a União Europeia também proibiu mercúrio em instrumentos de medição não eléctricos, tais como termômetros e barômetros. A proibição aplica-se apenas aos novos dispositivos, e contém isenções para o sector dos cuidados de saúde e um período de carência de dois anos para os fabricantes de barómetros.
Noruega
Noruega decretou uma proibição total da utilização de mercúrio na fabricação e importação / exportação de produtos com mercúrio, a partir de 1º de janeiro de 2008. Em 2002, vários lagos na Noruega foram encontrados para ter um mau estado de poluição por mercúrio, com um excesso de 1 ng / g de mercúrio no sedimento. Em 2008, o ministro do Ambiente de Desenvolvimento, Erik Solheim, da Noruega, disse: "Mercury está entre as toxinas ambientais mais perigosos. Alternativas satisfatórias para Hg em produtos estão disponíveis, e é, portanto, cabendo a induzir uma proibição ".
Suécia
Mercury foi proibida na Suécia em 2009.
Dinamarca
Em 2008, a Dinamarca também proibiu amálgama de mercúrio dental.
