
Arsênico
Fundo para as escolas Wikipédia
Crianças SOS oferecem um download completo desta seleção para as escolas para uso em escolas intranets. Com SOS Children você pode escolher para patrocinar crianças em mais de cem países
| Arsênico | |||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
33 Como | |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| Aparência | |||||||||||||||||||||||||||||||||||||
cinza metálico  | |||||||||||||||||||||||||||||||||||||
| Propriedades gerais | |||||||||||||||||||||||||||||||||||||
| Nome, símbolo, número | arsênico, As, 33 | ||||||||||||||||||||||||||||||||||||
| Pronúncia | / ɑr s ɨ n ɪ k / AR -sə-nik, também / ɑr s ɛ n ɪ k / ar- SEN -ik quando atributivo | ||||||||||||||||||||||||||||||||||||
| Categoria Metallic | metalóide | ||||||||||||||||||||||||||||||||||||
| Grupo, período, bloco | 15 (pnictogens), 4, p | ||||||||||||||||||||||||||||||||||||
| Peso atômico padrão | 74,92160 (2) | ||||||||||||||||||||||||||||||||||||
| Configuração eletrônica | [ Ar ] 4s 2 3d 10 4p 3 2, 8, 18, 5  | ||||||||||||||||||||||||||||||||||||
| História | |||||||||||||||||||||||||||||||||||||
| Descoberta | Cedo Idade do Bronze ( 2500 aC) | ||||||||||||||||||||||||||||||||||||
| Primeiro isolamento | Albertus Magnus (1250) | ||||||||||||||||||||||||||||||||||||
| Propriedades físicas | |||||||||||||||||||||||||||||||||||||
| Fase | sólido | ||||||||||||||||||||||||||||||||||||
| Densidade (perto RT) | 5,727 g · cm -3 | ||||||||||||||||||||||||||||||||||||
| Líquido densidade no pf | 5,22 g cm -3 · | ||||||||||||||||||||||||||||||||||||
| Ponto de sublimação | 887 K, 615 ° C, 1137 ° F | ||||||||||||||||||||||||||||||||||||
| Ponto Triplo | 1090 K (817 ° C), 3628 kPa | ||||||||||||||||||||||||||||||||||||
| Ponto crítico | 1,673 K,? MPa | ||||||||||||||||||||||||||||||||||||
| Calor de fusão | (Cinzento) 24,44 kJ mol -1 · | ||||||||||||||||||||||||||||||||||||
| Calor de vaporização | ? 34,76 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||
| Capacidade calorífica molar | 24,64 J · · mol -1 K -1 | ||||||||||||||||||||||||||||||||||||
| Pressão de vapor | |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| Propriedades atômicas | |||||||||||||||||||||||||||||||||||||
| Estados de oxidação | 5, 3, 2, 1, -3 (Moderadamente ácida óxido) | ||||||||||||||||||||||||||||||||||||
| Eletronegatividade | 2,18 (escala de Pauling) | ||||||||||||||||||||||||||||||||||||
| Energias de ionização ( Mais) | 1º: 947,0 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||
| 2: 1798 kJ · mol -1 | |||||||||||||||||||||||||||||||||||||
| 3: 2735 kJ · mol -1 | |||||||||||||||||||||||||||||||||||||
| Raio atômico | 119 pm | ||||||||||||||||||||||||||||||||||||
| O raio de covalência | 119 ± 16:00 | ||||||||||||||||||||||||||||||||||||
| Van der Waals raio | 185 pm | ||||||||||||||||||||||||||||||||||||
| Miscelânea | |||||||||||||||||||||||||||||||||||||
| A estrutura de cristal | trigonal simples  | ||||||||||||||||||||||||||||||||||||
| Ordenamento magnético | diamagnetic | ||||||||||||||||||||||||||||||||||||
| Resistividade elétrica | (20 ° C) 333 Nco · m | ||||||||||||||||||||||||||||||||||||
| Condutividade térmica | 50,2 W · m -1 · K -1 | ||||||||||||||||||||||||||||||||||||
| O módulo de Young | 8 GPa | ||||||||||||||||||||||||||||||||||||
| Massa de módulo | 22 GPa | ||||||||||||||||||||||||||||||||||||
| Dureza de Mohs | 3,5 | ||||||||||||||||||||||||||||||||||||
| Dureza Brinell | 1440 MPa | ||||||||||||||||||||||||||||||||||||
| Número de registo CAS | 7440-38-2 | ||||||||||||||||||||||||||||||||||||
| A maioria dos isótopos estáveis | |||||||||||||||||||||||||||||||||||||
| Ver artigo principal: Isótopos de arsénio | |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
O arsênico é um elemento químico com o símbolo de como e número atômico 33. Arsénio ocorre em muitos minerais, geralmente em conjugação com o enxofre e os metais, e também como um cristal puro elementar. Ele foi documentada pela primeira vez por Albertus Magnus em 1250. O arsênico é um metalóide. Pode existir em várias formas alotrópicas , embora apenas a forma cinza tem utilização importante na indústria.
A principal utilização de arsénico metálico é para reforçar as ligas de cobre e especialmente chumbo (por exemplo, em baterias de carro). O arsênico é um tipo comum n dopante em semicondutores dispositivos eletrônicos, ea composto optoeletrônicos arseneto de gálio é o semicondutor mais comum em uso depois de silício dopado. Arsénio e seus compostos, especialmente o trióxido, são utilizadas na produção de pesticidas, produtos de madeira tratada, herbicidas, e insecticidas. Estas aplicações estão em declínio, no entanto.
O arsênico é notoriamente venenoso para a vida multicelular, embora algumas espécies de bactérias são capazes de usar compostos de arsénio como metabolitos respiratórias. A contaminação por arsênico das águas subterrâneas é um problema que afeta milhões de pessoas em todo o mundo.
Características
Características físicas
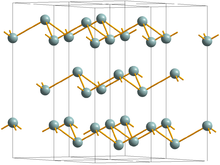
Os três arsênico mais comuns allotropes são arsênico cinza, amarelo e preto metálico, com ser cinza a cinza arsênico mais comum. (α-As, grupo espacial R 3 m No. 166) adota uma estrutura de camada dupla que consiste em muitos babados anéis de seis membros entrelaçados. Devido a fraca ligação entre as camadas, arsénio cinza é frágil e tem uma relativamente baixa dureza de Mohs de 3,5. Mais próximo e-mais próximos vizinhos próximos formar um complexo octaédrico distorcido, com três átomos no mesmo sendo um pouco mais perto do que os três átomos no próximo dupla camada. Esta embalagem relativamente estreita conduz a uma elevada densidade de 5,73 g / cm 3. Arsênico Gray é um semimetal, mas torna-se um semicondutor com um bandgap de 1,2-1,4 eV se amorphized. arsênico Amarelo é macio e ceroso e um pouco semelhante ao tetraphosphorus (P 4). Ambos têm quatro átomos dispostos num tetraédrica estrutura em que cada átomo está ligado a cada um dos outros três átomos por uma ligação simples. Este alótropo instável, sendo molecular, é o mais volátil, menos densa e mais tóxicos. Arsênico amarelo sólido é produzido por arrefecimento rápido de vapor de arsênico, como 4. É rapidamente transformado no arsênico cinza pela luz. A forma amarela tem uma densidade de 1,97 g / cm 3. Preto arsénio é semelhante em estrutura aos fósforo vermelho.
Isótopos
Naturalmente que ocorre arsênico é composto por um estável isótopo , 75 como. A partir de 2003, pelo menos 33 radioisótopos também foram sintetizados, que varia em massa atómica de 60 a 92. A maior parte destes é estável 73 Tal como acontece com uma semi-vida de 80,3 dias. Isótopos que são mais leves do que os 75 estáveis Como tendem a decair por β + decaimento, e aqueles que são mais pesadas tendem a deterioração pela β - decadência, com algumas exceções.
Pelo menos 10 isómeros nucleares foram descritos, que variam em massa atómica de 66 a 84. O mais estável de isómeros de arsénio é 68m Tal como acontece com uma semi-vida de 111 segundos.
Química
Quando aquecido no ar, arsênico oxida para trióxido de arsênio; os vapores de esta reação tem um odor semelhante a alho . Este odor pode ser detectado em minerais tais como o arsenieto de marcantes arsenopyrite com um martelo. Arsénio (e alguns compostos de arsénio) sublima por aquecimento à pressão atmosférica, convertendo directamente para um estado gasoso sem uma intervenção no estado líquido 887 K (614 ° C). O ponto triplo é de 3,63 MPa e 1090 K (820 ° C). Marcas de arsénio ácido arsénico com concentrado de ácido nítrico , ácido arsenioso com ácido nítrico diluído, e trióxido de arsénico com concentrado ácido sulfúrico .

Compostos
Os compostos de arsénio, em alguns aspectos se assemelham àqueles de fósforo , que ocupa o mesmo grupo (coluna) da tabela periódica . O arsênico é menos comumente observada no estado pentavalente, no entanto. Os mais comuns estados de oxidação para o arsénio são: -3 na arsenietos, tais como compostos intermetálicos de liga-like; e 3 no arsenitos arseniatos, (III), e compostos mais organoarsenic. O arsênico também liga facilmente a si mesmo como visto na praça como 3-
4 íons no mineral skutterudite. No estado de oxidação +3, o arsénio é geralmente piramidal, devido à influência do par solitário de elétrons .
Inorgânico
Formas de arsénio incolor, inodoro, óxidos cristalinos As 2 O 3 (" arsênico branco ") e As 2 O 5, o que está higroscópico e facilmente solúvel em água para formar soluções ácidas. Arsénio ácido (V) é um ácido fraco. Seus sais são chamados arseniatos, que é a base de contaminação por arsênico das águas subterrâneas, um problema que afeta muitas pessoas. Arsenatos sintéticos incluem Paris Green (cobre (II) acetoarsenito), arsenato de cálcio, e arseniato de hidrogênio chumbo. Os três últimos têm sido usados como agrícola insecticidas e venenos .
Os passos de protonação entre o arseniato e ácido arsénico são semelhantes às que existem entre fosfato e ácido fosfórico . Ao contrário ácido de fósforo, ácido arsenoso é verdadeiramente tribásico, com a fórmula por (OH) 3.
Uma ampla variedade de compostos de enxofre de arsénio são conhecidos. Orpiment ( As 2 S 3) e rosalgar ( Como 4 S 4) são um pouco abundantes e foram anteriormente utilizados como pigmentos de pintura. Em Como 4 S 10, arsênico tem um estado de oxidação formal de +2 em As 4 S 4, que conta com As-Como as pontes de modo que o total de covalencia Como ainda é três.
O trifluoreto, o tricloreto, tribrometo de boro, e triiodeto de arsénio (III) são bem conhecidos, ao passo que apenas Pentafluoride arsênico (ASF 5) é o único penta importante. Mais uma vez refletindo a menor estabilidade do 5+ estado de oxidação, o pentacloreto só é estável abaixo de -50 ° C.
Compostos Organoarsenic
Uma grande variedade de compostos organoarsenic são conhecidos. Vários foram desenvolvidos como agentes de guerra química durante a Primeira Guerra Mundial, incluindo vesicantes, como agentes lewisite e vômitos, tais como adamsite. Ácido cacodílico, que é de interesse histórico e prático, surge a partir da metilação de trióxido de arsênico, uma reação que não tem analogia em química de fósforo.
Alloys
O arsénio é utilizado como o elemento do grupo 5 no Semicondutores III-V arsenieto de gálio, arsenieto de índio, e arsenieto de alumínio. A contagem de electrões de valência de GaAs é o mesmo que um par de átomos de Si, mas o estrutura de banda é completamente diferente, o que resulta em massa propriedades distintas. Outras ligas de arsénio incluem o semicondutores II-IV arsenieto de cádmio.
Ocorrência e produção

Minerals com a massa fórmula e MAs 2 (M = Fe, Ni, Co) são as fontes comerciais dominantes de arsénio, em conjunto com realgar (um mineral de sulfureto de arsénio) e arsênico nativa. Um mineral é ilustrativo arsenopirita ( Fe Como S ), que está estruturalmente relacionada com a pirite de ferro . Muitos menores como contendo minerais são conhecidos. Arsénio também ocorre em várias formas orgânicas no ambiente. Arsênico inorgânico e seus compostos, ao entrar no cadeia alimentar, são progressivamente metabolizado em uma forma menos tóxica do arsênico através de um processo de metilação.
Outras vias que ocorrem naturalmente de exposição incluem cinzas vulcânicas, intemperismo de minerais e minérios contendo arsênico, e dissolvido em água subterrânea. Ela também é encontrada em alimentos, água, solo e ar. O arsênico é absorvido por todas as plantas, mas é mais concentrada em vegetais de folhas, arroz, suco de maçã e de uva e frutos do mar. Uma via adicional de exposição é através da inalação.

Em 2005, a China foi o maior produtor de arsênico branco com quase 50% de participação mundial, seguido pelo Chile, Peru e Marrocos, de acordo com o Britânico Geological Survey eo United States Geological Survey. A maioria das operações em os EUA ea Europa têm fechado por razões ambientais. O arsénio é recuperado principalmente como um produto secundário a partir da purificação de cobre. O arsênico é parte da poeira fundição de cobre, ouro, chumbo e fundições.
Em assar no ar de arsenopirite, sublima de arsénio como óxido de arsénio (III), deixando os óxidos de ferro, enquanto torrefacção sem ar resulta na produção de arsénico metálico. A purificação adicional a partir de enxofre e outros Calcogênios é conseguido através sublimação em vácuo ou numa atmosfera de hidrogénio ou por meio de destilação a partir de mistura de chumbo-arsénio fundido.
História


A palavra arsênico foi emprestado do Palavra siríaca ܠܐ ܙܐܦܢܝܐ (al) eo zarniqa Palavra persa زرنيخ Zarnikh, que significa "amarelo orpiment ", em grego como arsenikon (Αρσενικόν). Ele também está relacionado com os Arsenikos palavra grega semelhantes (Αρσενικός), que significa "masculino" ou "potente". A palavra foi adotada em Arsenicum Latina e arsênico francês velho, do que o Inglês arsênico palavra é derivada. sulfetos de arsênio (orpiment, realgar) e óxidos de ter sido conhecida e utilizada desde os tempos antigos. Zósimo (cerca de 300 AD) descreve sandarach torrefação (realgar) para obter nuvem de arsénio ( óxido arsenioso), que, em seguida, reduz a metálico arsênico. Como os sintomas de envenenamento por arsênico foram um pouco mal definido, foi frequentemente utilizada para assassinato, até o advento da Teste Marsh, uma análise química sensível para a sua presença. (Outro teste menos sensível, mas mais geral é a Teste Reinsch.) Devido à sua utilização pela classe dominante para matar um ao outro e sua potência e discrição, o arsênico foi chamado o veneno dos reis eo rei de Venenos.
Durante a Idade do Bronze , o arsênico foi muitas vezes incluídas na bronze, o que tornou a liga mais dura (o chamado " bronze arsenical "). Albertus Magnus (Alberto Magno, 1193-1280) se acredita ter sido o primeiro a isolar o elemento de um composto em 1250, pelo sabão de aquecimento juntamente com trisulfide arsênico. Em 1649, Johann Schröder publicou duas maneiras de preparar arsênico. Cristais de elemental arsênico (nativo) são encontrados na natureza, embora rara.
De Cadet fumegante líquido (impuro cacodilo), muitas vezes reivindicadas como o primeiro sintético composto organometálico, foi sintetizado em 1760 pela Louis Claude Cadet de Gassicourt pela reacção de acetato de potássio com trióxido de arsênico.
No Era vitoriana, "arsênico" ("arsênico branco" ou trióxido de arsénico) foi misturado com vinagre e giz e comido por mulheres para melhorar a tez de seus rostos, tornando a sua pele mais pálida para mostrar que eles não trabalhar nos campos. O arsênico também foi esfregado os rostos e braços de mulheres para "melhorar a sua aparência". O uso acidental de arsénio na adulteração de produtos alimentares levaram a a doce intoxicação Bradford em 1858, o que resultou em cerca de 20 mortes.
Aplicações
Agrícola

A toxicidade do arsénico para insetos , bactérias e fungos levou à sua utilização como um conservante de madeira. Na década de 1950 um processo de tratamento de madeira com arseniato de cobre cromado (também conhecido como CCA ou TANALITH) foi inventado, e por décadas o tratamento foi a mais extensa utilização industrial de arsênico. Um aumento da apreciação da toxicidade do arsénico resultou numa proibição para o uso da CCA em produtos de consumo; a União Europeia e Estados Unidos iniciaram este processo em 2004. CCA continua em uso pesado em outros países, no entanto, por exemplo, plantações de borracha da Malásia.
O arsênico também foi usado em vários inseticidas agrícolas, rescisão e venenos. Por exemplo, arseniato de hidrogênio chumbo foi um inseticida em comum árvores de fruto, mas o contato com o composto, por vezes, resultou em danos cerebrais entre aqueles que trabalham os pulverizadores. Na segunda metade do século 20, arsenato monossódico de metilo (MSMA) e arseniato dissódico metilo (DSMA) - formas orgânicas menos tóxicas de arsênio - substituíram arseniato de chumbo na agricultura.
Arsénio ainda é adicionado a alimentos de origem animal, em particular em os EUA como um método de prevenção de doenças e estimulação do crescimento. Um exemplo é roxarsone, que é utilizado como um broiler arranque em cerca de 70% dos produtores de frangos de corte desde 1995. A Poultry Act-Veneno Livre de 2009 propõe a proibição do uso de roxarsone em suínos industrial e produção de aves. Alpharma, uma subsidiária da Pfizer Inc., que produz roxarsone, tem vendas da droga suspendido voluntariamente em resposta a estudos que mostram níveis elevados de arsênico em frangos tratados.
Uso médico
Durante os dias 18, 19 e do século 20, uma série de compostos de arsénio têm sido utilizados como medicamentos, incluindo arsphenamine (por Paul Ehrlich) e trióxido de arsênio (por Thomas Fowler). Bem como arsphénamine Neosalvarsan foi indicado para sífilis e tripanossomíase, mas foi substituído pelo modernos antibióticos . O trióxido de arsénio tem sido utilizado em uma variedade de maneiras ao longo dos últimos 500 anos, mas mais frequentemente no tratamento de cancro . Os EUA Food and Drug Administration em 2000. Este composto aprovado para o tratamento de pacientes com leucemia promielocítica aguda que é resistente aos ATRA. Também foi usado como A solução de Fowler em psoríase. Recentemente nova pesquisa foi feita na localização de tumores usando arsênico-74 (um emissor de positrões). As vantagens de usar este isótopo em vez do anteriormente utilizado iodo -124 é que o sinal no PET scan é mais claro como o corpo tende a transportar iodo na glândula tireóide produzindo muito barulho.
Em doses subtóxicos, compostos de arsénio solúveis actuar como estimulantes, e já foram populares em pequenas doses como medicina por pessoas em meados do século 18.
Alloys
A principal utilização de arsénio metálico é para liga de chumbo. Componentes de chumbo em baterias de carro são reforçadas pela presença de uma pequena percentagem de arsénico. Dezincification pode ser fortemente reduzida pela adição de arsénio para latão, uma liga de cobre-zinco. Arsenieto de gálio é um importante semicondutor material, utilizado em circuitos integrados . Circuitos feitos de GaAs são muito mais rápido (mas também muito mais caro) do que as feitas em silicone . Ao contrário de silício tem um bandgap directa, e por isso pode ser utilizado em diodos laser e LEDs para converter diretamente a eletricidade em luz .
Militar
Após a Primeira Guerra Mundial , os Estados Unidos construiu um arsenal de 20 mil toneladas de lewisite (ClCH = CHAsCl 2), um arma química que é um vesicant (agente blister) e irritante para o pulmão. O estoque foi neutralizada com água sanitária e despejados no Golfo do México após a década de 1950. Durante a Guerra do Vietnã o United States usado Azul agente, uma mistura de cacodilato de sódio e a sua forma de ácido, como um dos herbicidas do arco-íris para privar invadir soldados norte-vietnamitas de cobertura da folhagem e arroz.
Outros usos
- Acetoarsenito de cobre foi usado como um verde pigmento conhecido sob muitos nomes, incluindo " Paris Green 'e' verde esmeralda '. Isso causou numerosos envenenamentos arsênico. Verde de Scheele, um arseniato de cobre, foi usada no século 19 como um agente corante em doces.
- Também é usado em bronzeadores e pirotecnia.
- Até 2% de arsénico é usado em ligas de chumbo por tiros de chumbo e balas.
- O arsénio é adicionado em pequenas quantidades a alfa-bronze para torná-lo dezincification resistente. Este grau de bronze é usado para fazer acessórios sanitários ou outros itens que estão em constante contato com a água.
- O arsênico também é usado para preservação de amostras taxonômica.
- Até recentemente arsénio foi utilizado em vidro óptico. Fabricantes de vidro modernas, sob pressão de ambientalistas, removeu-o, juntamente com chumbo .
Papel biológico
Bactérias

Algumas espécies de bactérias obtêm sua energia por vários combustíveis oxidantes enquanto arseniato de redução a arsenito. Sob condições ambientais oxidativas algumas bactérias usar arsenito, o qual é oxidado para arsenate como combustível para o seu metabolismo. O enzimas envolvidas são conhecidas como reductases arsenate (arr).
Em 2008, foi descoberto que bactérias empregar uma versão da fotossíntese em ausência de oxigénio como com arsenitos doadores de elétrons, arseniatos produtores (apenas fotossíntese tão comum utiliza a água como doador de elétrons, produzindo oxigênio molecular). Pesquisadores conjecturar que, ao longo da história, estes organismos fotossintetizantes produziu os arseniatos que permitiram que as bactérias redutoras de arsenate para prosperar. Um estirpe PHS-1 foi isolado e está relacionada com a gammaproteobacterium Ectothiorhodospira shaposhnikovii. O mecanismo é desconhecido, mas uma enzima Arr codificado pode funcionar em sentido inverso à sua conhecida homólogos.
Apesar de arseniato e aniões de fosfato são semelhantes estruturalmente, não existe evidência para a substituição de fosfato de ATP ou ácidos nucleicos por arsénico.
Hereditariedade
Arsénio tem sido associada a mudanças epigenéticas, mudanças hereditárias na expressão gênica que ocorrem sem mudanças na Sequência de ADN. Estes incluem a metilação do DNA, histonas modificação, e Interferência de ARN. Níveis tóxicos de arsénico causar hypermethylation DNA significativo de genes supressores de tumor p16 e p53, aumentando assim o risco de carcinogênese. Estes eventos epigenética foram estudadas in vitro utilizando células de rim humano e, in vivo utilizando células de fígado de rato e leucócitos do sangue periférico de seres humanos. Espectrometria de massa com plasma indutivo acoplado (ICP-MS) é usada para detectar os níveis precisos de arsénio intracelular e as suas outras bases envolvidas na modificação epigenética de ADN. Estudos investigando o arsénio como um fator epigenético vai ajudar no desenvolvimento de biomarcadores precisos de exposição e susceptibilidade.
A samambaia freio Chinês ( Pteris vittata) hyperaccumulates arsénio presente no solo nas suas folhas e tem uma utilização proposta em fitorremediação.
Biomethylation
Arsênico inorgânico e seus compostos, ao entrar no cadeia alimentar, são progressivamente metabolizado através de um processo de metilação. Por exemplo, o molde Scopulariopsis brevicaulis produz quantidades significativas de trimetilarsina se arsênico inorgânico está presente. O composto orgânico arsenobetaine é encontrado em alguns alimentos marinhos tais como peixes e algas, e também em cogumelos em concentrações maiores. Ingestão da pessoa média é de cerca de 10-50 mg / dia. Valores relativos a 1000 � não são incomuns após o consumo de peixes ou cogumelos, mas há pouco perigo em comer peixe porque este composto arsênico é quase non-toxic.
Questões ambientais
Ocorrência na água potável
Contaminação por arsênico generalizada de águas subterrâneas levou a uma epidemia maciça de envenenamento por arsênico em Bangladesh e nos países vizinhos. Estima-se que aproximadamente 57 milhões de pessoas na Bacia Bengal está bebendo águas subterrâneas com concentrações de arsénio elevada acima da Organização Mundial de Saúde de padrão 10 's partes por bilhão (ppb). No entanto, um estudo sobre as taxas de câncer em Taiwan sugerido que aumentos significativos na mortalidade por câncer de aparecer apenas em níveis acima de 150 ppb. O arsénio na água subterrânea é de origem natural, e é libertado a partir do sedimento para as águas subterrâneas, devido ao condições anóxicas do subsolo. Esta água subterrânea começou a ser usado após locais e ocidentais ONGs eo governo de Bangladesh realizou um tubo raso maciça bem programa de água potável no final do século XX. Este programa foi projetado para evitar beber das águas superficiais contaminados por bactérias, mas não conseguiu testar para o arsénio na água subterrânea. Muitos outros países e distritos em Sudeste da Ásia, como Vietnã e Camboja têm ambientes geológicos favoráveis à geração de águas subterrâneas elevados de arsénio. Arsenicosis foi relatada em Nakhon Si Thammarat, Tailândia , em 1987, ea Chao Phraya River é suspeito de conter altos níveis de arsênico ocorrência natural dissolvido, mas não foi um problema de saúde pública devido ao uso de água engarrafada.
Nos Estados Unidos, o arsênico é mais comumente encontrado nas águas terrestres do sudoeste. Partes de Nova Inglaterra, Michigan, Wisconsin, Minnesota e os Dakotas também são conhecidos por terem concentrações significativas de arsênico na água subterrânea. Os níveis aumentados de câncer de pele têm sido associados com a exposição ao arsênio em Wisconsin, mesmo em níveis abaixo do padrão de água de 10 partes por bilhão beber, embora esta relação não foi comprovada. De acordo com um recente filme financiado por os EUA Superfund, milhões de poços particulares têm níveis de arsênico desconhecidos, e em algumas áreas de os EUA, mais de 20% dos poços podem conter níveis que excedem os limites estabelecidos.
Baixo nível de exposição ao arsênico em concentrações encontradas comumente em US água potável compromete a resposta imune inicial para H1N1 ou infecção da gripe suína de acordo com cientistas NIEHS-suportados. O estudo, realizado em ratos de laboratório, sugere que as pessoas expostas ao arsénio na água potável podem estar em risco aumentado para doença mais grave ou morte em resposta à infecção do vírus.
Alguns canadenses estão bebendo água que contém arsênico inorgânico. Águas poço cavado privados estão em maior risco para contendo arsênico inorgânico. Água de poço análises preliminares normalmente não faz teste de arsênico. Pesquisadores do Serviço Geológico do Canadá ter modelado variação relativa do potencial de risco arsênico natural para a província de New Brunswick. Este estudo tem implicações importantes para a água potável e saúde preocupações relativas ao arsénio inorgânico.
A evidência epidemiológica do Chile mostra uma ligação dose-dependente entre exposição ao arsênico crônica e várias formas de câncer, em especial quando outros fatores de risco, como o tabagismo, estão presentes. Estes efeitos foram demonstrados para persistir abaixo de 50 ppb.
Análise de múltiplos estudos epidemiológicos sobre exposição ao arsênico inorgânico sugere um aumento do risco pequeno, mas mensurável para câncer de bexiga em 10 ppb. De acordo com Peter Ravenscroft do Departamento de Geografia da Universidade de Cambridge, cerca de 80 milhões de pessoas em todo o mundo consomem entre 10 e 50 ppb de arsênico na água potável. Se todos eles consumida exatamente 10 ppb de arsênico na água potável, o já citado múltipla análise estudo epidemiológico poderia prever um adicional de 2.000 casos de câncer de bexiga sozinho. Isto representa uma sub-estimativa clara do impacto global, uma vez que não incluem pulmão ou o cancro da pele, e explicitamente subestima a exposição. Aqueles expostos a níveis de arsênico acima do atual padrão da OMS devem ponderar os custos e benefícios de remediação arsênico.
(1973) as avaliações iniciais de remoção de arsênico dissolvido por beber processos de tratamento de água demonstraram que o arsênico é muito eficazmente removido por co-precipitação com tanto ferro ou óxidos de alumínio. A utilização de ferro como coagulante, em particular, foi encontrada para remover arsénio com eficiências superiores a 90%. Vários sistemas de mídia de adsorção foram aprovados para uso de serviço de ponto-de-em um estudo financiado pela United States Environmental Protection Agency (EPA) eo National Science Foundation (NSF). Uma equipe de cientistas e engenheiros europeus e indianos criaram seis estações de tratamento de arsênio em Bengala Ocidental com base no método de remediação in-situ (Tecnologia SAR). Esta tecnologia não use quaisquer produtos químicos e arsênico é deixado como uma forma insolúvel (+5 estado) na zona subterrânea por recarregar as águas gaseificadas no aquífero e, assim, o desenvolvimento de uma zona de oxidação para apoiar arsênico oxidantes micro-organismos. Este processo não produz qualquer corrente de resíduos ou lamas e é relativamente barato.
Outro método eficaz e barato para remover arsênico de água de poço contaminada é afundar poços 500 pés ou mais profundas para chegar a águas mais puras. Um recente 2011 estudo financiado pelo Instituto Nacional de Programa de Pesquisa Superfund Ciências de Saúde Ambiental 'dos EUA mostra que sedimentos profundos pode remover arsênico e tirá-lo de circulação. Através deste processo chamado de adsorção em que varas de arsénio para as superfícies das partículas do sedimento profundas, o arsénio pode ser naturalmente removido do poço de água.
Separações magnéticas de arsênico em muito baixo campo magnético gradientes foram demonstradas no ponto de uso de purificação de água com elevada área de superfície e- monodispersa magnetita (Fe 3 O 4) nanocristais. Utilizando a área superficial específica elevada de Fe 3 O 4 nanocristais a massa de desperdício associado com a remoção de arsénio de água foi reduzido drasticamente.
Estudos epidemiológicos sugerem uma correlação entre o consumo crônico de água potável contaminada com arsênico ea incidência de todas as principais causas de mortalidade. A literatura fornece razão para acreditar exposição ao arsênico é causal na patogênese da diabetes.
Engenheiro húngara László Schremmer descobriu recentemente que pela utilização de filtros baseados em engodos que é possível reduzir o teor de arsénio da água para 3 ug / L. Isto é especialmente importante em áreas onde a água potável são fornecidos por filtração da água extraída do subsolo aqüífero.
Preservação da madeira em os EUA
A partir de 2002, as indústrias baseadas nos Estados Unidos consumiu 19.600 toneladas de arsênico. Noventa por cento deste foi utilizada para o tratamento de madeira com arseniato de cobre cromado (CCA). Em 2007, 50% das 5280 toneladas métricas de consumo foi ainda utilizado para este fim. Nos Estados Unidos, o voluntário phasing-out de arsênico na produção de produtos de consumo e produtos residenciais e de construção em geral de consumo começou em 31 de dezembro de 2003, e os produtos químicos alternativos são agora usados, como Alkaline Copper Quaternário, boratos, azol de cobre, ciproconazole, e propiconazole.
Embora interrompido, esta aplicação é também um dos mais preocupação para o público em geral. A grande maioria dos mais velhos madeira tratada com pressão foi tratada com CCA. CCA madeira ainda está em uso generalizado em muitos países, e foi muito usado durante a última metade do século 20 como uma estrutural e ao ar livre material de construção. Embora o uso do CCA madeira serrada foi proibido em muitas áreas após estudos que mostraram que o arsênico pode lixiviar para fora da madeira em torno do solo (a partir de equipamentos de playground, por exemplo), o risco também é apresentado pela queima de madeira mais velho CCA. A ingestão directa ou indirecta de cinzas de madeira queimada da madeira CCA tem causado mortes em animais e intoxicações graves no ser humano; a dose letal humana é cerca de 20 gramas de carbonato de sódio. Scrap CCA madeira de locais de construção e demolição podem ser inadvertidamente usado em incêndios comerciais e domésticos. Protocolos para a eliminação segura do CCA madeira não existem uniformemente por todo o mundo; há também a preocupação em alguns setores sobre a generalizada eliminação de aterros de tal madeira.
Mapeamento de lançamentos industriais em os EUA
Uma ferramenta que mapeia lançamentos de arsênico para determinados locais nos Estados Unidos e também fornece informações adicionais sobre esses lançamentos é TOXMAP. TOXMAP é um Sistema de Informação Geográfica (GIS) da Divisão de Serviços de Informação Especializada do United States National Library of Medicine (NLM) que usa mapas dos Estados Unidos para ajudar os usuários a explorar visualmente os dados do Agência de Estados Unidos de Proteção Ambiental (EPA) Toxics Release Inventory e Superfund Programas de investigação fundamental. TOXMAP é um recurso financiado pelo Governo Federal dos EUA. Informação química e saúde ambiental da TOXMAP é retirado de Toxicologia Rede de Dados do NLM (TOXNET) e PubMed e de outras fontes autorizadas.
Toxicidade e precauções
Arsénio e muitos de seus compostos são venenos especialmente potentes. Muitas fontes de água perto de minas estão contaminados por esses venenos. Nos Estados Unidos, a concentração máxima permitida na água potável é de 10 ppb e 5 ppb para a água engarrafada. Não há um padrão para o alimento, embora em 2012 a cobertura da imprensa solicitado chamadas para o desenvolvimento de tal. A República Popular da China tem um padrão alimentar.
Compostos de arsénico elementar e arsênico são classificados como " tóxico "e" perigoso para o ambiente "na União Europeia ao abrigo Directiva 67/548 / CEE. O Agência Internacional para a Investigação do Cancro (IARC) reconhece compostos de arsénio e arsénio como grupo 1 agentes cancerígenos, ea UE enumera trióxido de arsênio, pentóxido de arsénio e sais arsenate como categoria 1 agentes cancerígenos.
O arsénio é conhecido por causar arsenicosis devido à sua manifestação na água potável ", as espécies mais comuns sendo arsenate [Haso 2-
4; As (V)] e arsenito de [H 3 AsO 3; As (III)] ".
Tratamento
Tratamento de envenenamento por arsênico crônica é facilmente realizado. Anti-lewisite britânico ( dimercaprol) é prescrito em doses de 5 mg / kg até 300 mg a cada 4 horas para o primeiro dia, e depois a cada seis horas para o segundo dia e, finalmente, a cada 8 horas para 8 dias adicionais. No entanto, o EUA de Agência de Substâncias Tóxicas e Registro de Doenças (ATSDR) afirma que os efeitos a longo prazo da exposição ao arsênico não pode ser previsto. O sangue, urina, cabelo, unhas e pode ser testado para o arsénio; no entanto, esses testes não podem prever possíveis resultados de saúde a partir da exposição. A excreção ocorre na urina e de longa duração da exposição ao arsénio tem sido associada ao cancro da bexiga e renal, além disso para o cancro do fígado, da próstata, da pele, pulmões, e cavidade nasal.
Mecanismo biológico
A alta afinidade de arsénio óxidos (III) para tióis é geralmente designado como a causa da elevada toxicidade. Tióis, geralmente sob a forma de resíduos de cisteína, mas também em tais como cofactores ácido lipóico e coenzima A, estão situados nos sítios ativos de muitos importantes enzimas.
Arsénio interrompe ATP produção através de vários mecanismos. Ao nível do ciclo do ácido cítrico, ácido lipóico inibe o arsénio, o qual é um co-factor para piruvato desidrogenase. Além disso, através da competição com fosfato, arsenate desacopla fosforilação oxidativa, inibindo assim a redução ligados a energia de NAD +, respiração mitocondrial e síntese de ATP. Produção de peróxido de hidrogênio também é aumentado, o que, especula-se, tem potencial para formar espécies reativas de oxigênio e estresse oxidativo. Estas interferências metabólicas levar à morte de multi-sistema falha do órgão. Presume-se que a falha do órgão a ser a partir de morte celular por necrose, Não apoptose, uma vez que as reservas de energia têm sido muito empobrecido de apoptose a ocorrer.
A post mortem em uma morte envenenamento por arsênico revela de cor vermelha tijolo- mucosa, devido a grave hemorragia .
Apesar de arsênico causa toxicidade, também pode desempenhar um papel protetor.
