
Holmium
Sobre este escolas selecção Wikipedia
Crianças SOS oferecem um download completo desta seleção para as escolas para uso em escolas intranets. Você quer saber sobre o patrocínio? Veja www.sponsorachild.org.uk
| Holmium | |||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
67 Ho | |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| Aparência | |||||||||||||||||||||||||||||||||||||
branco prateado  | |||||||||||||||||||||||||||||||||||||
| Propriedades gerais | |||||||||||||||||||||||||||||||||||||
| Nome, símbolo, número | holmium, Ho, 67 | ||||||||||||||||||||||||||||||||||||
| Pronúncia | / h oʊ l m Eu ə m / HOHL -mee-əm | ||||||||||||||||||||||||||||||||||||
| Categoria elemento | lantanídeos | ||||||||||||||||||||||||||||||||||||
| Grupo, período, bloco | n / D, 6, f | ||||||||||||||||||||||||||||||||||||
| Peso atômico padrão | 164,93032 | ||||||||||||||||||||||||||||||||||||
| Configuração eletrônica | [ Xe ] 6s 4f 11 2 2, 8, 18, 29, 8, 2 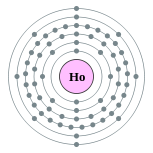 | ||||||||||||||||||||||||||||||||||||
| História | |||||||||||||||||||||||||||||||||||||
| Descoberta | Marc Delafontaine (1878) | ||||||||||||||||||||||||||||||||||||
| Propriedades físicas | |||||||||||||||||||||||||||||||||||||
| Fase | sólido | ||||||||||||||||||||||||||||||||||||
| Densidade (perto RT) | 8,79 g cm -3 · | ||||||||||||||||||||||||||||||||||||
| Líquido densidade no pf | 8,34 g cm -3 · | ||||||||||||||||||||||||||||||||||||
| Ponto de fusão | 1734 K , 1461 ° C, 2662 ° F | ||||||||||||||||||||||||||||||||||||
| Ponto de ebulição | 2993 K, 2720 ° C, 4928 ° F | ||||||||||||||||||||||||||||||||||||
| Calor de fusão | 17,0 kJ mol -1 · | ||||||||||||||||||||||||||||||||||||
| Calor de vaporização | 265 kJ mol -1 · | ||||||||||||||||||||||||||||||||||||
| Capacidade calorífica molar | 27,15 J · · mol -1 K -1 | ||||||||||||||||||||||||||||||||||||
| Pressão de vapor | |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| Propriedades atômicas | |||||||||||||||||||||||||||||||||||||
| Estados de oxidação | 3, 2, 1 ( óxido de base) | ||||||||||||||||||||||||||||||||||||
| Eletronegatividade | 1,23 (escala de Pauling) | ||||||||||||||||||||||||||||||||||||
| Energias de ionização | 1º: 581,0 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||
| Segunda: 1140 kJ mol -1 · | |||||||||||||||||||||||||||||||||||||
| 3: 2204 kJ · mol -1 | |||||||||||||||||||||||||||||||||||||
| Raio atômico | 176 pm | ||||||||||||||||||||||||||||||||||||
| O raio de covalência | 192 ± 19:00 | ||||||||||||||||||||||||||||||||||||
| Miscelânea | |||||||||||||||||||||||||||||||||||||
| A estrutura de cristal | hexagonal repleto de perto | ||||||||||||||||||||||||||||||||||||
| Ordenamento magnético | paramagnético | ||||||||||||||||||||||||||||||||||||
| Resistividade elétrica | ( RT) (poli) 814 Nco · m | ||||||||||||||||||||||||||||||||||||
| Condutividade térmica | 16.2 W · m -1 · K -1 | ||||||||||||||||||||||||||||||||||||
| Expansão térmica | ( RT) (poli) 11.2 uM / (mK) | ||||||||||||||||||||||||||||||||||||
| Velocidade do som (haste fina) | (20 ° C) 2.760 m · s -1 | ||||||||||||||||||||||||||||||||||||
| O módulo de Young | 64,8 GPa | ||||||||||||||||||||||||||||||||||||
| Módulo de cisalhamento | 26,3 GPa | ||||||||||||||||||||||||||||||||||||
| Massa de módulo | 40,2 GPa | ||||||||||||||||||||||||||||||||||||
| Rácio de Poisson | 0,231 | ||||||||||||||||||||||||||||||||||||
| Dureza de Vickers | 481 MPa | ||||||||||||||||||||||||||||||||||||
| Dureza Brinell | 746 MPa | ||||||||||||||||||||||||||||||||||||
| Número de registo CAS | 7440-60-0 | ||||||||||||||||||||||||||||||||||||
| A maioria dos isótopos estáveis | |||||||||||||||||||||||||||||||||||||
| Ver artigo principal: Isótopos de hólmio | |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
Holmium é um elemento químico com o símbolo Ho e número atómico 67. Parte da série dos lantanídeos , hólmio é um terra-rara. Holmium foi descoberto pelo químico sueco Per Theodor Cleve. Sua óxido foi isolado pela primeira vez a partir de minérios de terras raras em 1878 eo elemento foi nomeado após a cidade de Estocolmo.
Holmium elementar é um branco prateado relativamente macio e maleável do metal . É também para ser reactivo encontrado na natureza não combinada, mas quando isolado, é relativamente estável em ar seco, à temperatura ambiente. No entanto, ele reage com a água e oxida facilmente, e também irá queimar no ar quando aquecido.
Holmium é encontrado nos minerais monazita e gadolinita, e é geralmente comercialmente extraído de monazite utilizando técnicas de permuta iónica. Seus compostos na natureza, e em quase todo o seu laboratório de química, são trivalently oxidada, contendo íons Ho (III). Iões trivalentes hólmio têm propriedades fluorescentes semelhantes a muitos outros iões de terras raras (enquanto produzindo o seu próprio conjunto de linhas de emissão de luz originais), e iões de hólmio são assim usados da mesma maneira como algumas outras terras raras, em certas aplicações de laser e corantes de vidro.
Hólmio tem a maior força magnética de qualquer elemento e, portanto, é usado para o peças de pólos das mais fortes estáticos ímãs . Porque hólmio absorve fortemente neutrões, que também é usada em barras de controle nuclear.
Características
Propriedades físicas

Holmium é um elemento relativamente macio e maleável, que é bastante corrosão e resistente à estável em ar seco a temperatura padrão e pressão. No ar húmido e a altas temperaturas , no entanto, é rapidamente oxida, a formação de um óxido de cor amarelada. Na sua forma pura, holmium possui um metálico, brilho prateado brilhante.
Óxido Holmium tem algumas alterações de cor bastante dramáticas, dependendo das condições de iluminação. À luz do dia, é uma cor amarela tannish. Sob trichromatic luz, é um vermelho alaranjado impetuoso, quase confunde com o aspecto de óxido de érbio sob as mesmas condições de iluminação. A mudança está relacionada com as bandas de emissão afiadas dos iões trivalentes destes elementos, na qualidade de substâncias fosforescentes.
Hólmio tem a maior momento magnético (10,6 μ
B) de qualquer elemento natural e possui outras propriedades magnéticas incomuns. Quando combinado com ítrio , que forma altamente magnéticos compostos. Holmium é paramagnética em condições ambiente, mas é ferromagnético a temperaturas inferiores a 19 K .
Propriedades químicas
Holmium mancha de metal lentamente no ar e arde com facilidade para formar óxido de hólmio (III):
- 4 Ho + 3 O 2 → 2 Ho 2 O 3
Holmium é bastante electropositiva e é geralmente trivalente. Ele reage lentamente com água fria e bastante rapidamente com a água quente para formar hidróxido de hólmio:
- Ho 2 (s) + 6 H2O (l) → 2 Ho (OH) 3 (aq) + 3H 2 (g)
De metal Hólmio reage com todos os halogéneos:
- Ho 2 (s) + 3 F 2 (g) → 2 Hof 3 (s) [rosa]
- Ho 2 (s) + 3 Cl2 (g) → 2 HOCl 3 (s) [amarelo]
- Ho 2 (s) + 3 Br 2 (g) → 2 HOBr 3 (s) [amarelo]
- Ho 2 (s) + 3 I 2 (g) → 2 HoI 3 (s) [amarelo]
Hólmio dissolve prontamente em diluída de ácido sulfúrico para formar soluções contendo os (iii) iões Ho amarelo, que existem como uma [HO (OH 2) 9] 3+ complexos:
- Ho 2 (s) + 3 H 2 SO 4 (aq) → 2 Ho 3+ (aq) + SO 3 2-
4 (aq) + 3H 2 (g)
Estado de oxidação mais comum do Holmium é +3. Hólmio na solução está na forma de Ho 3+ rodeado por nove moléculas de água. Hólmio dissolve em ácidos.
Isótopos
Natural hólmio contém um estável isótopo , holmium-165. Alguns isótopos radioactivos sintéticos são conhecidos; o mais estável é o hólmio-163, com uma semi-vida de 4570 anos. Todos os outros radioisótopos tem estado fundamental metade não vive mais de 1,117 dias, ea maioria tem metade vive com menos de 3 horas. No entanto, o metastable 166 m1 Ho tem uma meia-vida de cerca de 1200 anos por causa de sua alta rodada. Este facto, em combinação com uma alta energia de excitação resultante num particularmente rico espectro de decaimento raios gama produzidos quando os de-excita estado metastable, faz com que este isótopo útil em física nuclear experiências como um meio para calibrar as respostas de energia e eficiências intrínsecas espectrômetros de raios gama.
História
Holmium (Holmia, Latin nome para Estocolmo ) foi descoberto por Marc e Delafontaine Jacques-Louis Soret em 1878 que percebeu o aberrante espectrográfica bandas de absorção do elemento então desconhecido (eles chamam de "Elemento X"). Mais tarde, em 1878, Per Teodor Cleve descobriu independentemente do elemento, enquanto ele estava trabalhando em érbia terra ( óxido de érbio).
Usando o método desenvolvido por Carl Gustaf Mosander, Cleve removeu primeiramente todos os contaminantes conhecidos de érbia. O resultado desse esforço foi dois novos materiais, um marrom e um verde. Ele nomeou a substância Holmia marrom (após o nome latino para a cidade de Cleve casa, Estocolmo) eo verde um Thulia. Holmia foi encontrado mais tarde para ser o óxido de hólmio e foi Thulia óxido de túlio. Em papel clássico de Henry Moseley em números atômicos, holmium foi atribuído um número atômico de 66. Evidentemente, a preparação holmium ele tinha sido dado para investigar tinha sido grosseiramente impuras, dominado pela vizinha (e unplotted) disprósio. Teria visto linhas de emissão de raios-X para ambos os elementos, mas assumido que os dominantes pertencia a hólmio, em vez da impureza disprósio.
Ocorrência e produção

Como todas as outras terras raras, o hólmio não é naturalmente encontrado como elemento livre. Ele ocorre combinado com outros elementos em gadolinite, monazita, e outros minerais de terras raras. As principais áreas de mineração são China , Estados Unidos , Brasil , Índia , Sri Lanka e Austrália , com reservas estimadas de holmium como 400.000 toneladas.
Holmium faz-se 1,4 partes por milhão da crosta terrestre em peso. Isso torna o elemento mais abundante 56 em crosta terrestre. Holmium torna-se uma parte por milhão dos solos , a 400 partes por quatrilhão de água do mar , e quase nenhum atmosfera da Terra . Holmium é raro para um dos lantanídeos. Faz-se 500 partes por trilhão do universo em peso.
É extraída comercialmente através de permuta de iões a partir de areia a monazite (0,05% hólmio) mas ainda é difícil separar outras terras raras. O elemento foi isolada a partir da redução do seu anidro cloreto ou fluoreto metálico com cálcio . Sua abundância estimada na Terra crosta é de 1,3 mg / kg. Holmium obedece ao Oddo-Harkins governar: como um elemento ímpar, é menos abundante do que o seu imediato de número par vizinhos, disprósio e érbio . No entanto, isso é o mais abundante dos pesados ímpares lantanídeos . A principal fonte de corrente são algumas das argilas ion-adsorção do sul da China. Algumas delas têm uma composição de terra-rara, semelhante à encontrada em . xenotime ou gadolinite ítrio torna-se cerca de dois terços do total, em peso; hólmio é em torno de 1,5%. Os próprios minérios originais são muito magra, talvez apenas 0,1% dos lantanídeos total, mas são facilmente extraído. Holmium é relativamente barato para um metal de terra rara com o preço de cerca de US $ 1000 por kg.
Aplicações

Hólmio tem a maior força magnética de qualquer elemento, e por isso é usada para criar o mais forte gerado artificialmente Os campos magnéticos, quando colocados dentro de alta resistência imans como uma peça de pólo magnético (também chamado de concentrador de fluxo magnético). Uma vez que pode absorver nêutrons produzidos-fissão nuclear, ele também é usado em barras de controle nuclear.
Holmium é usado em �rio- ferro - romã (YIG) - e �rio- lantânio -fluoreto (YLF) lasers de estado sólido encontrado em equipamentos de microondas (que por sua vez são encontrados em uma variedade de configurações de cuidados médicos e dentários). Holmium lasers emitem em 2,08 micrómetros, e, portanto, são seguros para os olhos. Eles são utilizados em aplicações médicas, dentais, e fibra-óptica.
Hólmio é um dos corantes utilizados para cúbicos de zircônia e vidro , proporcionando coloração amarela ou vermelha. Vidro contendo soluções de óxido de óxido de hólmio hólmio e (geralmente em ácido perclórico) tem picos de absorção óptica afiadas no intervalo espectral 200-900 nm. Eles são, portanto, utilizado como um padrão de calibração para espectrofotómetros ópticos, e estão disponíveis comercialmente.
Os radioactivos de longa vida, mas Ho-166 m1 (ver "isótopos" acima) é usado na calibração de espectrômetros de raios gama.
Papel biológico
Hólmio não desempenha nenhum papel biológico em seres humanos , mas os seus sais são capazes de estimular metabolismo. Os seres humanos tipicamente consomem cerca de um miligrama de holmium um ano. As plantas não são facilmente levar até holmium do solo. Alguns vegetais tiveram seu conteúdo holmium medido, e elevou-se a 100 partes por trilhão.
Toxicidade
Grandes quantidades de holmiium sais pode causar graves danos se inalada, consumida por via oral, ou injectado. Os efeitos biológicos de hólmio durante um longo período de tempo não são conhecidos. Holmium tem um baixo nível de toxicidade aguda.

